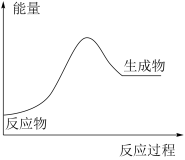
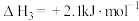下列有关说法中正确的是
| A.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)在低温下能自发进行,则该反应的△H<0 |
| B.NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的△H<0 |
| C.稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mo1-1则稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
| D.在合成氨工业中N2的量越多,H2的转化率越大,因此充入的N2越多越有利于NH3的合成 |
更新时间:2023/11/12 13:21:26
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知在稀溶液中强酸与强碱反应生成1 mol水时放出的热量,叫做中和热,下列说法中正确的是
| A.中和热的测定实验中需要用到的主要玻璃仪器有:两只大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒 |
| B.可以用保温杯来代替烧杯做有关测定中和热的实验 |
| C.在测定中和热的实验中,至少需要测定并记录的温度是2次 |
| D.测定中和热实验中,若所使用的稀NaOH溶液的物质的量稍大于稀盐酸,则会导致所测得的中和热数值偏高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,下列热化学方程式书写正确的是( )
A. Ba(OH)2(aq)+ Ba(OH)2(aq)+ H2SO4(aq)=== H2SO4(aq)=== BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
B.KOH(aq)+ H2SO4(aq)=== H2SO4(aq)=== K2SO4(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 K2SO4(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| C.2NaOH(aq)+H2SO4(aq)=== Na2SO4(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1 |
D.KOH(aq)+ H2SO4(浓)=== H2SO4(浓)=== K2SO4(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 K2SO4(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列热化学方程式书写正确的是(△H的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H= -1367.0kJ/mol (△H代表乙醇燃烧热) |
| B.H2SO4 (aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ/mol (△H代表中和热) |
| C.2H2(g)+O2(g)=2H2O(g) ΔH=- 483.6 kJ/mol (反应热) |
| D.C+O2=CO2 ΔH=-393.5 kJ/mol (反应热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列依据热化学方程式得出的结论正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) ΔH=a;2C(s)+O2(g)=2CO(g) ΔH=b,则a>b |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=483.6kJ·mol1,则氢气的燃烧热为241.8 kJ·mol1 |
| C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=57.3kJ·mol1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3 kJ |
| D.已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知强酸与强碱的稀溶液发生中和反应生成可溶性盐的热化学方程式可表示为

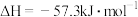 ,又知弱电解质的电离是吸热过程。向1L0.5
,又知弱电解质的电离是吸热过程。向1L0.5 的
的 溶液中分别加入下列物质:①稀醋酸、②浓硫酸、③稀硝酸,恰好完全反应时的焓变分别为
溶液中分别加入下列物质:①稀醋酸、②浓硫酸、③稀硝酸,恰好完全反应时的焓变分别为 、
、 、
、 ,则
,则 、
、 、
、 的关系是
的关系是


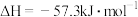 ,又知弱电解质的电离是吸热过程。向1L0.5
,又知弱电解质的电离是吸热过程。向1L0.5 的
的 溶液中分别加入下列物质:①稀醋酸、②浓硫酸、③稀硝酸,恰好完全反应时的焓变分别为
溶液中分别加入下列物质:①稀醋酸、②浓硫酸、③稀硝酸,恰好完全反应时的焓变分别为 、
、 、
、 ,则
,则 、
、 、
、 的关系是
的关系是A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法错误的是
A.一定温度下,反应MgCl2(l) Mg(l)+ Cl2(g)的△H>0,△S>0 Mg(l)+ Cl2(g)的△H>0,△S>0 |
| B.△H<0,△S>0的反应在温度低时不能自发进行 |
| C.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| D.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) △H=+185.57kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】科研人员利用Cu/ZnO作催化剂,在光照条件下实现了CO2和H2合成CH3OH,该反应历程示意图如下:
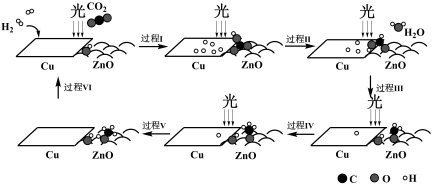
下列说法错误的是

下列说法错误的是
| A.过程I中光能为化学键的断裂提供能量 | B.过程Ⅱ中存在极性共价键的断裂与形成 |
| C.经历反应Ⅴ后,氢原子的总数减少 | D.在常温常压下,总反应的ΔS<0 |
您最近一年使用:0次



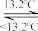 Sn(白,s)
Sn(白,s)