电化学在化工、冶金、机械、电子、航空、航天、轻工、仪表、医学、材料、能源、金属腐蚀与防护、环境科学等科技领域获得了广泛的应用。
Ⅰ.电解精炼镓的装置如图所示,粗镓含 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为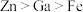 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
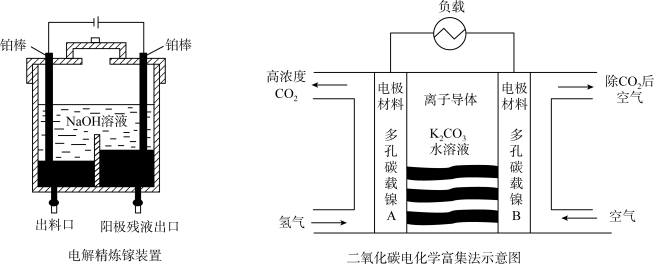
(1)电解后,电解槽底部阳极泥中所含的金属有_____ 。
(2)电解过程中阴极的电极反应式是_____ 。
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中, 向多孔碳载镍
向多孔碳载镍_____ (填“A”或“B”)电极移动。
(4)负极的电极反应式是_____ 。
(5)在多孔碳载镍A电极上消耗1
 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是_____ L。
Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。
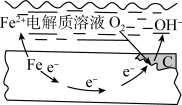
(6)钢铁吸氧腐蚀的正极反应式是_____ 。
(7)下列关于金属腐蚀的防护说法正确的是_____ 。
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
Ⅰ.电解精炼镓的装置如图所示,粗镓含
 、
、 、
、 杂质,已知镓(
杂质,已知镓( )的化学性质与铝(
)的化学性质与铝( )相似,金属活动性顺序为
)相似,金属活动性顺序为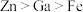 ,镓(
,镓( )的熔点为29.8℃。
)的熔点为29.8℃。
(1)电解后,电解槽底部阳极泥中所含的金属有
(2)电解过程中阴极的电极反应式是
Ⅱ.载人航天器中的物质和能源资源十分宝贵,二氧化碳的富集与转化是氧气再生的核心问题,电化学富集二氧化碳的方法如图所示。回答下列问题:
(3)离子导体中,
 向多孔碳载镍
向多孔碳载镍(4)负极的电极反应式是
(5)在多孔碳载镍A电极上消耗1

 ,理论上多孔碳载镍B电极转化的
,理论上多孔碳载镍B电极转化的 在标准状况下的体积是
在标准状况下的体积是Ⅲ.日常生活中使用的金属往往含有杂质,当这样的金属与潮湿的空气或者电解质溶液接触时,会在其表面的杂志附近形成许多微小的原电池而被腐蚀。钢铁吸氧腐蚀的原理如图所示。

(6)钢铁吸氧腐蚀的正极反应式是
(7)下列关于金属腐蚀的防护说法正确的是
①用电镀的方法,在钢铁制品表面镀上一层不易被腐蚀的金属,能够减缓金属的腐蚀。
②镀铜铁制品镀层受损后,铁制品比受损前更易生锈。
③改变金属内部组成、结构可以防止金属腐蚀。
④牺牲阳极保护法是将被保护的金属作正极,以一种活动性较强的金属作负极。
⑤外加电流阴极保护法是将被保护的金属作阴极,惰性电极作辅助阳极,连接直流电源。
23-24高二上·河南郑州·期中 查看更多[2]
更新时间:2023-11-14 07:13:35
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
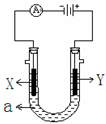
(1)若X、Y都是石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:①电解池中X极上的电极反应式为_______________________ ,在X极附近观察到的现象是___________________ 。
②Y电极上的电极反应式为__________________________ ,一段时间后电解质溶液中看到的实验现象是_________________________ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_______________ ,电极反应式是______________________ 。
②Y电极的材料是______________ ,电极反应式是__________________ 。(说明:杂质发生的电极反应不必写出)

(1)若X、Y都是石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】电解饱和食盐水的反应为2NaCl+2H2O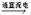 Cl2↑+H2↑+2NaOH。
Cl2↑+H2↑+2NaOH。
(1)在上述方程式上标出电子转移的方向和数目_____ 。
(2)该反应中被氧化的元素是_____ 。阴极产物之一为H2,阴极上发生的变化为____ 反应(选填“氧化”、“还原”)。
(3)电解产物氯气既能作氧化剂,也能作还原剂。下列反应中氯气只作氧化剂的是___ (填写编号)。
a.Cl2+2KI→2KCl+I2
b.Cl2+ 2NaOH →NaCl + NaClO + H2O
c.CuCl2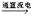 Cl2↑+ Cu
Cl2↑+ Cu
d.3Cl2+ 2Fe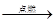 2FeCl3
2FeCl3
 Cl2↑+H2↑+2NaOH。
Cl2↑+H2↑+2NaOH。(1)在上述方程式上标出电子转移的方向和数目
(2)该反应中被氧化的元素是
(3)电解产物氯气既能作氧化剂,也能作还原剂。下列反应中氯气只作氧化剂的是
a.Cl2+2KI→2KCl+I2
b.Cl2+ 2NaOH →NaCl + NaClO + H2O
c.CuCl2
 Cl2↑+ Cu
Cl2↑+ Cu d.3Cl2+ 2Fe
 2FeCl3
2FeCl3
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】银锌电池广泛用作于各种电子仪器的电源。它的充电放电过程可表示为:2Ag+Zn(OH)2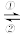 Ag2O +Zn+H2O,
Ag2O +Zn+H2O,
回答下列有关问题:
(1)电池的放电过程是________ (填“①”或“②”)。
(2)该电池属于________ (填“酸”“碱”或“中”)性电池。
(3)反应①是________ (填“放热”或“吸热”)反应。
(4)写出充电时的电极反应式:
阳极:______________________ ,
阴极:______________________ 。
(5)充电时,电池的阳极应接电源的________ 极。
 Ag2O +Zn+H2O,
Ag2O +Zn+H2O,回答下列有关问题:
(1)电池的放电过程是
(2)该电池属于
(3)反应①是
(4)写出充电时的电极反应式:
阳极:
阴极:
(5)充电时,电池的阳极应接电源的
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

(1)充电时,原电池的负极与电源__ 极相连,B极的电极反应式为__ ,A极的电极反应式为__ 。
(2)放电时,负极的电极反应式为__ 。
(3)在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2___ L(标准状况下)。
(4)若在常温常压下,1gCH3OH(l)燃烧生成CO2和液态H2O时放热22.68kJ,表示甲醇燃烧热的热化学方程式为___ 。

(1)充电时,原电池的负极与电源
(2)放电时,负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2
(4)若在常温常压下,1gCH3OH(l)燃烧生成CO2和液态H2O时放热22.68kJ,表示甲醇燃烧热的热化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
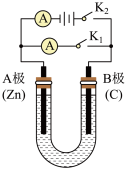
【推荐2】如图所示,U形管内盛有150mL的溶液,按要求回答下列问题:
(1)打开K2,闭合K1,若所盛溶液为稀硫酸,则B极为___________ 极(填电极名称),该装置的能量转化形式为:__________ ,B极的电极反应式为:______________________ 。
(2)打开K1,闭合K2,若所盛溶液为NaCl溶液,一段时间后U形管内溶液的pH___________ (填“变大”、“不变”或“变小”),总反应的化学方程式是:______________________ 。若要使U形管内溶液恢复到起始状态,应向U形管内的溶液加入(或通入)___________ 。
(3)如果要在铁块上镀上铜,打开K1,闭合K2,电解液选用CuSO4溶液,则A电极的材料应换成是___ (填“铁块”或“纯铜”),反应一段时间后电解质溶液中Cu2+的浓度将会_____ (填“增大”、“减小”或“不变”)。
(1)打开K2,闭合K1,若所盛溶液为稀硫酸,则B极为
(2)打开K1,闭合K2,若所盛溶液为NaCl溶液,一段时间后U形管内溶液的pH
(3)如果要在铁块上镀上铜,打开K1,闭合K2,电解液选用CuSO4溶液,则A电极的材料应换成是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】燃料电池具有广阔的发展前途,科学家近年研制出一种微型的燃料电池,采用甲醇取代氢气做燃料可以简化电池设计,该电池有望取代传统电池。某学生在实验室利用碱性甲醇燃料电池电解Na2SO4溶液。
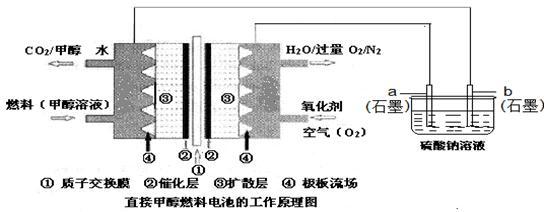
请根据图示回答下列问题:
(1)图中a电极是______ (填“正极”、“负极”、“阴极”或“阳极”)。该电极上发生的电极反应式为_________________________________________ 。
(2)碱性条件下,通入甲醇的一极发生的电极反应式为____________________________ 。
(3)当消耗3.36 L氧气时(已折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是__ 。
(4)25℃、101kPa时,燃烧16g甲醇生成CO2和H2O(l),放出的热量为363.26kJ,写出甲醇燃烧的热化学方程式:_________________________________________ 。

请根据图示回答下列问题:
(1)图中a电极是
(2)碱性条件下,通入甲醇的一极发生的电极反应式为
(3)当消耗3.36 L氧气时(已折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是
(4)25℃、101kPa时,燃烧16g甲醇生成CO2和H2O(l),放出的热量为363.26kJ,写出甲醇燃烧的热化学方程式:
您最近半年使用:0次
【推荐1】在日常生活中,金属腐蚀的现象普遍存在,金属腐蚀常常是自发进行的。回答下列问题:
(1)钢铁腐蚀分为析氢腐蚀和吸氧腐蚀:
①在酸性环境中,主要发生的腐蚀称为___________ (填“析氢”或“吸氧”)腐蚀,此时正极上的电极反应式为___________ 。
②发生吸氧腐蚀时,每转移0.2mol电子,消耗气体的体积为___________ mL(标准状况下)。
(2)钢铁的保护法如图所示:___________ (填“牺牲阳极保护法”或“外加电流法”),此时锌板上发生的电极反应为___________ 。
②图2中,a为电源的___________ (填“正”或“负”)极,判断的理由为___________ 。
(1)钢铁腐蚀分为析氢腐蚀和吸氧腐蚀:
①在酸性环境中,主要发生的腐蚀称为
②发生吸氧腐蚀时,每转移0.2mol电子,消耗气体的体积为
(2)钢铁的保护法如图所示:
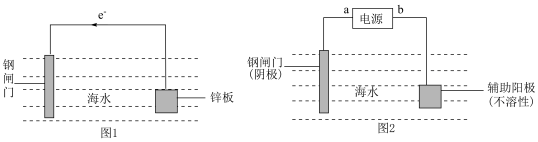
②图2中,a为电源的
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①②③三种不同的环境中
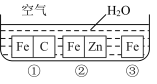
请回答:
(1)金属腐蚀主要分为__________ 腐蚀和_____________ 腐蚀两种。
(2)铁被腐蚀的速率由快到慢的顺序是_________________ (填序号)。
(3)①中正极的电极反应式为_________________________________________________ ,②中负极的电极反应式为_________________________________________ 。
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有__________ (填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接

请回答:
(1)金属腐蚀主要分为
(2)铁被腐蚀的速率由快到慢的顺序是
(3)①中正极的电极反应式为
(4)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】取6根铁钉,6支干净的试管及其他材料,如图所示。
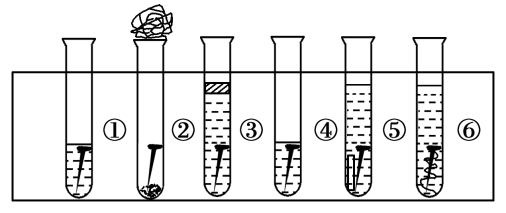
试管①放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管②在试管底部放入硅胶(是一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触;
试管③先放入一根铁钉,趁热倒入煮沸的蒸馏水(已赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触;
试管④中放入铁钉注入食盐水,使铁钉和空气及食盐水接触;
试管⑤放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片;
试管⑥放入相连的铁钉和铜丝,注入自来水,浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况。
(1)上述实验中铁钉发生了电化学腐蚀的是____ (填试管序号);在电化学腐蚀中,负极反应是____ ,正极反应是______ 。
(2)从铁钉被腐蚀的情况可知引起和促进铁钉被腐蚀的条件是_________ 。
(3)为防止铁的锈蚀,工业上普遍采用的方法是____________ (答两种方法)。

试管①放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管②在试管底部放入硅胶(是一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触;
试管③先放入一根铁钉,趁热倒入煮沸的蒸馏水(已赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触;
试管④中放入铁钉注入食盐水,使铁钉和空气及食盐水接触;
试管⑤放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片;
试管⑥放入相连的铁钉和铜丝,注入自来水,浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况。
(1)上述实验中铁钉发生了电化学腐蚀的是
(2)从铁钉被腐蚀的情况可知引起和促进铁钉被腐蚀的条件是
(3)为防止铁的锈蚀,工业上普遍采用的方法是
您最近半年使用:0次



