已知几种元素的性质或原子结构的相关叙述如表所示,回答下列问题。
(1)元素X的一种同位素用作相对原子质量的标准,这种同位素的原子符号是___________ 。X的另一种同位素可用来测定文物所属年代,这种同位素的原子符号是___________ 。
(2)Y形成的另一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是___________ 。
(3)元素Z在海水中含量非常高,海水中含Z元素的化合物主要是___________ (填化学式),电离方程式为___________ 。
(4)画出T的原子结构示意图:___________ 。
(5)由X元素组成的单质在Y元素组成的常见单质中完全燃烧,生成的产物用足量的氢氧化钠溶液吸收,反应的化学方程式为___________ 。
| 元素编号 | 元素性质或原子结构的相关叙述 |
| T | 失去一个电子后形成与Ne相同的核外电子排布 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其某种单质是空气的主要成分,也是最常见的助燃剂 |
| Z | 原子核外有3个电子层,最外层比次外层少1个电子 |
(2)Y形成的另一种单质,主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)元素Z在海水中含量非常高,海水中含Z元素的化合物主要是
(4)画出T的原子结构示意图:
(5)由X元素组成的单质在Y元素组成的常见单质中完全燃烧,生成的产物用足量的氢氧化钠溶液吸收,反应的化学方程式为
更新时间:2023-11-16 11:37:59
|
相似题推荐
填空题
|
适中
(0.65)
真题
【推荐1】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为__________ 、_________ ;
(2)XZ2与YZ2分子的立体结构分别是_________ 和_________ ,相同条件下两者在水中的溶解度较大的是_________ (写分子式),理由是_________ ;
(3)Q的元素符号是_________ ,它属于第_________ 周期,它的核外电子排布式为_________ ,在形成化合物时它的最高化合价为_________ ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键_________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q的元素符号是
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5,则两种水溶液中由水电离出的 浓度之比是
浓度之比是___________ 。
(2)A、B、D、E四种元素组成的某高中常见的无机化合物,受热易分解。写出少量该化合物溶液与足量的 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(3)A、B、D、E四种元素组成的某高中常见的无机化合物浓度为0.1mol/L时,常温下pH最接近___________(填序号)。
(4)在一个装有可移动活塞的容器中进行如下反应: ,反应达到平衡后,测得容器中含有
,反应达到平衡后,测得容器中含有 0.5mol,
0.5mol, 0.2mol,
0.2mol,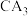 0.2mol,总容积为1.0L。
0.2mol,总容积为1.0L。
①如果达成此平衡前各物质起始的量有以下几种可能,其中不合理的是___________ (填序号)。
A. 0.6mol,
0.6mol, 0.5mol,
0.5mol,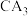 0mol
0mol
B. 0mol,
0mol, 0mol,
0mol,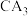 1.2mol
1.2mol
C. 0.6mol/L,
0.6mol/L, 0.5mol/L,
0.5mol/L,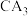 0.2mol/L
0.2mol/L
②求算此平衡体系的平衡常数
___________ 。
③如果保持温度和压强不变,向上述平衡体系中加入0.18mol ,平衡将
,平衡将___________ (填“正向”、“逆向”或“不”)移动。
④已知0.4mol液态 与足量的液态双氧水反应,生成
与足量的液态双氧水反应,生成 和水蒸气,放出256.65kJ的热量。写出该反应的热化学方程式
和水蒸气,放出256.65kJ的热量。写出该反应的热化学方程式___________ 。
(1)常温下,X、Y的水溶液的pH均为5,则两种水溶液中由水电离出的
 浓度之比是
浓度之比是(2)A、B、D、E四种元素组成的某高中常见的无机化合物,受热易分解。写出少量该化合物溶液与足量的
 溶液反应的离子方程式:
溶液反应的离子方程式:(3)A、B、D、E四种元素组成的某高中常见的无机化合物浓度为0.1mol/L时,常温下pH最接近___________(填序号)。
| A.5.6 | B.7.0 | C.8.4 | D.13.0 |
 ,反应达到平衡后,测得容器中含有
,反应达到平衡后,测得容器中含有 0.5mol,
0.5mol, 0.2mol,
0.2mol,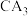 0.2mol,总容积为1.0L。
0.2mol,总容积为1.0L。①如果达成此平衡前各物质起始的量有以下几种可能,其中不合理的是
A.
 0.6mol,
0.6mol, 0.5mol,
0.5mol,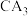 0mol
0molB.
 0mol,
0mol, 0mol,
0mol,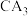 1.2mol
1.2molC.
 0.6mol/L,
0.6mol/L, 0.5mol/L,
0.5mol/L,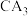 0.2mol/L
0.2mol/L②求算此平衡体系的平衡常数

③如果保持温度和压强不变,向上述平衡体系中加入0.18mol
 ,平衡将
,平衡将④已知0.4mol液态
 与足量的液态双氧水反应,生成
与足量的液态双氧水反应,生成 和水蒸气,放出256.65kJ的热量。写出该反应的热化学方程式
和水蒸气,放出256.65kJ的热量。写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示是元素周期表的一部分,根据①~⑩在周期表中的位置按题目要求回答:

(1)在元素①~⑩中,非金属性最强的元素是__ (填元素名称)。
(2)在元素⑥~⑩中,离子半径最小的元素的离子结构示意图为__ 。
(3)元素⑥⑦⑧的最高价氧化物对应的水化物,按碱性从强到弱的顺序排列是__ (用化学式表示)。
(4)用电子式表示元素①和③形成的化合物甲的形成过程__ 。
(5)为验证ⅦA族部分元素非金属性的递变规律,设计了如图所示装置进行实验,请回答:

①实验室制取单质⑩的化学反应方程式__ 。
②A中发生反应的离子方程式是__ 。
③棉花中浸有的NaOH溶液的作用是(用离子方程式表示)__ 。
④为验证溴与碘非金属性强弱:通入一定量⑩的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到__ 。
⑤通过此实验,某同学得到结论:“溴比碘非金属性强”,这一说法是否正确,请说明理由___ 。
⑥化合物乙、丙均由①④⑥⑨四种元素组成,请写出乙与丙发生反应的离子反应方程式___ 。

(1)在元素①~⑩中,非金属性最强的元素是
(2)在元素⑥~⑩中,离子半径最小的元素的离子结构示意图为
(3)元素⑥⑦⑧的最高价氧化物对应的水化物,按碱性从强到弱的顺序排列是
(4)用电子式表示元素①和③形成的化合物甲的形成过程
(5)为验证ⅦA族部分元素非金属性的递变规律,设计了如图所示装置进行实验,请回答:

①实验室制取单质⑩的化学反应方程式
②A中发生反应的离子方程式是
③棉花中浸有的NaOH溶液的作用是(用离子方程式表示)
④为验证溴与碘非金属性强弱:通入一定量⑩的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
⑤通过此实验,某同学得到结论:“溴比碘非金属性强”,这一说法是否正确,请说明理由
⑥化合物乙、丙均由①④⑥⑨四种元素组成,请写出乙与丙发生反应的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下列物质中,互为同系物的有_______ ,互为同分异构体的有_______ ,互为同素异形体的有_______ ,属于同位素的有_______ ,是同一种物质的有_______ 。
①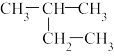 ②白磷;③2,3-二甲基丁烷;④
②白磷;③2,3-二甲基丁烷;④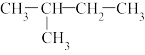 ;⑤
;⑤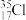 ;⑧红磷;⑦
;⑧红磷;⑦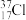 ;⑧
;⑧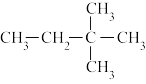
(2)已知2-甲基-1,3-丁二烯可与溴水发生加成反应,按要求作答:
①发生1,2-加成所得有机产物的结构简式为_______ ;
②发生1,4-加成反应的化学方程式为_______ 。
(1)下列物质中,互为同系物的有
①
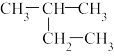 ②白磷;③2,3-二甲基丁烷;④
②白磷;③2,3-二甲基丁烷;④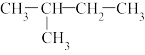 ;⑤
;⑤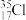 ;⑧红磷;⑦
;⑧红磷;⑦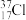 ;⑧
;⑧
(2)已知2-甲基-1,3-丁二烯可与溴水发生加成反应,按要求作答:
①发生1,2-加成所得有机产物的结构简式为
②发生1,4-加成反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据要求回答下列问题:
I. ①H、D、T ②H2O、D2O ③石墨、金刚石 ④ 和
和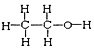
四组微粒或物质中,互为同位素的是_______ ;(填序号,下同) 互为同素异形体的是_____ 。
II.现有①金刚石 ②干冰 ③Na2SO4 ④NH4Cl 四种物质,按下列要求回答:
(1)晶体熔化时需要破坏共价键的是_____ (填序号,下同);
(2)熔点最低的是_______
(3)晶体中只存在一种微粒作用力是_______ ;
(4)属于离子晶体的是________ 。
I. ①H、D、T ②H2O、D2O ③石墨、金刚石 ④
 和
和
四组微粒或物质中,互为同位素的是
II.现有①金刚石 ②干冰 ③Na2SO4 ④NH4Cl 四种物质,按下列要求回答:
(1)晶体熔化时需要破坏共价键的是
(2)熔点最低的是
(3)晶体中只存在一种微粒作用力是
(4)属于离子晶体的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】物质的量是学习化学的基础。
(1)19g某二价金属的氯化物 中含有
中含有 ,金属A的相对原子质量是
,金属A的相对原子质量是___________ 。
(2)现有标准状况下CO和 混合气体6.72L,其质量为10g,则此混合气体中,CO和
混合气体6.72L,其质量为10g,则此混合气体中,CO和 的物质的量之比是
的物质的量之比是___________ 。
(3)将 的氯化钡溶液与
的氯化钡溶液与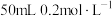 的氯化钠溶液混合,若不考虑溶液混合时体积的变化,则混合溶液中氯离子的浓度是
的氯化钠溶液混合,若不考虑溶液混合时体积的变化,则混合溶液中氯离子的浓度是___________ 。
(4)若将 通入热的烧碱溶液中,可以发生如下两个反应:
通入热的烧碱溶液中,可以发生如下两个反应: 和
和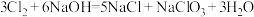 。从氧化还原角度分析
。从氧化还原角度分析 表现了氧化性、还原性,当混合液中
表现了氧化性、还原性,当混合液中 和
和 的个数比为15:2时,混合液中
的个数比为15:2时,混合液中 和
和 的个数比为
的个数比为___________ 。
(5)碘是人体必需的微量元素之一,国家规定在食盐中添加碘的标准为20-30mg/kg。已知碘的一种核素是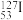 ,则该原子的中子数是
,则该原子的中子数是___________
(6)把27g含镁、铝、铜的合金粉末分为两等份,一份放入过量氢氧化钠溶液中,得到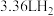 (标准状况),另一份放入过量盐酸中,得到
(标准状况),另一份放入过量盐酸中,得到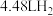 (标准状况)。该合金中镁、铝、铜的物质的量之比为___________
(标准状况)。该合金中镁、铝、铜的物质的量之比为___________
(7)已知MHCl=36.5g/mol浓盐酸的密度为 ,质量分数为36.5%,则浓盐酸的物质的量浓度为
,质量分数为36.5%,则浓盐酸的物质的量浓度为___________
(1)19g某二价金属的氯化物
 中含有
中含有 ,金属A的相对原子质量是
,金属A的相对原子质量是(2)现有标准状况下CO和
 混合气体6.72L,其质量为10g,则此混合气体中,CO和
混合气体6.72L,其质量为10g,则此混合气体中,CO和 的物质的量之比是
的物质的量之比是(3)将
 的氯化钡溶液与
的氯化钡溶液与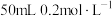 的氯化钠溶液混合,若不考虑溶液混合时体积的变化,则混合溶液中氯离子的浓度是
的氯化钠溶液混合,若不考虑溶液混合时体积的变化,则混合溶液中氯离子的浓度是(4)若将
 通入热的烧碱溶液中,可以发生如下两个反应:
通入热的烧碱溶液中,可以发生如下两个反应: 和
和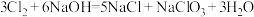 。从氧化还原角度分析
。从氧化还原角度分析 表现了氧化性、还原性,当混合液中
表现了氧化性、还原性,当混合液中 和
和 的个数比为15:2时,混合液中
的个数比为15:2时,混合液中 和
和 的个数比为
的个数比为(5)碘是人体必需的微量元素之一,国家规定在食盐中添加碘的标准为20-30mg/kg。已知碘的一种核素是
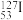 ,则该原子的中子数是
,则该原子的中子数是(6)把27g含镁、铝、铜的合金粉末分为两等份,一份放入过量氢氧化钠溶液中,得到
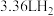 (标准状况),另一份放入过量盐酸中,得到
(标准状况),另一份放入过量盐酸中,得到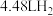 (标准状况)。该合金中镁、铝、铜的物质的量之比为___________
(标准状况)。该合金中镁、铝、铜的物质的量之比为___________| A.2:1:3 | B.2:4:1 | C.1:2:3 | D.3:2:4 |
 ,质量分数为36.5%,则浓盐酸的物质的量浓度为
,质量分数为36.5%,则浓盐酸的物质的量浓度为
您最近一年使用:0次



