NaCl是一种化工原料,可以制备一系列物质,如图所示。

(1)下列说法不正确的是___________(填字母)。
(2)Cl2与Ca(OH)2反应的化学方程式为___________ 。
(3)84消毒液(含次氯酸钠)不能与洁厕剂(含盐酸)混合使用,否则可能产生使人中毒的气体,请解释其原因___________ (用化学反应方程式表示)。
(4)纯净的氢气在氯气中燃烧的现象是___________ 。
(5)实验室常用浓盐酸和MnO2加热制备氯气,请写出该反应的离子方程式___________ 。

(1)下列说法不正确的是___________(填字母)。
| A.Na2CO3的热稳定性比NaHCO3强 |
| B.侯氏制碱法可以制得Na2CO3 |
| C.图示转化反应都是氧化还原反应 |
| D.焰色试验中需用硫酸洗净铁丝,并灼烧至与原来的火焰颜色相同为止 |
(2)Cl2与Ca(OH)2反应的化学方程式为
(3)84消毒液(含次氯酸钠)不能与洁厕剂(含盐酸)混合使用,否则可能产生使人中毒的气体,请解释其原因
(4)纯净的氢气在氯气中燃烧的现象是
(5)实验室常用浓盐酸和MnO2加热制备氯气,请写出该反应的离子方程式
更新时间:2023-10-05 10:54:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学源于生活,下列物质为生活中常见的日用品,括号内为对应物品的主要成分或有效成分。
①食盐(NaCl) ②食醋( ) ③结晶苏打(
) ③结晶苏打( ) ④双氧水(
) ④双氧水( ) ⑤高锰酸钾消毒液(
) ⑤高锰酸钾消毒液( ) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)
) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)
回答下列问题:
(1)以上物质的主要成分或有效成分属于盐的是________ (填序号)。
(2)若要鉴别某白色晶体是食盐还是结晶苏打,可以用________ (填序号)来鉴别,若白色固体是结晶苏打,观察到的现象是________ 。
(3)酸性 和
和 会发生如下反应:
会发生如下反应:______
________ ________
________ ________
________ ________
________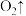 (配平上述方程式)。
(配平上述方程式)。
(4)在清洗卫生间时,84消毒液和洁厕灵不能混合使用,用离子方程式表示其原因:________ 。
(5)家庭厨卫管道内常因毛发、菜渣、纸棉纤维等而造成堵塞,请用化学方程式表示管道疏通剂的疏通原理:________ 。
①食盐(NaCl) ②食醋(
 ) ③结晶苏打(
) ③结晶苏打( ) ④双氧水(
) ④双氧水( ) ⑤高锰酸钾消毒液(
) ⑤高锰酸钾消毒液( ) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)
) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)回答下列问题:
(1)以上物质的主要成分或有效成分属于盐的是
(2)若要鉴别某白色晶体是食盐还是结晶苏打,可以用
(3)酸性
 和
和 会发生如下反应:
会发生如下反应:________
 ________
________ ________
________ ________
________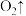 (配平上述方程式)。
(配平上述方程式)。(4)在清洗卫生间时,84消毒液和洁厕灵不能混合使用,用离子方程式表示其原因:
(5)家庭厨卫管道内常因毛发、菜渣、纸棉纤维等而造成堵塞,请用化学方程式表示管道疏通剂的疏通原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在第一次世界大战期间,有一次德军与英、法军在比利时对峙,黎明时,英、法军前线战壕的士兵突然看到一股黄绿色气体逐渐袭来,很快数百名英、法军战士窒息而死。后来人们在打扫战场时,发现跑到山坡上的士兵竟幸免于难。
(1)由上述事例可归纳出氯气的性质有_______ 。
(2)写出下列反应的化学方程式,并用单线桥法表示出反应中电子转移情况。
①铁丝在氯气中燃烧:_______ 。
②铁粉溶于盐酸中:_______ 。
(3)将新鲜的花瓣放入干燥的氯气中可观察到的现象是_______ , 原因是_______ 。
(4)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸_______ , 反应的化学方程式为_______ 。
(1)由上述事例可归纳出氯气的性质有
(2)写出下列反应的化学方程式,并用单线桥法表示出反应中电子转移情况。
①铁丝在氯气中燃烧:
②铁粉溶于盐酸中:
(3)将新鲜的花瓣放入干燥的氯气中可观察到的现象是
(4)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精、含氯消毒剂、过氧乙酸等可有效灭活病毒。回答下列问题:
(1)Cl2是最早用于饮用水消毒的物质,主要是利用Cl2溶于水生成的次氯酸灭活病毒。
①Cl2与水反应的化学方程式为_______ 。
②氯水经光照后酸性增强,用化学方程表示其原因:_______ 。
(2)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。
①漂白液的有效成分为_______ 。
②它的消毒原理是_______ (用化学方程式表示)。
③由以上反应证明 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸_______ 。
④工业生产漂白粉的化学方程式为_______ 。
(3)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8gNa2O2中阴离子的物质的量为_______ 。
(4)将 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为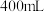 。试计算:
。试计算:
①原混合物中 的质量为
的质量为_______  。
。
②所得溶液的物质的量浓度为_______  。
。
(1)Cl2是最早用于饮用水消毒的物质,主要是利用Cl2溶于水生成的次氯酸灭活病毒。
①Cl2与水反应的化学方程式为
②氯水经光照后酸性增强,用化学方程表示其原因:
(2)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。
①漂白液的有效成分为
②它的消毒原理是
③由以上反应证明
 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸④工业生产漂白粉的化学方程式为
(3)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8gNa2O2中阴离子的物质的量为
(4)将
 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为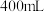 。试计算:
。试计算:①原混合物中
 的质量为
的质量为 。
。②所得溶液的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
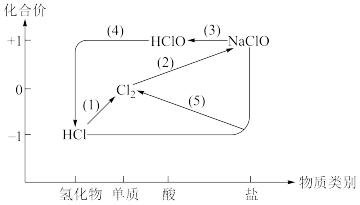
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了___________ 反应
(2)制备84消毒液的化学方程式为___________ 。
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为___________ 。
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为___________ 。
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为___________ (用离子反应方程式表示)。
 通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
通入NaOH溶液制备84消毒液(有效成分为NaClO),利用氯及其化合物的“价类”二维图表示其中涉及的各物质之间的转化关系 。回答下列问题:
(1)实验室用二氧化锰和浓盐酸反成制备氯气,在制取Cl2的反应中,浓盐酸发生了
(2)制备84消毒液的化学方程式为
(3)84消毒液中加入少量醋酸(CH3COOH)可增强效果,该反应的化学方程式为
(4)次氯酸不稳定,光照条件下易分解。该反应的化学方程式为
(5)84消毒液不能与洁厕剂(含盐酸)一起混合使用的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组对钠及其化合物进行实验探究。
(1)由于金属钠很容易跟空气中的___________ (填化学式)等物质反应,通常将它保存在___________ 里。
(2)将一小块Na投入到盛有适量水的烧杯中,反应的离子方程式为___________ 。反应放出大量热,依据的现象是___________ 。
(3)将氯气通入加热中的钠,反应的化学方程式为___________ 。
(4) 常做供氧剂,其与
常做供氧剂,其与 反应的化学方程式为
反应的化学方程式为___________ 。
(5)加热 固体发生反应的化学方程式为
固体发生反应的化学方程式为___________ 。
(1)由于金属钠很容易跟空气中的
(2)将一小块Na投入到盛有适量水的烧杯中,反应的离子方程式为
(3)将氯气通入加热中的钠,反应的化学方程式为
(4)
 常做供氧剂,其与
常做供氧剂,其与 反应的化学方程式为
反应的化学方程式为(5)加热
 固体发生反应的化学方程式为
固体发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】医疗机构常用质量分数为7.45% 的次氯酸钠消毒液(密度为1.00 g·cm−3)进行消毒,回答下列问题:
(1)该消毒液的物质的量浓度为_______ mol·L−1(保留到小数点后2位)。
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液_______ mL;量取时若仰视,所配溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”)。
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是_______ 。
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式_______ ;蘸有NaOH溶液的脱脂棉吸收黄绿色气体的离子方程式是_______ 。
(1)该消毒液的物质的量浓度为
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请完成下列问题:
(1)画出氯原子结构示意图___ 。
(2)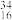 S2-微粒中的质子数是
S2-微粒中的质子数是___ ,中子数是___ 。
(3)49g硫酸的物质的量为___ mol,其完全电离产生H+的个数为___ 。
(4)写出实验室制氯气的离子方程式:___ 。
(1)画出氯原子结构示意图
(2)
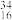 S2-微粒中的质子数是
S2-微粒中的质子数是(3)49g硫酸的物质的量为
(4)写出实验室制氯气的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列化学用语填空:
(1)水分子的电子式_______ ;S2-的离子结构示意图_______ 。
(2)短周期元素原子半径最大的元素(不考虑稀有气体)_______ (用元素符号表示)。
(3)实验室制氯气的离子方程式_______ 。
(4)铜与稀硝酸反应,装置上部有红棕色气体产生的原因(用化学方程式表示)_______ 。
(5)盛放NaOH溶液的试剂瓶为什么不能用玻璃瓶塞(用化学方程式表示)_______ 。
(1)水分子的电子式
(2)短周期元素原子半径最大的元素(不考虑稀有气体)
(3)实验室制氯气的离子方程式
(4)铜与稀硝酸反应,装置上部有红棕色气体产生的原因(用化学方程式表示)
(5)盛放NaOH溶液的试剂瓶为什么不能用玻璃瓶塞(用化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠元素在自然界都以化合物的形式存在。
(1)过氧化钠中氧元素的化合价为_______ 价,焰色试验为_______ 色(填颜色)。
(2)过氧化钠用于呼吸面具的反应方程式为①_______ ,②_______ 。上述反应中,从氧化还原的角度分析,过氧化钠的作用是_______ 。
(3)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为_______ 。

(4)若要除去碳酸钠固体中的碳酸氢钠,发生反应的化学方程为_______ 。
(1)过氧化钠中氧元素的化合价为
(2)过氧化钠用于呼吸面具的反应方程式为①
(3)利用下图比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

(4)若要除去碳酸钠固体中的碳酸氢钠,发生反应的化学方程为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式是___________ ,俗称____________ ,其水溶液显_______ 性(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为_____________ 。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者_________ 后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为__________________________ 。
(1)碳酸氢钠的化学式是
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,图1为钠的价类二维图:请回答以下问题:

(1)图1中缺失的物质类别是___________ ,利用如图2实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ ,写出实验过程中试管中发生反应的化学方程式:___________ 。
(2)能说明热稳定性碳酸钠比碳酸氢钠强的实验现象是___________ 、___________
(3)向 300mL 某物质的量浓度的 NaOH 溶液中缓慢通入一定量的 CO2 (忽略溶液体积的变化),充分反应后,得到Na2CO3 和NaHCO3 的混合溶液。向上述所得溶液中,逐滴滴加1molL1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
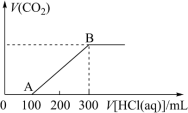
①AB段发生反应的离子方程式___________ ;
②原溶液中,溶质Na2CO3 和 NaHCO3 物质的量之比为___________ 。

(1)图1中缺失的物质类别是
(2)能说明热稳定性碳酸钠比碳酸氢钠强的实验现象是
(3)向 300mL 某物质的量浓度的 NaOH 溶液中缓慢通入一定量的 CO2 (忽略溶液体积的变化),充分反应后,得到Na2CO3 和NaHCO3 的混合溶液。向上述所得溶液中,逐滴滴加1molL1的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:

①AB段发生反应的离子方程式
②原溶液中,溶质Na2CO3 和 NaHCO3 物质的量之比为
您最近一年使用:0次



