下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究钠在氧气中燃烧所得固体成分 | 取少量加热后的固体粉末,加入少量蒸馏水 | 若有气泡产生,则证明燃烧后的固体粉末为Na2O2 |
| B | 比较KMnO4、Cl2 和Fe3+的氧化性 | 向酸性 KMnO4 溶液中滴入 FeCl2溶液,紫红色溶液变浅并伴有黄绿色气体产生 | 氧化性强弱:KMnO4>Cl2>Fe3+ |
| C | 制备 Fe(OH)3胶体 | 向沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。用红色激光笔照射液体 | 若产生一条光亮的“通路”,则得到Fe(OH)3 胶体 |
| D | 检验某溶液中是否存在K+ | 用玻璃棒蘸取待测液放在酒精灯外焰上灼烧,观察火焰的颜色 | 若看到火焰为黄色,则一定不存在 K+ |
| A.A | B.B | C.C | D.D |
更新时间:2023-11-27 15:52:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验装置或对实验的描述不正确的是


| A.装置①为配制一定浓度的溶液时的定容操作 |
| B.装置②可用于实验室制备Fe(OH)3胶体 |
C.装置③验证 与水反应的热量变化 与水反应的热量变化 |
| D.装置④可以较长时间看到Fe(OH)2白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关元素及其化合物的叙述正确的是( )
| A.Fe( OH)3胶体无色、透明,能发生丁达尔现象 |
| B.CO2通入CaCl2溶液中生成CaCO3沉淀 |
| C.将稀硫酸滴加到Fe( NO3)2溶液中无明显现象 |
| D.H2、SO2、CO2三种气体都可以用浓硫酸干燥 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向 CuSO4 溶液中逐滴加入 KI 溶液至过量,观察到产生白色沉淀 CuI,溶液变为棕黄色.再向反应后的混合物中不断通入SO2 气体,溶液逐渐变成无色.下列分析正确的是( )
| A.滴加KI 溶液时,转移1mol e﹣ 时生成1 mol 白色沉淀 |
| B.滴加KI 溶液时,反应的离子方程式:Cu2++3I﹣═CuI↓+I2 |
| C.通入SO2后溶液逐渐变成无色,体现了SO2 的漂白性 |
| D.上述实验条件下,物质的还原性:Cu2+>I2>SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】比较法是研究物质性质的重要方法,下列性质比较中错误的是
A.碱性: | B.分散质粒子直径:氢氧化铁胶体>硫酸铜溶液 |
| C.熔点:铝合金>铝 | D.氧化性: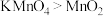 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验方案不能达到目的是
A.用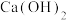 溶液鉴别 溶液鉴别 溶液和 溶液和 溶液 溶液 |
B.用丁达尔效应鉴别 胶体和 胶体和 溶液 溶液 |
C.用饱和 溶液除去 溶液除去 中混有的HCl 中混有的HCl |
D.用焰色反应鉴别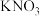 固体和NaCl固体 固体和NaCl固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关实验操作或反应现象的叙述中正确的是
| A.在氢氧化钠溶液中滴入氯化铁饱和溶液,用于制备氢氧化铁胶体 |
| B.进行焰色试验时,若实验室无铂丝或铁丝,可以用玻璃棒代替 |
| C.用玻璃棒蘸取少量新制氯水点在pH试纸上,并与标准比色卡对照,测定其pH |
| D.将足量二氧化硫通入滴有酚酞的氢氧化钠溶液中,溶液褪色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列解释实验事实的离子方程式正确的是
A.工业上制漂白粉: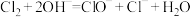 |
B.用 溶液腐蚀铜线路板: 溶液腐蚀铜线路板: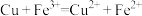 |
C. 溶液中滴加少量的 溶液中滴加少量的 : :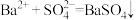 |
D. 与 与 反应制备 反应制备 : :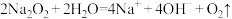 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用如图所示装置进行下列实验:将①中溶液逐滴滴入②中,预测的现象不合理的是(尾气装置略)
| 选项 | ①中物质 | ②中的物质 | 预测②中的现象 | 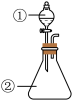 |
| A | 乙醛溶液 | 酸性高锰酸钾溶液 | 瓶中紫色溶液逐渐褪色 | |
| B | 70%硫酸 | 亚硫酸钠粉末 | 白色粉末逐渐溶解,有气泡产生 | |
| C | 稀盐酸 | 碳酸钠饱和溶液 | 立即产生大量气泡 | |
| D | 蒸馏水 | 过氧化钠粉末 | 产生气泡,滴加酚酞溶液后先变红后褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液蒸干
溶液蒸干 饱和溶液,持续续加热,并不断搅拌
饱和溶液,持续续加热,并不断搅拌 胶体
胶体
 溶液的pH
溶液的pH
 2NaOH+ H2↑+Cl2↑
2NaOH+ H2↑+Cl2↑ 溶液滴入
溶液滴入 溶液中
溶液中 通入饱和氨盐水中
通入饱和氨盐水中 通入酸性
通入酸性 溶液中
溶液中

