现有下列物质:①硫磺、②金刚砂、③酒精、④小苏打、⑤NaHSO4固体、⑥Na2O2、⑦氨气、⑧稀硝酸、⑨四氯化碳,选序号填入下列空格:
(1)属于电解质的是___________ ;
(2)属于共价化合物的是___________ ;
(3)既含有离子键又含有共价键的是___________ ;
(4)熔化破坏共价键的___________ ;
(5)写出属于酸式盐的物质在水溶液中反应的离子方程式:___________ ;
(6)分别写出⑥、⑨的电子式___________ 、___________ 。
(1)属于电解质的是
(2)属于共价化合物的是
(3)既含有离子键又含有共价键的是
(4)熔化破坏共价键的
(5)写出属于酸式盐的物质在水溶液中反应的离子方程式:
(6)分别写出⑥、⑨的电子式
更新时间:2023/10/25 22:50:42
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】以下是物质的组成、分类以及符号表征.
I.请按要求回答以下问题
(1)相同质量的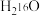 与超重水
与超重水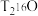 所含中子数之比为
所含中子数之比为______ ,与足量金属钠反应产生的气体在相同状况下的质量比为______ 。
Ⅱ.下列变化:① 溶于水;②酒精溶于水;③
溶于水;②酒精溶于水;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥碘升华;⑦
溶于水;⑥碘升华;⑦ 受热分解;⑧氨气液化;⑨
受热分解;⑧氨气液化;⑨ 熔化;⑩
熔化;⑩ 熔化
熔化
(2)以上变化过程所涉及到的物质中,只含有共价键的是______ (填相对应的序号,下同),属于共价化合物的是______ 。
(3)以上变化没有化学键被破坏的是______ ,只有离子键被破坏的是______ (填序号)。
(4)⑦中物质的电子式为用电子式表示______ ,③中物质的形成过程______ 。
I.请按要求回答以下问题
(1)相同质量的
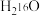 与超重水
与超重水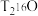 所含中子数之比为
所含中子数之比为Ⅱ.下列变化:①
 溶于水;②酒精溶于水;③
溶于水;②酒精溶于水;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥碘升华;⑦
溶于水;⑥碘升华;⑦ 受热分解;⑧氨气液化;⑨
受热分解;⑧氨气液化;⑨ 熔化;⑩
熔化;⑩ 熔化
熔化(2)以上变化过程所涉及到的物质中,只含有共价键的是
(3)以上变化没有化学键被破坏的是
(4)⑦中物质的电子式为用电子式表示
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】磷酸和亚磷酸(H3PO3)是磷元素的两种含氧酸。亚磷酸与NaOH反应只生成NaHPO3和NaH2PO3两种盐,则H3PO3的结构式为___________ ,其为___________ 元酸,原因是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)汞的原子结构示意图 ,汞在周期表中位于第
,汞在周期表中位于第__________ 周期。
(2) 、
、 、
、 分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是
分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是___________ 。
(3)下列有关性质的比较能用元素周期律解释的是_______ 。
a.酸性: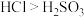
b.非金属性:
c.碱性: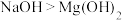
d.热稳定性:
(4)硒( )与硫位于同一主族,均是生命必需元素。下列推断正确的是
)与硫位于同一主族,均是生命必需元素。下列推断正确的是___________ 。
a.硒元素的最低负化合价为 价
价
b.二氧化硒( )具有还原性
)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为___________ 。
②X的氢化物的电子式___________ 。
 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)汞的原子结构示意图
 ,汞在周期表中位于第
,汞在周期表中位于第(2)
 、
、 、
、 分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是
分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:
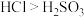
b.非金属性:

c.碱性:
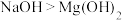
d.热稳定性:

(4)硒(
 )与硫位于同一主族,均是生命必需元素。下列推断正确的是
)与硫位于同一主族,均是生命必需元素。下列推断正确的是a.硒元素的最低负化合价为
 价
价b.二氧化硒(
 )具有还原性
)具有还原性c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为
②X的氢化物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钛及其合金在航空航天、生物医学等领域具有非常重要的应用价值和广阔的应用前景,可通过下面的转化制取:
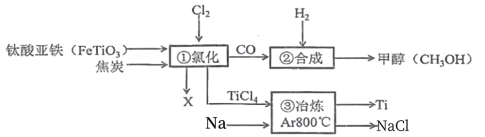
(1)反应①的化学方程式为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为____ ,发生氧化反应的物质为____ 。
(2)反应②中,若在标准状况下有5.6LCO参与反应,则转移电子数为____ ,反应②中生成的甲醇属于____ 。
A.氧化物 B.碱 C.有机物 D.电解质 E.非电解质
(3)“反应③”须在无氧和非水性 溶剂中进行,原因是____ 。写出反应③的化学方程式并用双线桥法 表示该反应电子转移的方向和数目____ 。

(1)反应①的化学方程式为:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X为
(2)反应②中,若在标准状况下有5.6LCO参与反应,则转移电子数为
A.氧化物 B.碱 C.有机物 D.电解质 E.非电解质
(3)“反应③”须在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有以下物质:①氮气 ②液态CO2 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔融的KNO3 ⑨NaOH溶液,请回答下列问题(填序号):
(1)以上物质能导电的是_______ 。
(2)以上物质中属于电解质的是_______ 。
(1)以上物质能导电的是
(2)以上物质中属于电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列物质:①纯H2SO4、②KHSO4固体、③盐酸、④氢氧化铁胶体、⑤冰醋酸、⑥熔融MgCl2、⑦石墨、⑧蔗糖溶液、⑨Ba(OH)2固体、⑩氨水。
(1)上述状态下可导电的物质是__________ (填序号,下同),属于电解质的是__________ 。
(2)0.1mol/L的①②③⑤溶液中水电离出的氢离子浓度的大小关系:__________ 。
(3)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。
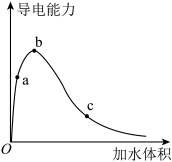
a、b、c三点CH3COOH的电离程度的大小关系为__________ ;a、b、c三点溶液用1 mol/LNaOH溶液中和,消耗NaOH溶液体积的大小关系为__________ 。
(4)常温下,现有同体积pH=10的⑨⑩的溶液,根据题目条件回答下列问题。
a.同等程度稀释⑨⑩溶液,下列数值会减小的是__________ 。
A.c(OH-) B . C.
C. 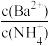 D.
D. 
b.将⑨⑩分别用同浓度的盐酸中和,消耗的盐酸的量:⑨___ ⑩(填“>”“<”或“=”)。
c.将体积为Va、pH=10的⑨溶液,与体积为Vb、pH=3的盐酸溶液混合后,pH等于5,则Va:Vb=______ 。
(1)上述状态下可导电的物质是
(2)0.1mol/L的①②③⑤溶液中水电离出的氢离子浓度的大小关系:
(3)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

a、b、c三点CH3COOH的电离程度的大小关系为
(4)常温下,现有同体积pH=10的⑨⑩的溶液,根据题目条件回答下列问题。
a.同等程度稀释⑨⑩溶液,下列数值会减小的是
A.c(OH-) B .
 C.
C. 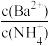 D.
D. 
b.将⑨⑩分别用同浓度的盐酸中和,消耗的盐酸的量:⑨
c.将体积为Va、pH=10的⑨溶液,与体积为Vb、pH=3的盐酸溶液混合后,pH等于5,则Va:Vb=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列物质:① N2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl。
(1)只由非极性键构成的物质是__________________ (填编号)。
(2)由离子键和极性键构成的物质是_______________ 。
(3)⑤H2O2的电子式为:_________________ 。
(4)用电子式表示⑥MgF2的形成过程:______________ 。
(5)下列说法不正确的是________ 。
①共价化合物中含共价键,也可能含离子键
②因为H2CO3酸性<H2SO3酸性,所以非金属性C<S
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤熔融状态能导电的物质是离子化合物
⑥由分子组成的化合物中一定存在共价键
A. ①③⑤ B. ①②⑥ C. ①②④⑤ D. ①③⑤⑥
(1)只由非极性键构成的物质是
(2)由离子键和极性键构成的物质是
(3)⑤H2O2的电子式为:
(4)用电子式表示⑥MgF2的形成过程:
(5)下列说法不正确的是
①共价化合物中含共价键,也可能含离子键
②因为H2CO3酸性<H2SO3酸性,所以非金属性C<S
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤熔融状态能导电的物质是离子化合物
⑥由分子组成的化合物中一定存在共价键
A. ①③⑤ B. ①②⑥ C. ①②④⑤ D. ①③⑤⑥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用下列各组物质序号填空:
①O2和O3; ②1H、2H、3H; ③NH4C1; ④N2;⑤BaCl2; ⑥H2SO4; ⑦K2O
(1)互为同位素的是__________________ ;(2)互为同素异形体的是__________________ ;
(3)属于共价化合物的是______________ ;(4)含有共价键的离子化合物是______________ 。
①O2和O3; ②1H、2H、3H; ③NH4C1; ④N2;⑤BaCl2; ⑥H2SO4; ⑦K2O
(1)互为同位素的是
(3)属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空
(1)在①Ar、②N2、③SiO2、④K2S、⑤NH4Cl五中物质中,只存在共价键的是___________ ;只存在离子键的是___________ ;既有离子键,又有共价键的是___________ ;不存在化学键的是___________
(2)将Ba(OH)2•8H2O晶体研细后与NH4Cl晶体一起放入烧杯中,用玻璃棒快速搅拌,闻到有刺激性气味的气体产生,此反应为___________ (“吸热”或“放热”)反应,反应的方程式为___________
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,则负极材料是_______ (写名称),正极电极反应为________ ;溶液中 向
向_________ 极移动
(4)工业合成氨缓解了有限耕地与不断增长的人口对粮食大量需求之间的矛盾。已知拆开1mol化学键所需要的能量叫键能。相关键能数据如表:
结合表中所给信息,计算生成2molNH3时_______ (填“吸收”或“放出”)的热量是______ kJ。
(1)在①Ar、②N2、③SiO2、④K2S、⑤NH4Cl五中物质中,只存在共价键的是
(2)将Ba(OH)2•8H2O晶体研细后与NH4Cl晶体一起放入烧杯中,用玻璃棒快速搅拌,闻到有刺激性气味的气体产生,此反应为
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,则负极材料是
 向
向(4)工业合成氨缓解了有限耕地与不断增长的人口对粮食大量需求之间的矛盾。已知拆开1mol化学键所需要的能量叫键能。相关键能数据如表:
| 共价键 | H﹣H | N≡N | N﹣H |
| 键能(kJ•mol-1) | 436.0 | 945.0 | 391.0 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3.请回答下列问题:
(1)Na3N的电子式是___________ ,该化合物由___________ 键形成。
(2)Na3N与盐酸反应生成___________ 种盐,其电子式是___________ 。
(3)比较Na3N中两种微粒的半径:r(Na+)___________ r(N3-)。(填“>”“=”或“<”)
(1)Na3N的电子式是
(2)Na3N与盐酸反应生成
(3)比较Na3N中两种微粒的半径:r(Na+)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.(1)某种铵根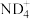 中的中子数是
中的中子数是_____ ,核外电子数是_____ 。
(2)下列装置能够组成原电池的是____ 。
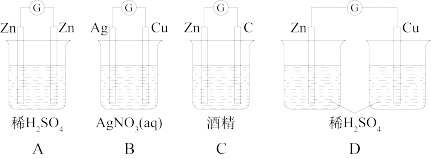
(3)已知拆开1molH—H键、1molI—I、1molH—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要____ (填“放出”或“吸收”)____ kJ的热量。
(4)用电子式表示CS2的形成过程:____ 。
Ⅱ.(1)下列物质:A.CO2 B.H2O2 C.He D.CuSO4•5H2O E.NH4Cl F.Na2O2 G.Al2O3
①既含有离子键又含有共价键的是____ ;(填序号,下同);
②既存在非极性共价键又存在极性共价键的是_______ 。
(2)下列变化:①碘的升华,②冰融化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解,化学键未被破坏的是____ ;仅共价键被破坏的是____ 。
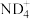 中的中子数是
中的中子数是(2)下列装置能够组成原电池的是

(3)已知拆开1molH—H键、1molI—I、1molH—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要
(4)用电子式表示CS2的形成过程:
Ⅱ.(1)下列物质:A.CO2 B.H2O2 C.He D.CuSO4•5H2O E.NH4Cl F.Na2O2 G.Al2O3
①既含有离子键又含有共价键的是
②既存在非极性共价键又存在极性共价键的是
(2)下列变化:①碘的升华,②冰融化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解,化学键未被破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据要求回答下列问题:
I. 写出下列物质或微粒的电子式:
(1)CO2_________________
(2)N2__________________
(3) Na2O_____________
(4)NaOH________________
II. 下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答)_____________
含有共价键的共价化合物是(用序号回答)_______________
(2)当其熔化时,不破坏化学键的是(用序号回答)______________ .
I. 写出下列物质或微粒的电子式:
(1)CO2
(2)N2
(3) Na2O
(4)NaOH
II. 下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答)
含有共价键的共价化合物是(用序号回答)
(2)当其熔化时,不破坏化学键的是(用序号回答)
您最近一年使用:0次



