某实验小组用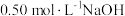 溶液和
溶液和 硫酸溶液进行反应热的测定,实验装置如图所示。
硫酸溶液进行反应热的测定,实验装置如图所示。
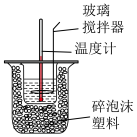
(1)装置中碎泡沫塑料的作用是___________ 。
(2)写出该反应中和热的热化学方程式已知:生成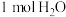 时放出的热量为
时放出的热量为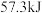 :
:___________ 。
(3)取 溶液和
溶液和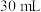 硫酸溶液进行实验,实验数据如表所示。
硫酸溶液进行实验,实验数据如表所示。
①近似认为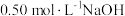 溶液和
溶液和 硫酸溶液的密度都是
硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 。则生成
。则生成 时的反应热
时的反应热
___________ (取小数点后一位)。
②上述实验数值结果与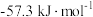 有偏差,产生偏差的原因不可能是
有偏差,产生偏差的原因不可能是___________ (填字母)。
a.实验装置保温、隔热效果差
b.量取 溶液的体积时仰视读数
溶液的体积时仰视读数
c.分多次把 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中
d.用温度计测定 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
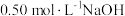 溶液和
溶液和 硫酸溶液进行反应热的测定,实验装置如图所示。
硫酸溶液进行反应热的测定,实验装置如图所示。
(1)装置中碎泡沫塑料的作用是
(2)写出该反应中和热的热化学方程式已知:生成
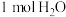 时放出的热量为
时放出的热量为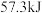 :
:(3)取
 溶液和
溶液和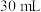 硫酸溶液进行实验,实验数据如表所示。
硫酸溶液进行实验,实验数据如表所示。| 温度 次数 | 起始温度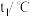 | 终止温度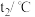 | 温度差平均值 | ||
 |  | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 |
| 2 | 27.0 | 27.1 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.1 | 26.2 | 26.3 | 30.1 | |
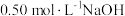 溶液和
溶液和 硫酸溶液的密度都是
硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 。则生成
。则生成 时的反应热
时的反应热
②上述实验数值结果与
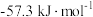 有偏差,产生偏差的原因不可能是
有偏差,产生偏差的原因不可能是a.实验装置保温、隔热效果差
b.量取
 溶液的体积时仰视读数
溶液的体积时仰视读数c.分多次把
 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中d.用温度计测定
 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
更新时间:2023-10-28 22:08:19
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】某校化学社2019年1月3日一吨多重的嫦娥四号探测器首次实现人类飞行器在月球背面的软着陆,它所搭载的“玉兔二号”月球车通过砷化镓(GaAs)太阳能电池提供能量开展工作。
Ⅰ.如图是As、Ga等元素所在元素周期表中的一部分
(1)上表中,原子半径最小的是___________ 元素,元素周期表中砷的位置是___________
(2)GaN、GaAs、GaP都是良好的半导体材料,晶体类型与晶体硅相同,它们的熔点如下表:
解释它们熔点变化的原因___________
(3)亚磷酸(H3PO3)与NaOH反应只能生成Na2HPO3和NaH2PO3两种盐,这两种盐溶液均呈碱性。根据以上信息判断,亚磷酸应属于___________ 酸(几元+强\弱酸),Na2HPO3溶液中阴离子浓度由大到小的次序为___________
Ⅱ.现有W、X、Y、Z、Q、R六种短周期主族元素,它们的原子序数依次增大,Z与Q同主族,且Z的氢化物常温时为液态。W、X的最外层电子数之和与Y的最外层电子数相等,W分别与X、Y、Z形成电子总数相等的分子。
(4)写出XZ2的电子式___________ ,元素R在周期表中的位置___________ 。
(5)X、Z、Q元素的氢化物的沸点最低的是___________ (用化学式表示)。
(6)Y4气态分子结构如图所示,已知断裂1molY-Y吸收167kJ的热量,生成1molY≡Y放出942kJ热量。试写出由Y4气态分子变成Y2态分子的热化学方程式___________ 。
Ⅲ.下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:
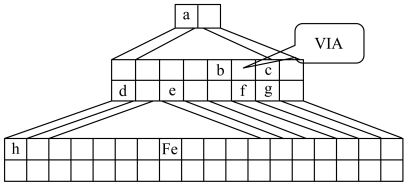
(7)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑___________ 。
(8)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH:___________ 。
(9)下列叙述正确的是___________
A.f与d形成离子化合物为电解质,故该晶体能导电。
B.c、f、g电负性强弱顺序为:g>f>c。
C.第一电离能:f>g>h>d
D.c与h形成化合物的水溶液显中性。
E.硒化氢的稳定性强于f的氢化物的稳定性。
F.h的最高价氧化物对应的水化物是一种强碱。
Ⅰ.如图是As、Ga等元素所在元素周期表中的一部分
| Al | Si | P |
| Ga | Ge | As |
(1)上表中,原子半径最小的是
(2)GaN、GaAs、GaP都是良好的半导体材料,晶体类型与晶体硅相同,它们的熔点如下表:
| 晶体 | GaN | GaAs | GaP |
| 熔点/℃ | 1700 | 1238 | 1480 |
(3)亚磷酸(H3PO3)与NaOH反应只能生成Na2HPO3和NaH2PO3两种盐,这两种盐溶液均呈碱性。根据以上信息判断,亚磷酸应属于
Ⅱ.现有W、X、Y、Z、Q、R六种短周期主族元素,它们的原子序数依次增大,Z与Q同主族,且Z的氢化物常温时为液态。W、X的最外层电子数之和与Y的最外层电子数相等,W分别与X、Y、Z形成电子总数相等的分子。
(4)写出XZ2的电子式
(5)X、Z、Q元素的氢化物的沸点最低的是
(6)Y4气态分子结构如图所示,已知断裂1molY-Y吸收167kJ的热量,生成1molY≡Y放出942kJ热量。试写出由Y4气态分子变成Y2态分子的热化学方程式
Ⅲ.下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:

(7)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑
(8)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH:
(9)下列叙述正确的是
A.f与d形成离子化合物为电解质,故该晶体能导电。
B.c、f、g电负性强弱顺序为:g>f>c。
C.第一电离能:f>g>h>d
D.c与h形成化合物的水溶液显中性。
E.硒化氢的稳定性强于f的氢化物的稳定性。
F.h的最高价氧化物对应的水化物是一种强碱。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】X、Y、Z、W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y﹑W均相邻,Y﹑Z和W三种元素的原子最外层电子数之和为17,且Z﹑W最外层电子数相同。
(1)用电子式表示X与Y所组成化合物的形成过程_________________ 。
(2)W在周期表中的位置是____________________ 。
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为__________ 。
(1)用电子式表示X与Y所组成化合物的形成过程
(2)W在周期表中的位置是
(3)已知,在101kPa时,X单质在1.00molO2中完全燃烧生成2.00mol液态H2O,放出571.6kJ的热量,则表示X单质燃烧热的热化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】随原子序数的递增,五种短周期元素原子半径与原子序数的关系如图所示。
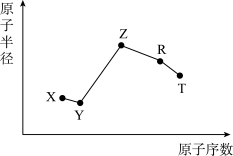
已知:TX2是现代光学及光纤制品的基本原料;ZY 能破坏水的电离平衡;Z3RY6在工业上常用作助熔剂。
(1)R在元素周期表中的位置是___ 。
(2)上述元素中的某两种元素可组成一种五原子共价化合物,该化合物的电子式为___ 。
(3)请用一个化学方程式比较X和Y的非金属性的强弱_____ 。
(4)工业上以Z3RY6作助熔剂的目的是____ 。
(5)已知11.5gZ的单质在X2中完全燃烧,恢复至室温,放出QkJ热量,该反应的热化学方程式为___ 。

已知:TX2是现代光学及光纤制品的基本原料;ZY 能破坏水的电离平衡;Z3RY6在工业上常用作助熔剂。
(1)R在元素周期表中的位置是
(2)上述元素中的某两种元素可组成一种五原子共价化合物,该化合物的电子式为
(3)请用一个化学方程式比较X和Y的非金属性的强弱
(4)工业上以Z3RY6作助熔剂的目的是
(5)已知11.5gZ的单质在X2中完全燃烧,恢复至室温,放出QkJ热量,该反应的热化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液温度。
回答下列问题:
(1)所用NaOH溶液要稍过量,理由是___________ 。
(2)如图装置中碎泡沫塑料及泡沫碎料板的作用是___________ 。
(3)将NaOH溶液倒入小烧杯中的确操作为___________ 。
A.分多次倒入 B.一次倒入
(4)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热|ΔH|=___________ (结果保留一位小数)。
(5)上述实验结果与理论值57.3 kJ/mol存在偏差,其原因可能是以下中的___________ 。
A.量完盐酸后未擦拭干净就量NaOH溶液的温度
B.量取盐酸溶液时仰视读数
C.读取最高温时错过最高值
(6)___________ (填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸。

①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液温度。
回答下列问题:
(1)所用NaOH溶液要稍过量,理由是
(2)如图装置中碎泡沫塑料及泡沫碎料板的作用是
(3)将NaOH溶液倒入小烧杯中的确操作为
A.分多次倒入 B.一次倒入
(4)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生记录数据如下:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
(5)上述实验结果与理论值57.3 kJ/mol存在偏差,其原因可能是以下中的
A.量完盐酸后未擦拭干净就量NaOH溶液的温度
B.量取盐酸溶液时仰视读数
C.读取最高温时错过最高值
(6)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】(1)煤燃烧的烟气(主要污染物SO2、NOx),经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)═NO2(g)+O2(g) △H=-200.9kJ•mol-1
NO(g)+ O2(g)═NO2(g) △H= -58.2kJ•mol-1
O2(g)═NO2(g) △H= -58.2kJ•mol-1
SO2(g)+O3(g)═SO3(g)+O2(g) △H=-241.6kJ•mol-1
(1)反应3NO(g)+O3(g)═3NO2(g)的△H=_______
(2)在标准状况下的11.2L甲烷完全燃烧生成 和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是
和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是____________
(3)中和热的测定是高中重要的定量实验,取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:

①从如图实验装置看,其中尚缺少的一种玻璃用品是______ ,除此之外,装置中的一个明显错误是______
②若0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热△H=______ (取小数点后一位)。
NO(g)+O3(g)═NO2(g)+O2(g) △H=-200.9kJ•mol-1
NO(g)+
 O2(g)═NO2(g) △H= -58.2kJ•mol-1
O2(g)═NO2(g) △H= -58.2kJ•mol-1SO2(g)+O3(g)═SO3(g)+O2(g) △H=-241.6kJ•mol-1
(1)反应3NO(g)+O3(g)═3NO2(g)的△H=
(2)在标准状况下的11.2L甲烷完全燃烧生成
 和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是
和液态水放出444.8 kJ•mol-1热量,能表示其燃烧热的热化学方程式的是(3)中和热的测定是高中重要的定量实验,取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:

①从如图实验装置看,其中尚缺少的一种玻璃用品是
②若0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热△H=
| 项目 | 反应起始温度T1(℃) | 终止温度T2(℃) | T2-T1 | ||
| HCl | NaOH | 平均温度 | |||
| 第1次 | 26.2 | 26.0 | 29.4 | ||
| 第2次 | 27.0 | 27.4 | 32.2 | ||
| 第3次 | 25.9 | 25.9 | 29.1 | ||
| 第4次 | 26.4 | 26.2 | 29.7 | ||
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】用50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)仔细观察实验装置,图中是否缺少一种玻璃仪器,如果缺少,缺少的是______________ (填仪器名称,如果不缺少,此空不填),图中是否有不妥之处,如果有请指出:________________________ (如果没有,此空不填)。

(2)大烧杯上如不盖硬纸板,求得的中和热ΔH将______ (填“偏大”“偏小”或“无影响”)。
(3)如果用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热____________ (填“相等”或“不相等”),简述理由:____________________________ 。
(1)仔细观察实验装置,图中是否缺少一种玻璃仪器,如果缺少,缺少的是

(2)大烧杯上如不盖硬纸板,求得的中和热ΔH将
(3)如果用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某实验小组用 的
的 溶液和
溶液和 的硫酸溶液进行中和反应反应热测定实验。
的硫酸溶液进行中和反应反应热测定实验。
(1)取 溶液和
溶液和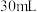 硫酸溶液进行实验,测得的实验数据如表。
硫酸溶液进行实验,测得的实验数据如表。
①请填写下表中的空白:
② 溶液和
溶液和 硫酸溶液的密度均近似为
硫酸溶液的密度均近似为 ,中和后生成的溶液比热容
,中和后生成的溶液比热容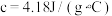 。则测得生成
。则测得生成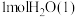 的热量为
的热量为________ kJ(取小数点后一位)。
③上述实验数值结果比正常值偏小,产生偏差的原因可能是________ (填字母)。
A.实验装置保温、隔热效果差
B.量取 溶液的体积时仰视读数
溶液的体积时仰视读数
C.分多次把 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中
D.用温度计测定 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度
(2)现将一定量稀氢氧化钠溶液、稀氢氧化钡溶液、稀氨水分别与 的稀硫酸恰好完全反应,其反应热分别为
的稀硫酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 由大到小关系为
由大到小关系为________ 。
 的
的 溶液和
溶液和 的硫酸溶液进行中和反应反应热测定实验。
的硫酸溶液进行中和反应反应热测定实验。(1)取
 溶液和
溶液和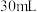 硫酸溶液进行实验,测得的实验数据如表。
硫酸溶液进行实验,测得的实验数据如表。①请填写下表中的空白:
| 温度/实验次数 | 起始温度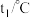 | 终止温度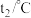 | 温度差平均值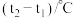 | ||
 |  | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 溶液和
溶液和 硫酸溶液的密度均近似为
硫酸溶液的密度均近似为 ,中和后生成的溶液比热容
,中和后生成的溶液比热容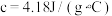 。则测得生成
。则测得生成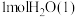 的热量为
的热量为③上述实验数值结果比正常值偏小,产生偏差的原因可能是
A.实验装置保温、隔热效果差
B.量取
 溶液的体积时仰视读数
溶液的体积时仰视读数C.分多次把
 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中D.用温度计测定
 溶液起始温度后直接测定
溶液起始温度后直接测定 溶液的温度
溶液的温度(2)现将一定量稀氢氧化钠溶液、稀氢氧化钡溶液、稀氨水分别与
 的稀硫酸恰好完全反应,其反应热分别为
的稀硫酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 由大到小关系为
由大到小关系为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学兴趣小组要完成中和反应反应热的测定实验。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、玻璃搅拌器、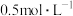 盐酸、
盐酸、 氢氧化钠溶液,实验尚缺少的玻璃仪器是
氢氧化钠溶液,实验尚缺少的玻璃仪器是___________ 、___________ 。
(2)实验中能否用环形铜丝搅拌器代替玻璃搅拌器___________ (填“能”或“否”),其原因是___________ 。
(3)他们记录的实验数据如下:
已知: ,反应后溶液的比热容c为
,反应后溶液的比热容c为 ,各物质的密度均为
,各物质的密度均为 。
。
①通过计算得出生成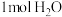 放出的热量为
放出的热量为___________ 。
②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:___________ 。
(4)若用氢氧化钾代替氢氧化钠,对测定结果___________ (填“有”或“无”)影响;若用醋酸代替盐酸做实验,测得中和热的数值___________ (填“大于”“小于”或“等于”)57.3。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、玻璃搅拌器、
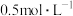 盐酸、
盐酸、 氢氧化钠溶液,实验尚缺少的玻璃仪器是
氢氧化钠溶液,实验尚缺少的玻璃仪器是(2)实验中能否用环形铜丝搅拌器代替玻璃搅拌器
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 生成 放出的热量 放出的热量 | |||
 | · | ||||
| a |  溶液 溶液 |  溶液 溶液 | 20℃ | 23.3℃ | |
| b |  溶液 溶液 |  溶液 溶液 | 20℃ | 23.5℃ | |
 ,反应后溶液的比热容c为
,反应后溶液的比热容c为 ,各物质的密度均为
,各物质的密度均为 。
。①通过计算得出生成
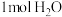 放出的热量为
放出的热量为②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:
(4)若用氢氧化钾代替氢氧化钠,对测定结果
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室利用如图装置进行中和反应的反应热的测定。回答下列问题:

(1)该图中有一种仪器未画出,它是___________________ 。
(2)在操作正确的前提下提高反应热测定的准确性的关键是___________________ 。
(4)如果用 的稀盐酸和氢氧化钠固体进行实验,则根据实验所得数据书写热化学方程式中的
的稀盐酸和氢氧化钠固体进行实验,则根据实验所得数据书写热化学方程式中的 将
将_____________ (填“偏大”“偏小”或“不变”),原因是___________________ 。
(4)利用 的稀盐酸与
的稀盐酸与 的稀氢氧化钠溶液进行实验,设溶液的密度均为
的稀氢氧化钠溶液进行实验,设溶液的密度均为 ,中和后溶液的比热容
,中和后溶液的比热容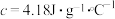 ,请根据下表中实验数据计算中和反应的反应热
,请根据下表中实验数据计算中和反应的反应热
____________ (取小数点后一位)。

(1)该图中有一种仪器未画出,它是
(2)在操作正确的前提下提高反应热测定的准确性的关键是
(4)如果用
 的稀盐酸和氢氧化钠固体进行实验,则根据实验所得数据书写热化学方程式中的
的稀盐酸和氢氧化钠固体进行实验,则根据实验所得数据书写热化学方程式中的 将
将(4)利用
 的稀盐酸与
的稀盐酸与 的稀氢氧化钠溶液进行实验,设溶液的密度均为
的稀氢氧化钠溶液进行实验,设溶液的密度均为 ,中和后溶液的比热容
,中和后溶液的比热容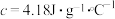 ,请根据下表中实验数据计算中和反应的反应热
,请根据下表中实验数据计算中和反应的反应热
温度 实验次数 | 起始温度 | 终止温度 | ||
 |  | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.4 |
| 2 | 27.0 | 27.4 | 27.2 | 31.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
您最近一年使用:0次



