分类法是常用的科学研究方法,通过对物质进行分类,我们可以更方便的认识物质变化的规律。
I.完成下列问题
(1)某同学在学习了物质分类和转化之后,对该侯氏制碱法反应原理进行了如下解读:CO2属于___________ (填具体物质类型,NH3·H2O属于碱,它们反应可生成了一种酸式盐,其化学式为___________ ,在一定温度下,该体系中各物质的溶解度如表所示,其中溶解度最小的溶质(即___________ 会析出,也即生成了沉淀反应得以发生),侯氏制碱法的反应原理是否属于离子反应,若是,请写出相应的离子方程式___________ 。若否,请在横线上写“否”。
(2)根据各物质的溶解度随温度变化的曲线,欲使 发生,应选择的温度可以是___________(填选项字母)。
发生,应选择的温度可以是___________(填选项字母)。

Ⅱ.完成下列问题
(3)下列物质中:①固体氯化钠;②CO2;③蔗糖晶体;④乙醇;⑤NaHSO4溶液;⑥CuSO4·5H2O;⑦盐酸;⑧Ba(OH)2溶液;⑨熔融氢氧化钠;⑩固体BaSO4。
属于混合物的是___________ (填写相应序号,下同);属于电解质的是___________ 可以导电的是___________ 。
Ⅲ.胶体属于分散系的一种,制备Fe(OH)3胶体的操作方法如下,回答下列问题:
制备Fe(OH)3胶体:向煮沸的蒸馏水中逐滴加入饱和的FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体。
(4)制备Fe(OH)3胶体的离子方程式为___________ 。
(5)如何用实验证明上述所制备的液体是胶体,___________ 。
I.完成下列问题
(1)某同学在学习了物质分类和转化之后,对该侯氏制碱法反应原理进行了如下解读:CO2属于
| 溶解度/g | HCO | Cl- | CO |
| Na+ | 9.6 | 36.0 | 21.8 |
| NH4+ | 21.7 | 372 | 100 |
(2)根据各物质的溶解度随温度变化的曲线,欲使
 发生,应选择的温度可以是___________(填选项字母)。
发生,应选择的温度可以是___________(填选项字母)。
| A.0-10℃ | B.10-20℃ | C.15-45℃ | D.70-80℃ |
Ⅱ.完成下列问题
(3)下列物质中:①固体氯化钠;②CO2;③蔗糖晶体;④乙醇;⑤NaHSO4溶液;⑥CuSO4·5H2O;⑦盐酸;⑧Ba(OH)2溶液;⑨熔融氢氧化钠;⑩固体BaSO4。
属于混合物的是
Ⅲ.胶体属于分散系的一种,制备Fe(OH)3胶体的操作方法如下,回答下列问题:
制备Fe(OH)3胶体:向煮沸的蒸馏水中逐滴加入饱和的FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体。
(4)制备Fe(OH)3胶体的离子方程式为
(5)如何用实验证明上述所制备的液体是胶体,
更新时间:2023-12-20 12:52:03
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】分类法对学习化学具有非常重要的作用。现有物质:①NaHSO4固体 ②CO ③盐酸 ④熔融的NaCl ⑤Ba(OH)2固体 ⑥铜 ⑦CuSO4∙5H2O ⑧氨水 ⑨Fe(OH)3胶体 ⑩SO2。请回答下列问题:
(1)上述物质中属于混合物的有___ (填序号,下同),属于电解质且能导电的有_____ 。
(2)上述物质中属于酸性氧化物的是____ (填序号),原因为____ (请用化学方程式说明)。
(3)①在水中的电离方程式为_______ ;将①与⑤加入水中混合后可得到中性溶液,发生反应的离子方程式为_______ 。
(4)⑨的制备方法为_______ ;⑨与FeCl3溶液的本质区别为_______ 。
(1)上述物质中属于混合物的有
(2)上述物质中属于酸性氧化物的是
(3)①在水中的电离方程式为
(4)⑨的制备方法为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列物质:①Fe ②CO2 ③酒精 ④NaHSO4 ⑤Ba(OH)2 ⑥熔融NaCl ⑦AgCl ⑧NaHCO3 ⑨H2S。(填序号,以下同)
(1)属于盐的是_______ 。
(2)属于电解质的是_______
(3)属于非电解质的是_______ 。
(4)属于强电解质的是_______ 。
(5)属于弱电解质的是_______ 。
(6)⑤在水中电离的方程式为_______ 。
(7)②与⑤反应的离子方程式为_______ 。
(8)区分Fe(OH)3胶体和FeCl3溶液实验方法_______ ;
(9)写出①和HCl反应的离子方程式_______
(1)属于盐的是
(2)属于电解质的是
(3)属于非电解质的是
(4)属于强电解质的是
(5)属于弱电解质的是
(6)⑤在水中电离的方程式为
(7)②与⑤反应的离子方程式为
(8)区分Fe(OH)3胶体和FeCl3溶液实验方法
(9)写出①和HCl反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】通过学习铁和铁的化合物的一些化学性质, 完成下列问题。
(1)高温下,铁粉与水蒸气反应的化学方程式是______________________ ;
其中________ 为氧化剂。
(2)

①往A溶液中分别滴入几滴KSCN溶液,溶液A的颜色变化________ 。将A的饱和溶液滴入沸水中并不断加热,可制得________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为________ 效应。
②写出上述过程中有关反应的离子方程式:
Fe2O3→A______________________ ;A→B______________________ 。
③C在空气中发生变化的现象是_____________________________ 。
(1)高温下,铁粉与水蒸气反应的化学方程式是
其中
(2)

①往A溶液中分别滴入几滴KSCN溶液,溶液A的颜色变化
②写出上述过程中有关反应的离子方程式:
Fe2O3→A
③C在空气中发生变化的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下面短文,并回答问题。
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射。在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应。产生丁达尔效应的实质是光的散射。
表1分散系对可见光的不同作用:
当入射光的波长略大于分散相粒子的直径时就发生光的散射。可见光的波长在400~760nm的范围,略大于一般胶体粒子的直径(1~100nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应。
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象。
(1)产生丁达尔效应的实质是_____ 。
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的_____ 溶液,继续煮沸至液体呈_____ 色即可。
(3)胶体区别于其他分散系的本质特征是_____ (填序号)。
A.胶体有丁达尔效应
B.胶体粒子可以透过滤纸
C.胶体的胶粒带有电荷
D.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是_____ 。
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射。在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应。产生丁达尔效应的实质是光的散射。
表1分散系对可见光的不同作用:
| 溶液 | 胶体 | 浊液 | |
| 光路示意图 | 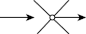 | 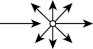 |  |
| 对光的主要作用 | 透射 | 散射 | 反射或折射 |
当入射光的波长略大于分散相粒子的直径时就发生光的散射。可见光的波长在400~760nm的范围,略大于一般胶体粒子的直径(1~100nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应。
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象。
(1)产生丁达尔效应的实质是
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的
(3)胶体区别于其他分散系的本质特征是
A.胶体有丁达尔效应
B.胶体粒子可以透过滤纸
C.胶体的胶粒带有电荷
D.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是_______ ,只有还原性的是_______ ,既有氧化性又有还原性的是_______ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②N2O4+H2O→HNO3+HNO2 ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是_______ (填序号)。
Ⅱ.根据胶体制备和性质完成以下问题
(3)某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加几滴饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl。
(a)判断胶体制备是否成功,可利用胶体的_______ 。
(b)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到_______ ,其原因是_______ 。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会_______ ,原因是_______ 。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会_______ ,原因是_______ 。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②N2O4+H2O→HNO3+HNO2 ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是
Ⅱ.根据胶体制备和性质完成以下问题
(3)某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加几滴饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl。
(a)判断胶体制备是否成功,可利用胶体的
(b)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
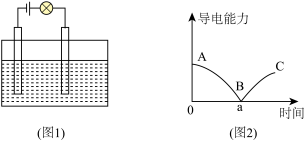
(1)在电解质溶液的导电性实验装置(如图1所示)中,若向某一电解质溶液中逐滴加另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮(如图2)的是___________(填字母)。
(2)在下列物质中,可以导电的是___________ (填序号,下同),是电解质的有___________ ,向盛有⑧的烧杯中逐滴加入⑤,当溶液中的 恰好完全沉淀时,发生反应的离子方程式为
恰好完全沉淀时,发生反应的离子方程式为___________ 。
①熔融的氯化钠 ②干燥的硝酸钾固体 ③蔗糖晶体 ④NH3 ⑤NaHSO4溶液 ⑥金刚石 ⑦Na2O ⑧ 溶液
溶液
(3)某无色透明溶液中可能含有下列离子中的一种或几种: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。现进行如下实验:
。现进行如下实验:
①取少量溶液用红色石蕊试纸检验,试纸变蓝。
②另取少量溶液逐滴滴加盐酸至过量,有气体放出,再加入BaCl2溶液,没有沉淀生成。
③另取少量溶液用足量硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
根据上述实验推断:原溶液中肯定存在的离子有___________ ,肯定不存在的离子有___________ ,实验②中产生气体的离子方程式为___________ 。
(1)在电解质溶液的导电性实验装置(如图1所示)中,若向某一电解质溶液中逐滴加另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮(如图2)的是___________(填字母)。

| A.盐酸中逐滴加入硝酸银溶液 | B.硫酸中逐滴加入氢氧化钠溶液 |
| C.石灰乳中滴加稀盐酸 | D.硫酸中逐滴加入氢氧化钡溶液 |
(2)在下列物质中,可以导电的是
 恰好完全沉淀时,发生反应的离子方程式为
恰好完全沉淀时,发生反应的离子方程式为①熔融的氯化钠 ②干燥的硝酸钾固体 ③蔗糖晶体 ④NH3 ⑤NaHSO4溶液 ⑥金刚石 ⑦Na2O ⑧
 溶液
溶液(3)某无色透明溶液中可能含有下列离子中的一种或几种:
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。现进行如下实验:
。现进行如下实验:①取少量溶液用红色石蕊试纸检验,试纸变蓝。
②另取少量溶液逐滴滴加盐酸至过量,有气体放出,再加入BaCl2溶液,没有沉淀生成。
③另取少量溶液用足量硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
根据上述实验推断:原溶液中肯定存在的离子有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】以下15种物质为中学化学中常见的物质:
①Cu②冰水混合物 ③NaHSO4④SO3 ⑤H2SO4 ⑥KClO3⑦CaCO3 ⑧NO2 ⑨Fe2O3 ⑩Fe(OH)3⑪ 稀盐酸⑫ CaO ⑬ Na2CO3 ⑭ K2SO4⑮ NaHCO3
请按下列要求回答(填写物质的标号):
(1)属于单质的是___________ ;属于混合物的是____________ ;属于氧化物的是__________ 。
(2)其中属于酸性氧化物的是_____________ ;碱性氧化物的是___________________ 。
(3)其中属于钠盐的是______________ ;属于硫酸盐的是_______________ ;属于碳酸盐的是_________ 。
(4)属于电解质的是________ 。
(5)属于酸的是________ 。
(6)属于碱的是________ 。
(7)属于盐的是_________ ;难溶性盐是________ 。
(8)书写电离方程式:KClO3:______________ ;H2SO4:________________________ 。
(9)配平:____ H2S+______ H2SO4=______ S↓+______ SO2↑+_____ H2O
①Cu②冰水混合物 ③NaHSO4④SO3 ⑤H2SO4 ⑥KClO3⑦CaCO3 ⑧NO2 ⑨Fe2O3 ⑩Fe(OH)3⑪ 稀盐酸⑫ CaO ⑬ Na2CO3 ⑭ K2SO4⑮ NaHCO3
请按下列要求回答(填写物质的标号):
(1)属于单质的是
(2)其中属于酸性氧化物的是
(3)其中属于钠盐的是
(4)属于电解质的是
(5)属于酸的是
(6)属于碱的是
(7)属于盐的是
(8)书写电离方程式:KClO3:
(9)配平:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】今有10种物质:① ②稀硝酸③纯醋酸④
②稀硝酸③纯醋酸④ ⑤空气⑥
⑤空气⑥ ⑦Fe(OH)3胶体⑧
⑦Fe(OH)3胶体⑧ 晶体⑨
晶体⑨ ⑩碘酒,(1)至(4)小题按信息用序号填空。
⑩碘酒,(1)至(4)小题按信息用序号填空。
(1)能导电的物质___________ 。
(2)电解质,但熔融状态下并不导电___________ 。
(3)强电解质___________ 。
(4)非电解质___________ 。
(5)区分Fe(OH)3胶体和 溶液实验方法
溶液实验方法___________ 。
(6)实验室中①通常保存在___________ 中。
(7)写出②和⑨反应的离子方程式___________ 。
(8)写出的③的电离方程式___________ 。
 ②稀硝酸③纯醋酸④
②稀硝酸③纯醋酸④ ⑤空气⑥
⑤空气⑥ ⑦Fe(OH)3胶体⑧
⑦Fe(OH)3胶体⑧ 晶体⑨
晶体⑨ ⑩碘酒,(1)至(4)小题按信息用序号填空。
⑩碘酒,(1)至(4)小题按信息用序号填空。(1)能导电的物质
(2)电解质,但熔融状态下并不导电
(3)强电解质
(4)非电解质
(5)区分Fe(OH)3胶体和
 溶液实验方法
溶液实验方法(6)实验室中①通常保存在
(7)写出②和⑨反应的离子方程式
(8)写出的③的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠是非常重要的一种元素,其化合物在生产、生活中有非常重要的用途。
(1)碳酸钠俗称苏打,又名纯碱,是一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。还广泛用于生活洗涤、酸类中和以及食品加工等。纯碱的生产历史悠久,先后经历了:路布兰制碱法、索尔维制碱法、侯德榜制碱法等历程。其中侯德榜制碱法又称联合制碱法,其关键反应步骤是:依次将___________ 和___________ (都填名称)两种气体通入精制饱和食盐水得到中间产物,该步骤涉及的离子方程式为___________
(2)焦亚硫酸钠( )在医药、橡胶、印染、食品等方面应用广泛。
)在医药、橡胶、印染、食品等方面应用广泛。
①生产 ,通常是由
,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
过饱和溶液经结晶脱水制得。写出该过程的化学方程式___________ 。
② 可用作食品的抗氧化剂。在测定某葡萄酒中
可用作食品的抗氧化剂。在测定某葡萄酒中 残留是时,取
残留是时,取 葡萄酒样品,用
葡萄酒样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 、滴定反应的离子方程式为
、滴定反应的离子方程式为___________ ,该样品中 的残留量为
的残留量为___________  (以
(以 计)
计)
(3)氢化钠是厨房最常见的调味品之一,而亚硝酸钠是一种重要的化工原料,有毒。由于亚硝酸钠外观与氯化钠类似且具有成味,因此偶有发生误食而中毒的事件。业上可以通过用 溶液吸收NO和
溶液吸收NO和 的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成
的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成 亚硝酸钠时理论上转移电子的数目为
亚硝酸钠时理论上转移电子的数目为___________  。
。
(1)碳酸钠俗称苏打,又名纯碱,是一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。还广泛用于生活洗涤、酸类中和以及食品加工等。纯碱的生产历史悠久,先后经历了:路布兰制碱法、索尔维制碱法、侯德榜制碱法等历程。其中侯德榜制碱法又称联合制碱法,其关键反应步骤是:依次将
(2)焦亚硫酸钠(
 )在医药、橡胶、印染、食品等方面应用广泛。
)在医药、橡胶、印染、食品等方面应用广泛。①生产
 ,通常是由
,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
过饱和溶液经结晶脱水制得。写出该过程的化学方程式②
 可用作食品的抗氧化剂。在测定某葡萄酒中
可用作食品的抗氧化剂。在测定某葡萄酒中 残留是时,取
残留是时,取 葡萄酒样品,用
葡萄酒样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 、滴定反应的离子方程式为
、滴定反应的离子方程式为 的残留量为
的残留量为 (以
(以 计)
计)(3)氢化钠是厨房最常见的调味品之一,而亚硝酸钠是一种重要的化工原料,有毒。由于亚硝酸钠外观与氯化钠类似且具有成味,因此偶有发生误食而中毒的事件。业上可以通过用
 溶液吸收NO和
溶液吸收NO和 的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成
的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成 亚硝酸钠时理论上转移电子的数目为
亚硝酸钠时理论上转移电子的数目为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。联合制碱法的工艺流程简化如下:

I.资料1:反应I中的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓
资料2:20℃时,溶解度小于0.0lg的物质属于难溶物;20℃时BaSO4溶解度为 g。
g。
资料3:表1有关物质的溶解度(20℃)
(1)操作I的名称为_______ ,反应II的化学方程式为_______ 。
(2)相同温度下,用pH试纸测量同等浓度的Na2CO3与NaHCO3溶液pH,_______ 溶液碱性强。
(3)离子反应: ,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是
,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是_______ 。
II.泡腾片是一种医药片剂,适用于儿童、老年人以及吞服药丸困难的患者。泡腾片放入水中,在崩解剂的作用下,即刻产生大量气泡(二氧化碳),使片剂迅速崩解形成水溶液,崩解剂主要由NaHCO3固体与柠檬酸固体组成。
(4)下列说法正确的是_______ (填字母)。
A.NaHCO3固体与柠檬酸固体不反应
B.柠檬酸在水中电离产生H+与NaHCO3反应
C.Na2CO3比NaHCO3稳定,受热不易分解
(5)某NaHCO3样品中含NaCl杂质,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中NaHCO3的质量分数是_______ 。

I.资料1:反应I中的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓
资料2:20℃时,溶解度小于0.0lg的物质属于难溶物;20℃时BaSO4溶解度为
 g。
g。资料3:表1有关物质的溶解度(20℃)
| 物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(1)操作I的名称为
(2)相同温度下,用pH试纸测量同等浓度的Na2CO3与NaHCO3溶液pH,
(3)离子反应:
 ,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是
,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是II.泡腾片是一种医药片剂,适用于儿童、老年人以及吞服药丸困难的患者。泡腾片放入水中,在崩解剂的作用下,即刻产生大量气泡(二氧化碳),使片剂迅速崩解形成水溶液,崩解剂主要由NaHCO3固体与柠檬酸固体组成。
(4)下列说法正确的是
A.NaHCO3固体与柠檬酸固体不反应
B.柠檬酸在水中电离产生H+与NaHCO3反应
C.Na2CO3比NaHCO3稳定,受热不易分解
(5)某NaHCO3样品中含NaCl杂质,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中NaHCO3的质量分数是
您最近一年使用:0次



