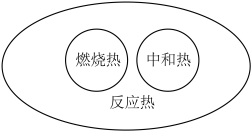
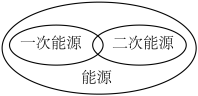
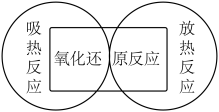
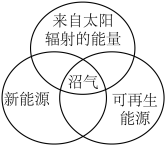
下列说法中,正确的是
A. 表示放热反应, 表示放热反应, 表示吸热反应 表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,可以是分数 |
C.含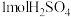 的溶液与含 的溶液与含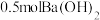 的溶液混合反应,放出的热量即为中和热 的溶液混合反应,放出的热量即为中和热 |
D. 与 与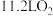 反应生成液态水放出的热量就是 反应生成液态水放出的热量就是 的燃烧热 的燃烧热 |
更新时间:2023-12-21 12:02:16
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是( )
| A.由H形成1 molH-H 键要吸收热量 |
| B.所有燃烧反应都是放热反应 |
| C.16g O3 单质中含有的分子个数为NA |
| D.凡经加热而发生的化学反应都是吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列过程放出热量的是
| A.水气化 | B.生石灰溶于水 | C.碳酸钙分解 | D.断开Cl—Cl键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关反应热的说法正确的是
| A.对于任何一个吸热反应,使用催化剂后,△H将降低 |
| B.反应热的大小与反应物所具有的总能量和生成物所具有的总能量相关 |
| C.甲烷的燃烧热△H=-890kJ/mol,则:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890kJ/mol |
| D.已知常温常压下HCl(aq)+NaOH(aq)=NaCl(aq)+H2O (1) △H=-57.3kJ/mol,则有H2SO4+Ba(OH)2=BaSO4+2H2O △H=-114.6kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=+57.3kJ/mol (中和热) |
| B.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H= -1367.0kJ/mol(燃烧热) |
| C.S(s)+O2(g)=SO2(g) △H= -296.8kJ/mol (反应热) |
| D.2NO2=O2+2NO △H=+116.2kJ/mol (反应热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列说法正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l) ΔH=−57.3kJ∙mol−1,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的ΔH |
| B.1mol H2与0.5mol O2反应放出的热量就是H2的燃烧热 |
| C.加入催化剂可以改变反应的活化能,不能改变焓变 |
D.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ∆H=−38.6kJ∙mol−1 2NH3(g) ∆H=−38.6kJ∙mol−1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】运用有关概念判断下列叙述正确的是( )
| A.1molH2燃烧放出的热量为H2的燃烧热 |
| B.Na2SO3和H2O2的反应为氧化还原反应 |
C.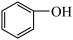 和 和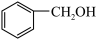 互为同系物 互为同系物 |
| D.Fe(OH)3胶体和FeSO4溶液均能产生丁达尔效应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在25 oC,101 kPa下,0.2 mol C2H2完全燃烧生成CO2和H2O(l)时放出259.92 kJ热量。表示上述反应的热化学方程式正确的是
| A.2C2H2(g)+5O2(g) = 4CO2(g)+2H2O(g) ∆H=+259.92 kJ/mol |
| B.2C2H2(g)+5O2(g) = 4CO2(g)+2H2O(l) ∆H=-259.92 kJ/mol |
| C.2C2H2(g)+5O2(g) = 4CO2(g)+2H2O(l) ∆H=+2599.2 kJ/mol |
| D.2C2H2(g)+5O2(g) = 4CO2(g)+2H2O(l) ∆H=-2599.2 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列有关反应热的说法正确的是
| A.在化学反应过程中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量 |
| B.甲烷标准燃烧热△H=-890kJ/mol,则:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890kJ/mol |
| C.已知常温常压下HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol,则有H2SO4+Ba(OH)2=BaSO4+2H2O △H=-114.6kJ/mol |
| D.已知S(s)+O2(g) =SO2(g) △H=-Q1kJ/mol,S(g)+O2(g) =SO2(g) △H=-Q2kJ/mol,则Q1<Q2 |
您最近一年使用:0次