碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
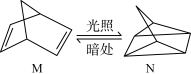
(1)有机物M经过太阳光照可转化成N,转化过程如下,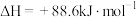 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是_______ 。
(2)已知 的燃烧热为
的燃烧热为 ,
,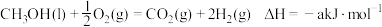 ,则a
,则a_______ 238.6(填“>”“<”或“=”)。
(3)使 和
和 通过灼热的炭层,生成
通过灼热的炭层,生成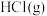 和
和 ,当有
,当有 参与反应时释放出
参与反应时释放出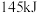 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式_______ 。
(4)常温常压下,断裂 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些化学键的键能(单位为
(理想)气体分子化学键所放出的能量称为键能,下表是一些化学键的键能(单位为 );
);
反应 的
的
_______ 。
(5)已知: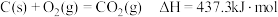
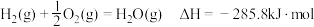
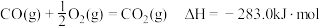
①写出煤气化(碳和水蒸气反应生成一氧化碳和氨气)的热化学方程式_______ 。
②计算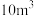 (标准状况下)水煤气完全燃烧放出的热量为
(标准状况下)水煤气完全燃烧放出的热量为_______  (结果保留小数点后一位)。
(结果保留小数点后一位)。
(1)有机物M经过太阳光照可转化成N,转化过程如下,
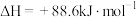 。则M、N相比,较稳定的是
。则M、N相比,较稳定的是
(2)已知
 的燃烧热为
的燃烧热为 ,
,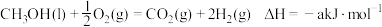 ,则a
,则a(3)使
 和
和 通过灼热的炭层,生成
通过灼热的炭层,生成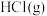 和
和 ,当有
,当有 参与反应时释放出
参与反应时释放出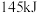 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式(4)常温常压下,断裂
 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些化学键的键能(单位为
(理想)气体分子化学键所放出的能量称为键能,下表是一些化学键的键能(单位为 );
);| 化学键 |  |  |  |  |
 | 414 | 489 | 158 | 565 |
 的
的
(5)已知:
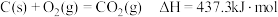
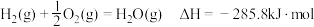
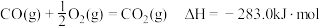
①写出煤气化(碳和水蒸气反应生成一氧化碳和氨气)的热化学方程式
②计算
 (标准状况下)水煤气完全燃烧放出的热量为
(标准状况下)水煤气完全燃烧放出的热量为 (结果保留小数点后一位)。
(结果保留小数点后一位)。
更新时间:2023-12-23 00:04:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。
SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。
(2)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=___________ 。
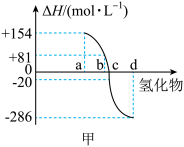
(3)热力学标准态(298.15K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫作该化合物的生成热(ΔH)。图甲为氧族元素中的氧、硫、硒(Se)、碲在生成1mol气态氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表那种元素,试写出硒化氢在上述条件下发生分解反应的热化学方程式为___________ 。
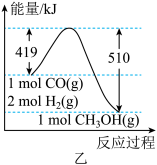
(4)图乙表示CO和H2反应生成CH3OH过程中能量变化示意图,请写出CO和H2反应的热化学方程式:___________ 。
(5)采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。
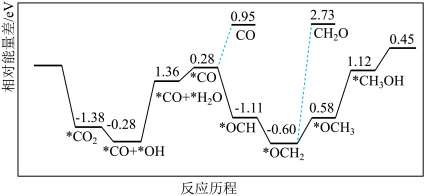
容易得到的副产物有CO和CH2O,其中相对较多的副产物为___________ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中___________ (填字母)的能量变化。
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(1)已知热化学方程式:SO2(g)+
 O2(g)
O2(g) SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。
SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。| A.等于196.64kJ | B.小于98.32kJ | C.小于196.64kJ | D.大于196.64kJ |
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | a |
(3)热力学标准态(298.15K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫作该化合物的生成热(ΔH)。图甲为氧族元素中的氧、硫、硒(Se)、碲在生成1mol气态氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表那种元素,试写出硒化氢在上述条件下发生分解反应的热化学方程式为

(4)图乙表示CO和H2反应生成CH3OH过程中能量变化示意图,请写出CO和H2反应的热化学方程式:

(5)采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。

容易得到的副产物有CO和CH2O,其中相对较多的副产物为
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学反应同时伴随着能量变化.是人类获取能量的重要途径。以下是常见的化学反应。
a.镁与盐酸反应 b.氢氧化钠与盐酸反应 c.盐酸与碳酸氢钠反应
d.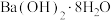 晶体与
晶体与 晶体反应
晶体反应
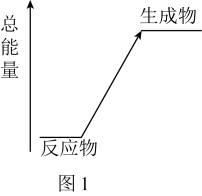
(1)以上化学反应中能用如图表示其能量变化的是________ (填字母),此类反应中有能量变化的原因是:断开反应物的化学键吸收的总能量________ (填“>”或“<”)形成生成物的化学键释放的总能量。___________ 。
②证实化学能转化为电能的实验现象是___________ 。
③正极的电极反应式是___________ 。
④烧杯中溶液的作用是___________ 。
a.电极材料 b.电极反应物 c.电子导体 d.离子导体
⑤从化学的角度分析,原电池产生电流的原因是___________ 。
a.镁与盐酸反应 b.氢氧化钠与盐酸反应 c.盐酸与碳酸氢钠反应
d.
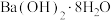 晶体与
晶体与 晶体反应
晶体反应(1)以上化学反应中能用如图表示其能量变化的是
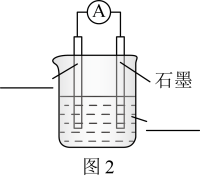
②证实化学能转化为电能的实验现象是
③正极的电极反应式是
④烧杯中溶液的作用是
a.电极材料 b.电极反应物 c.电子导体 d.离子导体
⑤从化学的角度分析,原电池产生电流的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】当溴与1,3-丁二烯在环己烷溶液中发生加成反应时,会得到两个产物A和B(不考虑立体化学)。在-15℃时A和B的比例为62:38;而在25℃时A和B的比例为12:88。
(1)画出化合物A和B的结构简式_____ ;并确定哪个为热力学稳定产物,哪个为动力学产物______ 。
(2)在室温下,A可以缓慢地转化为B.画出此转换过程的反应势能示意图和中间体的结构简式_____ 。
(3)根据以上的研究结果,确定以下反应的产物:
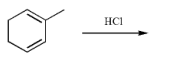
______
(1)画出化合物A和B的结构简式
(2)在室温下,A可以缓慢地转化为B.画出此转换过程的反应势能示意图和中间体的结构简式
(3)根据以上的研究结果,确定以下反应的产物:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)已知键能如下:H-H为akJ/mol N≡N为bkJ/mol N-H为ckJ/mol,则N2(g)+3H2(g) 2NH3(g) △H=
2NH3(g) △H=__________ ;
(2)石墨吸热生成金刚石,则二者中相对稳定的物质为_________________ ;
(3)明矾净水的离子方程式为:__________________________ ;
(4)催化剂可以加快化学反应速率的原因___________________ ,此外催化剂和升温都能提高活化分子的百分数,催化剂不能影响平衡的移动。
(5)常温时,pH=9的氨水溶液中,由水电离出的c(OH-)为_______________________ 。
 2NH3(g) △H=
2NH3(g) △H=(2)石墨吸热生成金刚石,则二者中相对稳定的物质为
(3)明矾净水的离子方程式为:
(4)催化剂可以加快化学反应速率的原因
(5)常温时,pH=9的氨水溶液中,由水电离出的c(OH-)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)下列变化:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。(填序号 )
化学键没有被破坏的是________ ;仅发生离子键破坏的是_______ ; 仅发生共价键破坏的是________ ;既发生离子键又发生共价键破坏的是_______ 。
(2)已知1mol Si中含1mol Si—Si键。
请回答下列问题:
①已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列物质的熔点高低(填“>”或“<”):SiC________ Si。
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)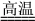 Si(s)+4HCl(g),则2 mol H2生成高纯硅需
Si(s)+4HCl(g),则2 mol H2生成高纯硅需________ (填“吸收”或“放出”)能量________ kJ。
化学键没有被破坏的是
(2)已知1mol Si中含1mol Si—Si键。
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列物质的熔点高低(填“>”或“<”):SiC
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
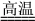 Si(s)+4HCl(g),则2 mol H2生成高纯硅需
Si(s)+4HCl(g),则2 mol H2生成高纯硅需
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢可构成火箭推进剂.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知:0.4mol液态肼与足量的液态过氧化氢反应生成N2和水蒸气时放出256.0kJ的热量。
(1)该反应的热化学方程式为________________ ;
(2)则16g液态肼与液态过氧化氢反应生成气态水时放出的热量是________________ kJ;
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是________________ 。
(1)该反应的热化学方程式为
(2)则16g液态肼与液态过氧化氢反应生成气态水时放出的热量是
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知下列热化学方程式:
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ / mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是__________ (填序号,下同),属于吸热反应的是__________ 。
(2)2g H2完全燃烧生成液态水,放出的热量为_____________ 。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为_________________________________ 。
②已知HCN稀溶液与NaOH稀溶液反应生成1mol H2O时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为_______________________________________________ 。
③在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________________________________________ 。
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ / mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2g H2完全燃烧生成液态水,放出的热量为
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为
②已知HCN稀溶液与NaOH稀溶液反应生成1mol H2O时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为
③在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂H2O2。当它们混合发生反应时,立即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol肼与足量H2O2反应,生成水蒸气和氮气,放出256.625 kJ的热量。
(1)该反应的热化学方程式为:_________________ 。
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ/mo则16 g肼与足量液态H2O2反应生成液态水时放出的热量是_________________ 。
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体之外,还有一个很大的优点是:_________________ 。
(4)发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) ΔH=+66.4 kJ·mol-1;N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
肼和二氧化氮反应的热化学方程式为:_________________ 。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=_________ 。
(6)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1______ ΔH2。(填“>”“<”或“=”)
(1)该反应的热化学方程式为:
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ/mo则16 g肼与足量液态H2O2反应生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体之外,还有一个很大的优点是:
(4)发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) ΔH=+66.4 kJ·mol-1;N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
肼和二氧化氮反应的热化学方程式为:
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+
 O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1C(石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=
(6)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在25℃、101KPa时,____________________________ 时所放出的热量,叫做该反应的燃烧热。在25℃、101KPa时,1g乙醇完全燃烧生成CO2和液态水时放热29.713kJ,则能表示乙醇燃烧热的热化学方程式为_________________________________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空
(1)在25℃、101kPa下,1mol气态H2与0.5mol气态O2反应生成1mol气态H2O,放出241.8kJ的热量:_____________
(2)在25℃、101kPa下,1mol气态H2与足量气态O2反应生成1mol液态H2O,放出285.8kJ的热量:____________________
(1)在25℃、101kPa下,1mol气态H2与0.5mol气态O2反应生成1mol气态H2O,放出241.8kJ的热量:
(2)在25℃、101kPa下,1mol气态H2与足量气态O2反应生成1mol液态H2O,放出285.8kJ的热量:
您最近一年使用:0次











 。则
。则 的燃烧热为
的燃烧热为

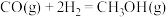
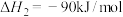
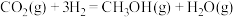 的
的





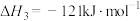
 的
的 。
。


