完成下列问题。
(1)
 。则
。则 的燃烧热为
的燃烧热为___________ 。
(2)二氧化碳加氢制甲醇一般认为通过如下步骤来实现:
①

②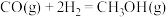
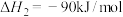
则反应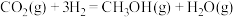 的
的
___________ kJ/mol。
(3)Deacon直接氧化法可按下列催化过程进行:





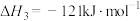
则 的
的
___________  。
。
(1)

 。则
。则 的燃烧热为
的燃烧热为(2)二氧化碳加氢制甲醇一般认为通过如下步骤来实现:
①


②
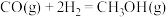
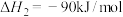
则反应
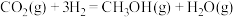 的
的
(3)Deacon直接氧化法可按下列催化过程进行:





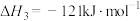
则
 的
的
 。
。
更新时间:2024-01-12 20:46:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】NF3是一种有毒、无味、无色的气体,NF3气体作为刻蚀剂和清洗剂在电子工业中有广泛的应用,回答下列问题:
(1)F2和液氨直接反应可制备NF3,反应的化学方程式为_____________________ 。反应过程中会涉及副反应:4F2+2NH3=N2F2+6HF,其中N2F2的结构式可表示为_______________ 。
(2)F2和固态(NH4)3AlF6反应可制备NF3,反应的化学方程式为:(NH4)3AlF6+6F2=2NF3+8HF+NH4AlF4,NH4AlF4+3F2=NF3+4HF+AlF3。若1 mol F2参加反应,最多可制得NF3______ mol,此时反应中转移电子______ mol。
(3)工业上用惰性电极电解含HF、NH4F等无水熔融物的方法生产NF3。电解过程中阳极的电极反应式为_______________________ ,阴极的电极反应式为______________________ 。
(4)一定条件下,向一带活塞的密闭容器中充入1 mol NF3气体,此时容器的体积为V L,在该条件下发生反应2NF3 N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为
N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为_________ mol·L−1。
(1)F2和液氨直接反应可制备NF3,反应的化学方程式为
(2)F2和固态(NH4)3AlF6反应可制备NF3,反应的化学方程式为:(NH4)3AlF6+6F2=2NF3+8HF+NH4AlF4,NH4AlF4+3F2=NF3+4HF+AlF3。若1 mol F2参加反应,最多可制得NF3
(3)工业上用惰性电极电解含HF、NH4F等无水熔融物的方法生产NF3。电解过程中阳极的电极反应式为
(4)一定条件下,向一带活塞的密闭容器中充入1 mol NF3气体,此时容器的体积为V L,在该条件下发生反应2NF3
 N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为
N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)依据事实,写出下列反应的热化学方程式。
①在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:___________________________________________ 。
②若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量__________________ 。
③已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为:________________________________ 。
(2)氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示:
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是____________ 。
②第II步为可逆反应。在800℃时,若CO的起始浓度为2.0 mol/L,水蒸气的起始浓度为3.0 mol/L,达到化学平衡状态后,测得CO2的浓度为1.2 mol/L,则此反应的平衡常数为____ ,CO的平衡转化率为_____ 。
①在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:
②若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量
③已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为:
(2)氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示:

①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是
②第II步为可逆反应。在800℃时,若CO的起始浓度为2.0 mol/L,水蒸气的起始浓度为3.0 mol/L,达到化学平衡状态后,测得CO2的浓度为1.2 mol/L,则此反应的平衡常数为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业常用铁钼氧化物作催化剂,用甲醇空气氧化法制甲醛,反应过程涉及如下反应:
(有关数据均在298K时测定)
反应Ⅰ: ,
,
反应Ⅱ: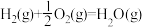
反应Ⅲ: ,
,
反应温度对甲醇氧化反应的影响如图所示。

(1)用反应Ⅲ制甲醛要比直接用反应Ⅰ制甲醛优越,原因是___________________________________________ 。
(2)生产时,要控制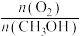 为0.4左右,目的是
为0.4左右,目的是__________________________ (试从反应热和反应适宜的温度思考)。
(3)下列说法不正确的是__________________________ 。
A.甲醇的转化率接近100%的原因是反应Ⅲ属于完全反应
B.氢气的摩尔燃烧热为‒241.8kJ•mol‒1
C.600K以后甲醛产率下降的原因可能是温度升高导致甲醛发生热分解反应
(有关数据均在298K时测定)
反应Ⅰ:
 ,
,
反应Ⅱ:
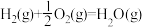
反应Ⅲ:
 ,
,
反应温度对甲醇氧化反应的影响如图所示。

(1)用反应Ⅲ制甲醛要比直接用反应Ⅰ制甲醛优越,原因是
(2)生产时,要控制
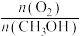 为0.4左右,目的是
为0.4左右,目的是(3)下列说法不正确的是
A.甲醇的转化率接近100%的原因是反应Ⅲ属于完全反应
B.氢气的摩尔燃烧热为‒241.8kJ•mol‒1
C.600K以后甲醛产率下降的原因可能是温度升高导致甲醛发生热分解反应
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为_______ 。(选序号)写出4g H2燃烧的热化学方程式_______ ;
(2)24g C完全燃烧,放出的热量为_______ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。
(1)C燃烧热的热化学方程式为
(2)24g C完全燃烧,放出的热量为
(3)液态水的稳定性
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】在25℃、101KPa时,____________________________ 时所放出的热量,叫做该反应的燃烧热。在25℃、101KPa时,1g乙醇完全燃烧生成CO2和液态水时放热29.713kJ,则能表示乙醇燃烧热的热化学方程式为_________________________________________ 。
您最近半年使用:0次
【推荐3】2SO2(g)+O2(g)=2SO3(g)反应过程中的能量变化如图所示。已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH1=-99 kJ/mol。请回答下列问题:

(1) 图中A、C分别表示________ 、________ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ;
(2) 图中ΔH=__________ kJ/mol;
(3) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______ 。

(1) 图中A、C分别表示
(2) 图中ΔH=
(3) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH
您最近半年使用:0次



