工业常用铁钼氧化物作催化剂,用甲醇空气氧化法制甲醛,反应过程涉及如下反应:
(有关数据均在298K时测定)
反应Ⅰ: ,
,
反应Ⅱ: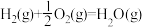
反应Ⅲ: ,
,
反应温度对甲醇氧化反应的影响如图所示。

(1)用反应Ⅲ制甲醛要比直接用反应Ⅰ制甲醛优越,原因是___________________________________________ 。
(2)生产时,要控制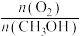 为0.4左右,目的是
为0.4左右,目的是__________________________ (试从反应热和反应适宜的温度思考)。
(3)下列说法不正确的是__________________________ 。
A.甲醇的转化率接近100%的原因是反应Ⅲ属于完全反应
B.氢气的摩尔燃烧热为‒241.8kJ•mol‒1
C.600K以后甲醛产率下降的原因可能是温度升高导致甲醛发生热分解反应
(有关数据均在298K时测定)
反应Ⅰ:
 ,
,
反应Ⅱ:
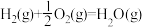
反应Ⅲ:
 ,
,
反应温度对甲醇氧化反应的影响如图所示。

(1)用反应Ⅲ制甲醛要比直接用反应Ⅰ制甲醛优越,原因是
(2)生产时,要控制
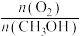 为0.4左右,目的是
为0.4左右,目的是(3)下列说法不正确的是
A.甲醇的转化率接近100%的原因是反应Ⅲ属于完全反应
B.氢气的摩尔燃烧热为‒241.8kJ•mol‒1
C.600K以后甲醛产率下降的原因可能是温度升高导致甲醛发生热分解反应
更新时间:2020-10-11 12:39:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气,已知:
N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;
试写出N2H4与 NO2反应的热化学方程式___________ 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3(g)的热化学方程式为___________ 。
(1)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气,已知:
N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;
试写出N2H4与 NO2反应的热化学方程式
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3(g)的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应Ⅰ:CH3OH(g) HCHO(g)+H2(g)△H1=+85.2kJ/mol
HCHO(g)+H2(g)△H1=+85.2kJ/mol
反应Ⅱ:CH3OH(g)+ O2(g)
O2(g) HCHO(g)+H2O(g)△H2
HCHO(g)+H2O(g)△H2
反应Ⅲ:2H2(g)+O2(g) 2H2O(g)△H3=-483.6kJ/mol
2H2O(g)△H3=-483.6kJ/mol
计算反应Ⅱ的反应热△H2=__ 。
反应Ⅰ:CH3OH(g)
 HCHO(g)+H2(g)△H1=+85.2kJ/mol
HCHO(g)+H2(g)△H1=+85.2kJ/mol反应Ⅱ:CH3OH(g)+
 O2(g)
O2(g) HCHO(g)+H2O(g)△H2
HCHO(g)+H2O(g)△H2反应Ⅲ:2H2(g)+O2(g)
 2H2O(g)△H3=-483.6kJ/mol
2H2O(g)△H3=-483.6kJ/mol计算反应Ⅱ的反应热△H2=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】一定温度下,向1.0 L密闭容器中加入0.60 mol X(g),发生反应X(g) Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
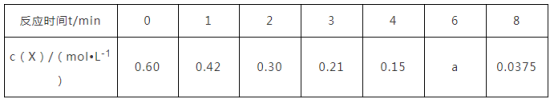
(1)0~3 min用Z表示的平均反应速率v(Z)=____ 。
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是_____________ 。由此规律推出反应在6 min时反应物的浓度a为____ mol·L-1。
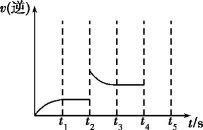
(3)反应的逆反应速率随时间变化的关系如图所示,t2时改变的条件可是______ 、_____ 。
 Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X的浓度与反应时间的数据如下表:
(1)0~3 min用Z表示的平均反应速率v(Z)=
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是
(3)反应的逆反应速率随时间变化的关系如图所示,t2时改变的条件可是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7% O2:11% N2:82%)。
(1)SO2的氧化反应是___ 反应(填“吸热”或“放热”)。
(2)根据图中所给信息,你认为工业上将SO2转化为SO3的适宜条件是___ 。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?___ (填“是”或“否”)。
(4)若保持温度和容积不变,平衡后通入氧气,再达平衡时则SO2浓度___ 。(填“增大”或“减小”)
(5)若保持温度和压强不变,平衡后通入He气,SO3的含量___ 。(填“增大”或“减小”)
 | 0.1个大气压 | 0.5个大气压 | 1个大气压 | 10个大气压 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(2)根据图中所给信息,你认为工业上将SO2转化为SO3的适宜条件是
(3)选择适宜的催化剂,是否可以提高SO2的转化率?
(4)若保持温度和容积不变,平衡后通入氧气,再达平衡时则SO2浓度
(5)若保持温度和压强不变,平衡后通入He气,SO3的含量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:
①4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为___________ ;NH3分解为N2和H2的热化学方程式______________________ 。
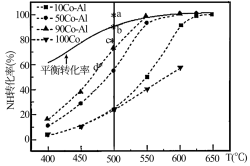
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为___________ 。同一催化剂下,温度高时NH3的转化率接近平衡转化率的原因___________ 。如果增大氨气浓度(其它条件不变),则b点对应的点可能为___________ 。(填“a”、“c”或“d”)
(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,30min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=___________ ,NH3转化率为___________ ;达到平衡后再加入1.0molNH3和0.2molH2,此时体系中v正___________ v逆(填“>“<”或“=”)。
(1)已知:
①4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为

(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,30min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=
您最近一年使用:0次

 催化还原
催化还原 、
、 的反应如下:
的反应如下: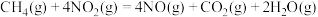
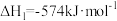
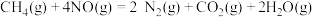

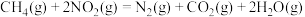

 。
。 还原
还原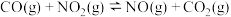
 ,其反应过程中的能量变化如图所示。
,其反应过程中的能量变化如图所示。
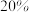 ,则
,则

