NF3是一种有毒、无味、无色的气体,NF3气体作为刻蚀剂和清洗剂在电子工业中有广泛的应用,回答下列问题:
(1)F2和液氨直接反应可制备NF3,反应的化学方程式为_____________________ 。反应过程中会涉及副反应:4F2+2NH3=N2F2+6HF,其中N2F2的结构式可表示为_______________ 。
(2)F2和固态(NH4)3AlF6反应可制备NF3,反应的化学方程式为:(NH4)3AlF6+6F2=2NF3+8HF+NH4AlF4,NH4AlF4+3F2=NF3+4HF+AlF3。若1 mol F2参加反应,最多可制得NF3______ mol,此时反应中转移电子______ mol。
(3)工业上用惰性电极电解含HF、NH4F等无水熔融物的方法生产NF3。电解过程中阳极的电极反应式为_______________________ ,阴极的电极反应式为______________________ 。
(4)一定条件下,向一带活塞的密闭容器中充入1 mol NF3气体,此时容器的体积为V L,在该条件下发生反应2NF3 N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为
N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为_________ mol·L−1。
(1)F2和液氨直接反应可制备NF3,反应的化学方程式为
(2)F2和固态(NH4)3AlF6反应可制备NF3,反应的化学方程式为:(NH4)3AlF6+6F2=2NF3+8HF+NH4AlF4,NH4AlF4+3F2=NF3+4HF+AlF3。若1 mol F2参加反应,最多可制得NF3
(3)工业上用惰性电极电解含HF、NH4F等无水熔融物的方法生产NF3。电解过程中阳极的电极反应式为
(4)一定条件下,向一带活塞的密闭容器中充入1 mol NF3气体,此时容器的体积为V L,在该条件下发生反应2NF3
 N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为
N2+3F2,达到平衡时测得容器中N2的浓度为0.1 mol·L−1,则平衡时NF3的浓度为
2019高三下·全国·专题练习 查看更多[1]
(已下线)2019年4月21日 《每日一题》 三轮复习-每周一测
更新时间:2019-04-18 16:16:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】硫、氮元素是高中化学学习的两种重要非金属元素,其价-类二维图分别如图。
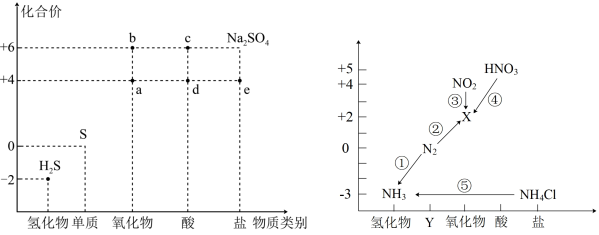
(1)图中物质“d”的化学式是___________ ;若不加任何其它试剂完成转化过程⑤,则⑤的反应为___________ 反应(填“吸热”或“放热”)。
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
(3)写出反应③的离子方程式___________ 。
(4)a的水溶液与H2S发生反应可观察到的实验现象是___________ 。
(5)若e为钾元素的正盐,能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O 被还原为Cr3+,请配平化学方程式:
被还原为Cr3+,请配平化学方程式:_________
___________K2SO3+___________K2Cr2O7+___________H2SO4=___________Cr2(SO4)3+___________K2SO4+___________H2O
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:
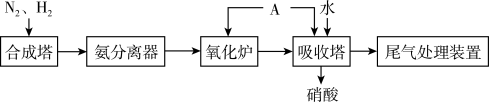
已知:用NaOH溶液进行尾气处理时的化学反应为: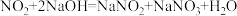 ,
,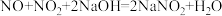 。
。
为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积必须满足的条件是:
___________ 。

(1)图中物质“d”的化学式是
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
| A.Ba(NO3)2溶液 | B.CaCl2溶液 | C.H2O2溶液 | D.Na2CO3溶液 |
(4)a的水溶液与H2S发生反应可观察到的实验现象是
(5)若e为钾元素的正盐,能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O
 被还原为Cr3+,请配平化学方程式:
被还原为Cr3+,请配平化学方程式:___________K2SO3+___________K2Cr2O7+___________H2SO4=___________Cr2(SO4)3+___________K2SO4+___________H2O
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:

已知:用NaOH溶液进行尾气处理时的化学反应为:
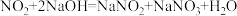 ,
,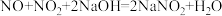 。
。为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积必须满足的条件是:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.海带中含有丰富的碘,某学习小组设计并进行以下实验:
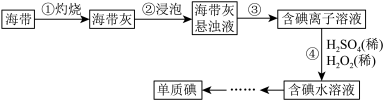
(1)步骤③的实验操作所用。用到的玻璃仪器有___________ 。步骤④的离子反应方程式为: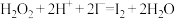 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是___________ ,还原剂是___________ 。步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现蓝色,说明有碘单质产生。
II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失, 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。
(2)写出潮湿环境下KI与氧气反应的化学方程式:___________ 。
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:
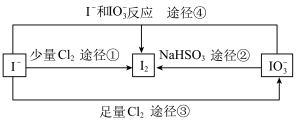
(3)四个途径中属于氧化还原反应的是___________ (填序号)。
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为: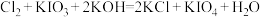 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(5)比较I2、 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:___________ 。

(1)步骤③的实验操作所用。用到的玻璃仪器有
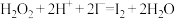 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,
 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。(2)写出潮湿环境下KI与氧气反应的化学方程式:
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:

(3)四个途径中属于氧化还原反应的是
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为:
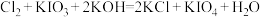 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)比较I2、
 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知在恒压下,密闭容器中发生反应CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),在不同温度、不同投料比时,NO2的平衡转化率见下表:
(1)该反应的ΔH____ 0(填“>”、“<”或“=”)。
(2)若400K时,将投料比为1:1的NO2和CH4的混合气体共0.04mol,充入一装有催化剂的容器中,充分反应后,平衡时NO2的体积百分数是____ (结果保留到小数点后一位)。
(3)在容积相同的两个密闭容器内(装有等量的某种催化剂)先各通入等物质的量的CH4,然后再分别充入等物质的量的NO和NO2,分别进行CH4(g)+4NO(g)⇌2N2(g)+CO2(g)+2H2O(g)和CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)。下图表示选取不同温度,并都在t秒时测定其中NOx转化率,绘得图象如下:

由图可知:①相同温度下,NO转化效率比NO2的低;②250~450℃时NOx转化率随温度升高而增大,450~600℃时NOx转化率随温度升高而减小。解释②的原因是____ 。
| n(NO2)/n(CH4) | 400K | 500K | 600K |
| 1:1 | 60% | 43% | 28% |
| 2:1 | 45% | 33% | 20% |
(1)该反应的ΔH
(2)若400K时,将投料比为1:1的NO2和CH4的混合气体共0.04mol,充入一装有催化剂的容器中,充分反应后,平衡时NO2的体积百分数是
(3)在容积相同的两个密闭容器内(装有等量的某种催化剂)先各通入等物质的量的CH4,然后再分别充入等物质的量的NO和NO2,分别进行CH4(g)+4NO(g)⇌2N2(g)+CO2(g)+2H2O(g)和CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)。下图表示选取不同温度,并都在t秒时测定其中NOx转化率,绘得图象如下:

由图可知:①相同温度下,NO转化效率比NO2的低;②250~450℃时NOx转化率随温度升高而增大,450~600℃时NOx转化率随温度升高而减小。解释②的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能。
Ⅰ.工业制备二甲醚的生产流程如下:

催化反应室中(压强2.0~10.0 MPa,温度230~280℃)进行下列反应:
CO(g)+2H2(g)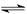 CH3OH(g)ΔH=-90.7 kJ/mol ①
CH3OH(g)ΔH=-90.7 kJ/mol ①
2CH3OH(g)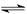 CH3OCH3(g)+H2O(g)ΔH=-23.5 kJ/mol ②
CH3OCH3(g)+H2O(g)ΔH=-23.5 kJ/mol ②
CO(g)+H2O(g)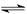 CO2(g)+H2(g)ΔH=-41.2 kJ/mol ③
CO2(g)+H2(g)ΔH=-41.2 kJ/mol ③
(1)甲烷氧化可制得合成气,反应如下:CH4(g)+ O2(g)
O2(g)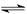 CO(g)+2H2(g) ΔH=-35.6 kJ/mol。该反应是
CO(g)+2H2(g) ΔH=-35.6 kJ/mol。该反应是_______ 反应(填“自发”或“非自发”)。
(2)催化反应室中总反应3CO(g)+3H2(g)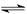 CH3OCH3(g)+CO2(g)的ΔH=
CH3OCH3(g)+CO2(g)的ΔH=___________ 。830℃时反应③的K=1.0,则在催化反应室中反应③的K_______ 1.0(填“>”、“<”或“=”)。
(3)上述反应中,可以循环使用的物质有_______ 。
Ⅱ.如图为绿色电源“二甲醚燃料电池”的工作原理示意图。b电极是_______ 极。

Ⅰ.工业制备二甲醚的生产流程如下:

催化反应室中(压强2.0~10.0 MPa,温度230~280℃)进行下列反应:
CO(g)+2H2(g)
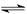 CH3OH(g)ΔH=-90.7 kJ/mol ①
CH3OH(g)ΔH=-90.7 kJ/mol ①2CH3OH(g)
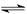 CH3OCH3(g)+H2O(g)ΔH=-23.5 kJ/mol ②
CH3OCH3(g)+H2O(g)ΔH=-23.5 kJ/mol ②CO(g)+H2O(g)
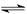 CO2(g)+H2(g)ΔH=-41.2 kJ/mol ③
CO2(g)+H2(g)ΔH=-41.2 kJ/mol ③(1)甲烷氧化可制得合成气,反应如下:CH4(g)+
 O2(g)
O2(g)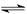 CO(g)+2H2(g) ΔH=-35.6 kJ/mol。该反应是
CO(g)+2H2(g) ΔH=-35.6 kJ/mol。该反应是(2)催化反应室中总反应3CO(g)+3H2(g)
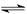 CH3OCH3(g)+CO2(g)的ΔH=
CH3OCH3(g)+CO2(g)的ΔH=(3)上述反应中,可以循环使用的物质有
Ⅱ.如图为绿色电源“二甲醚燃料电池”的工作原理示意图。b电极是

您最近一年使用:0次
【推荐3】大气污染物有 ,(主要指
,(主要指 和
和 )以及
)以及 等污染气体。研究去除这些大气污染物的有效措施是环保领域的重要课题。
等污染气体。研究去除这些大气污染物的有效措施是环保领域的重要课题。
(1) 溶液吸收法。主要反应有;
溶液吸收法。主要反应有;

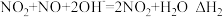
已知: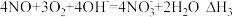
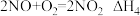
①求
______ (用 、
、 、
、 表示)。
表示)。
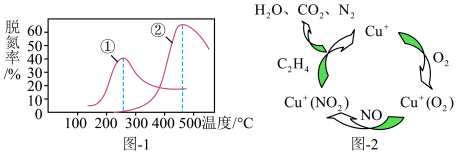
②烟气以固定的流速通过两种不同催化剂①和催化剂②时,在相同时间内测得烟气脱氮率如图-1,结合曲线②分析,当反应温度高于 时,
时, 的去除率迅速下降的原因可能是
的去除率迅速下降的原因可能是________ 。
(2)用稀硝酸吸收 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式______ 。
(3)煤燃烧排放的烟气中含有 和
和 ,采用碱性
,采用碱性 溶液作为吸收剂可同时对烟气进行脱硫,脱硝,在鼓泡反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫,脱硝,在鼓泡反应器中通入含有 和
和 的烟气,反应温度为
的烟气,反应温度为 ,
, 溶液浓度为
溶液浓度为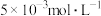 。充分反应足够长的时间后,溶液中离子浓度分析结果如下表。
。充分反应足够长的时间后,溶液中离子浓度分析结果如下表。
①写出 溶液脱氨过程中主要反应的离子方程式
溶液脱氨过程中主要反应的离子方程式_______ 。
②如果采用 替代
替代 ,其脱硫效果会更好。试从化学平衡原理分析,
,其脱硫效果会更好。试从化学平衡原理分析,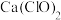 相比
相比 具有的优点是
具有的优点是_______ 。
(4)日前科学家在研究一种以乙烯作为还原剂的脱硝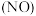 原理,其脱硝机理如图-2所示,若处理标况下
原理,其脱硝机理如图-2所示,若处理标况下 气体,需消耗标况下乙烯
气体,需消耗标况下乙烯_______ L。
 ,(主要指
,(主要指 和
和 )以及
)以及 等污染气体。研究去除这些大气污染物的有效措施是环保领域的重要课题。
等污染气体。研究去除这些大气污染物的有效措施是环保领域的重要课题。(1)
 溶液吸收法。主要反应有;
溶液吸收法。主要反应有;
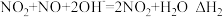
已知:
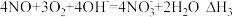
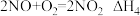
①求

 、
、 、
、 表示)。
表示)。②烟气以固定的流速通过两种不同催化剂①和催化剂②时,在相同时间内测得烟气脱氮率如图-1,结合曲线②分析,当反应温度高于
 时,
时, 的去除率迅速下降的原因可能是
的去除率迅速下降的原因可能是
(2)用稀硝酸吸收
 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式(3)煤燃烧排放的烟气中含有
 和
和 ,采用碱性
,采用碱性 溶液作为吸收剂可同时对烟气进行脱硫,脱硝,在鼓泡反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫,脱硝,在鼓泡反应器中通入含有 和
和 的烟气,反应温度为
的烟气,反应温度为 ,
, 溶液浓度为
溶液浓度为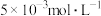 。充分反应足够长的时间后,溶液中离子浓度分析结果如下表。
。充分反应足够长的时间后,溶液中离子浓度分析结果如下表。| 离子 |  |  |  |  |  |
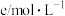 | 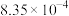 | 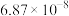 | 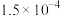 | 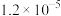 |  |
 溶液脱氨过程中主要反应的离子方程式
溶液脱氨过程中主要反应的离子方程式②如果采用
 替代
替代 ,其脱硫效果会更好。试从化学平衡原理分析,
,其脱硫效果会更好。试从化学平衡原理分析,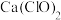 相比
相比 具有的优点是
具有的优点是(4)日前科学家在研究一种以乙烯作为还原剂的脱硝
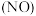 原理,其脱硝机理如图-2所示,若处理标况下
原理,其脱硝机理如图-2所示,若处理标况下 气体,需消耗标况下乙烯
气体,需消耗标况下乙烯
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学反应的焓变通常用实验进行测定,也可理论推算,回答下列问题。
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式_______________________________________ 。
(2)已知某工业生产中甲烷与水蒸气存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用_____________ 反应的△H。(写化学方程式)
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+ Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1
CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=___________ kJ·mol-1
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式
(2)已知某工业生产中甲烷与水蒸气存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+
 Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1 CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】填空。
(1)13gC2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,写出表示该物质燃烧反应的热化学方程式_______ 。
(2)1.00L1.00mol·L-1H2SO4溶液与2.00L1.00mol·L-1NaOH溶液完全反应,放出114.6kJ热量,写出该反应的热化学方程式_______ 。
(3)现有反应CO(g)+2H2(g)=CH3OH(g)过程中能量变化如图所示,写出该反应的热化学方程式_______ ;
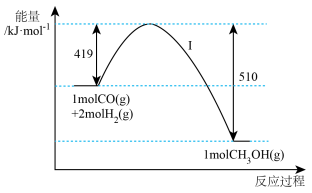
(4)同素异形体相互转化的反应热相当小而且转化速度较慢,有时还很不完全,测定反应热很困难。根据盖斯提出的“不管化学过程是一步完成或几步完成这个总过程的热效应是相等的”观点来计算反应热。
A、已知:①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1
②P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) ΔH2=-738.5kJ·mol-1
P4O10(s) ΔH2=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为_______ 。
B、已知反应:
①H2(g)+ O2(g)=H2O(g) ΔH1
O2(g)=H2O(g) ΔH1
②N2(g)+2O2(g)=2NO2(g) ΔH2
③ N2(g)+
N2(g)+ H2(g)=NH3(g) ΔH3
H2(g)=NH3(g) ΔH3
利用上述三个反应,计算4NH3(g)+7O2(g)=4NO2(g)+6H2O(g)的反应焓变为_______ (用含ΔH1、ΔH2、ΔH3的式子表示)。
(1)13gC2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,写出表示该物质燃烧反应的热化学方程式
(2)1.00L1.00mol·L-1H2SO4溶液与2.00L1.00mol·L-1NaOH溶液完全反应,放出114.6kJ热量,写出该反应的热化学方程式
(3)现有反应CO(g)+2H2(g)=CH3OH(g)过程中能量变化如图所示,写出该反应的热化学方程式

(4)同素异形体相互转化的反应热相当小而且转化速度较慢,有时还很不完全,测定反应热很困难。根据盖斯提出的“不管化学过程是一步完成或几步完成这个总过程的热效应是相等的”观点来计算反应热。
A、已知:①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1
②P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) ΔH2=-738.5kJ·mol-1
P4O10(s) ΔH2=-738.5kJ·mol-1则白磷转化为红磷的热化学方程式为
B、已知反应:
①H2(g)+
 O2(g)=H2O(g) ΔH1
O2(g)=H2O(g) ΔH1②N2(g)+2O2(g)=2NO2(g) ΔH2
③
 N2(g)+
N2(g)+ H2(g)=NH3(g) ΔH3
H2(g)=NH3(g) ΔH3利用上述三个反应,计算4NH3(g)+7O2(g)=4NO2(g)+6H2O(g)的反应焓变为
您最近一年使用:0次
【推荐3】化学能与热能的转化是当今化学研究的热点。回答下列问题:
(1)卤化镁高温分解的相对能量变化如图所示。
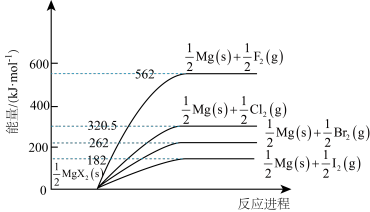
①写出该温度下MgF2(s)分解的热化学方程式:___________ 。
②反应MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=___________ kJ·mol-1。
(2)氢氟酸是一种弱酸,已知25℃时:HF(aq) H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为
H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为___________ ,氢氟酸的中和反应反应热的绝对值大于57.3kJ·mol-1的原因可能是___________ 。
(3)H2与F2在黑暗中混合也会发生剧烈反应,反应的热化学方程式为H2(g)+F2(g)=2HF(g) △H=—536.6kJ·mol-1,查阅文献,两种化学键键能数据如表:
则F2(g)=2F(g) △H=___________ kJ·mol-1。
(1)卤化镁高温分解的相对能量变化如图所示。
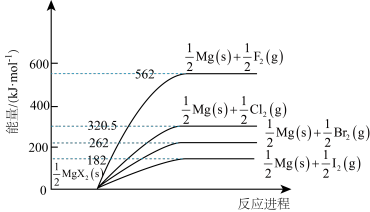
①写出该温度下MgF2(s)分解的热化学方程式:
②反应MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=
(2)氢氟酸是一种弱酸,已知25℃时:HF(aq)
 H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为
H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为(3)H2与F2在黑暗中混合也会发生剧烈反应,反应的热化学方程式为H2(g)+F2(g)=2HF(g) △H=—536.6kJ·mol-1,查阅文献,两种化学键键能数据如表:
| 化学键 | H—H | F—H |
| E/(kJ·mol-1) | 436 | 565 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 新型材料应用前景广泛,具有高导热率、高强度等特点,其制备与性质研究成为热点.相关数据如下:
新型材料应用前景广泛,具有高导热率、高强度等特点,其制备与性质研究成为热点.相关数据如下:
(1)根据元素性质判断, 中N的化合价为
中N的化合价为_____________ .
(2) 的制备有两种不同的方法:
的制备有两种不同的方法:
①化学气相沉积法.
Ⅰ.一定温度下,以 气体和
气体和 为原料制备
为原料制备 ,反应的化学方程式是
,反应的化学方程式是_____________ .
Ⅱ.上述反应适宜的温度范围是_____________ ℃(填字母).
a.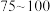 b.
b.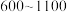 c.
c.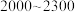
②铝粉直接氨化法.
 与
与 可直接化合为
可直接化合为 固体,
固体, 能将
能将 包裹,反应难以继续进行.控制温度,在
包裹,反应难以继续进行.控制温度,在 粉中均匀掺入适量
粉中均匀掺入适量 粉,可使
粉,可使 几乎全部转化为
几乎全部转化为 固体.
固体.
(3) 的原子结构示意图为
的原子结构示意图为_____________ ;
(4)结合信息分析,该过程发生的反应有:_____________ 、_____________ 和 .
.
(5) 材料在保存和使用时,应该避免与水直接接触,以防止材料发生水解反应.已知在水解反应中,元素的化合价保持不变,请完成
材料在保存和使用时,应该避免与水直接接触,以防止材料发生水解反应.已知在水解反应中,元素的化合价保持不变,请完成 水解反应的化学方程式:
水解反应的化学方程式:________
__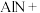 ____
____ _____________+_____________↑
_____________+_____________↑
 新型材料应用前景广泛,具有高导热率、高强度等特点,其制备与性质研究成为热点.相关数据如下:
新型材料应用前景广泛,具有高导热率、高强度等特点,其制备与性质研究成为热点.相关数据如下:| 物质 | 熔点/℃ | 沸点/℃ | 与 反应温度/℃ 反应温度/℃ | 相应化合物分解温度/℃ |
 | 660 | 2467 | 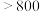 |  ( (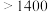 升华) 升华)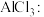 ( (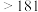 升华) 升华) |
 | 649 | 1090 | 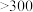 |  |
 中N的化合价为
中N的化合价为(2)
 的制备有两种不同的方法:
的制备有两种不同的方法:①化学气相沉积法.
Ⅰ.一定温度下,以
 气体和
气体和 为原料制备
为原料制备 ,反应的化学方程式是
,反应的化学方程式是Ⅱ.上述反应适宜的温度范围是
a.
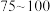 b.
b.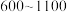 c.
c.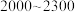
②铝粉直接氨化法.
 与
与 可直接化合为
可直接化合为 固体,
固体, 能将
能将 包裹,反应难以继续进行.控制温度,在
包裹,反应难以继续进行.控制温度,在 粉中均匀掺入适量
粉中均匀掺入适量 粉,可使
粉,可使 几乎全部转化为
几乎全部转化为 固体.
固体.(3)
 的原子结构示意图为
的原子结构示意图为(4)结合信息分析,该过程发生的反应有:
 .
.(5)
 材料在保存和使用时,应该避免与水直接接触,以防止材料发生水解反应.已知在水解反应中,元素的化合价保持不变,请完成
材料在保存和使用时,应该避免与水直接接触,以防止材料发生水解反应.已知在水解反应中,元素的化合价保持不变,请完成 水解反应的化学方程式:
水解反应的化学方程式:__
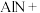 ____
____ _____________+_____________↑
_____________+_____________↑
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷酸氢二铵[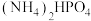 ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备
]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备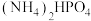 ,装置如图所示(夹持和搅拌装置已省略)。
,装置如图所示(夹持和搅拌装置已省略)。
(1)装置中活塞 的作用为
的作用为_______ 。实验过程中,当出现_______ 现象时,应及时关闭 ,打开
,打开 。
。
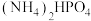 ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备
]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备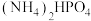 ,装置如图所示(夹持和搅拌装置已省略)。
,装置如图所示(夹持和搅拌装置已省略)。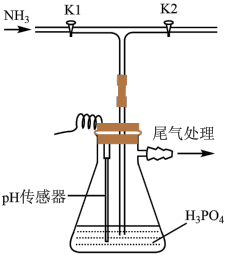
(1)装置中活塞
 的作用为
的作用为 ,打开
,打开 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4作催化剂,即发生反应,生成硫酸铜。其反应过程的第2步是:2Fe3++Cu===2Fe2++Cu2+,
(1)请写出其第l步反应的离子方程式__________________ 。
(2)总化学反应方程式____________________________
(3)利用Cu制备CuSO4的另一种方法可用化学方程式表示为_______________ 。
(4)以上两种方法______________ (填“前”、“后”) 者好,这样做的好处是
①_____________________________ ,②_________________________________ 。
(1)请写出其第l步反应的离子方程式
(2)总化学反应方程式
(3)利用Cu制备CuSO4的另一种方法可用化学方程式表示为
(4)以上两种方法
①
您最近一年使用:0次



