化学能与热能的转化是当今化学研究的热点。回答下列问题:
(1)卤化镁高温分解的相对能量变化如图所示。
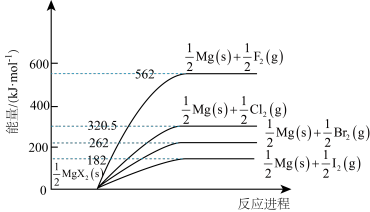
①写出该温度下MgF2(s)分解的热化学方程式:___________ 。
②反应MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=___________ kJ·mol-1。
(2)氢氟酸是一种弱酸,已知25℃时:HF(aq) H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为
H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为___________ ,氢氟酸的中和反应反应热的绝对值大于57.3kJ·mol-1的原因可能是___________ 。
(3)H2与F2在黑暗中混合也会发生剧烈反应,反应的热化学方程式为H2(g)+F2(g)=2HF(g) △H=—536.6kJ·mol-1,查阅文献,两种化学键键能数据如表:
则F2(g)=2F(g) △H=___________ kJ·mol-1。
(1)卤化镁高温分解的相对能量变化如图所示。
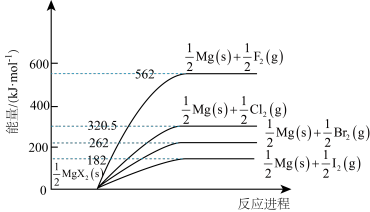
①写出该温度下MgF2(s)分解的热化学方程式:
②反应MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=
(2)氢氟酸是一种弱酸,已知25℃时:HF(aq)
 H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为
H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为(3)H2与F2在黑暗中混合也会发生剧烈反应,反应的热化学方程式为H2(g)+F2(g)=2HF(g) △H=—536.6kJ·mol-1,查阅文献,两种化学键键能数据如表:
| 化学键 | H—H | F—H |
| E/(kJ·mol-1) | 436 | 565 |
2023高三·全国·专题练习 查看更多[1]
(已下线)化学反应的热效应
更新时间:2023-12-18 20:51:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】依据事实,写出下列反应的热化学方程式。
(1)16gCH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量,写出CH4燃烧的热化学方程式:_______ 。
(2)实验测得25℃、101kPa时1molH2完全燃烧放出285.8kJ的热量,写出H2燃烧的热化学方程式:_______ 。
(3)1.0L1.0mol/LH2SO4溶液与2.0L1.0mol/LNaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式。_______
(4)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为_______
(5)在1.01×105Pa时,16gS在足量的氧气中充分燃烧生成二氧化硫,放出148.5KJ的热量,则S的燃烧热为_______ ,S燃烧的热化学方程式为_______ 。
(1)16gCH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量,写出CH4燃烧的热化学方程式:
(2)实验测得25℃、101kPa时1molH2完全燃烧放出285.8kJ的热量,写出H2燃烧的热化学方程式:
(3)1.0L1.0mol/LH2SO4溶液与2.0L1.0mol/LNaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式。
(4)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为
(5)在1.01×105Pa时,16gS在足量的氧气中充分燃烧生成二氧化硫,放出148.5KJ的热量,则S的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】1.00 L 1.00 mol·L-1硫酸溶液与2.00 L 1.00 mol·L-1NaOH溶液完全反应,放出114.6 kJ的热量,写出该反应的热化学方程式__________________________________________ ;由此得出,强酸与强碱在稀溶液中反应的中和热为_______________ 。若1molHF在水溶液中完全电离时放出10.4 kJ的热量,则当稀溶液中有1mol HF跟1mol NaOH反应时的热化学方程式为_____________________________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)对烟道气中的 进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由
进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,每生成
的能量变化如图所示,每生成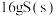 ,该反应
,该反应___________ (填“放出”或“吸收”)的热量为___________ kJ。
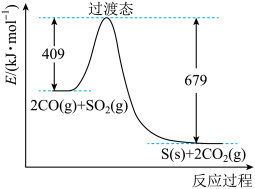
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
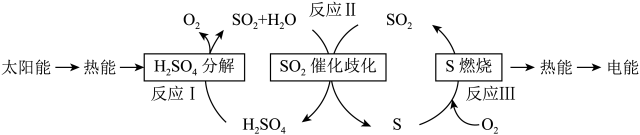
反应Ⅰ: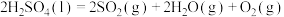
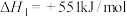
反应Ⅲ:
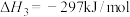
反应Ⅱ的热化学方程式为___________ 。
(3)近年来空气污染日益严重,原因之一是汽车尾气中含有NO、 、CO等气体。为消除汽车尾气的污染,可采取:NO和CO在催化转换器中发生如下反应:
、CO等气体。为消除汽车尾气的污染,可采取:NO和CO在催化转换器中发生如下反应:

 ;
;
已知: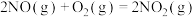
 ;
;
CO的燃烧热为 ;
;
 与CO发生反应的热化学方程式:
与CO发生反应的热化学方程式: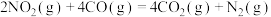

___________ (用 、
、 、
、 表示)。
表示)。
(4)工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下, 被空气中的
被空气中的 氧化为
氧化为 。
。 是钒催化剂的活性成分,
是钒催化剂的活性成分,
郭汗贤等提出: 在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:
在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:
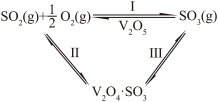
①有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
由此计算反应Ⅰ的
___________ kJ/mol。
②反应Ⅱ、Ⅲ的化学方程式为___________ 、___________ 。
(1)对烟道气中的
 进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由
进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,每生成
的能量变化如图所示,每生成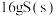 ,该反应
,该反应
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应Ⅰ:
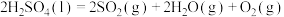
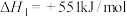
反应Ⅲ:

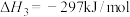
反应Ⅱ的热化学方程式为
(3)近年来空气污染日益严重,原因之一是汽车尾气中含有NO、
 、CO等气体。为消除汽车尾气的污染,可采取:NO和CO在催化转换器中发生如下反应:
、CO等气体。为消除汽车尾气的污染,可采取:NO和CO在催化转换器中发生如下反应:
 ;
;已知:
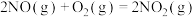
 ;
;CO的燃烧热为
 ;
; 与CO发生反应的热化学方程式:
与CO发生反应的热化学方程式: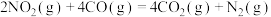

 、
、 、
、 表示)。
表示)。(4)工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下,
 被空气中的
被空气中的 氧化为
氧化为 。
。 是钒催化剂的活性成分,
是钒催化剂的活性成分,郭汗贤等提出:
 在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:
在对反应Ⅰ的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如下:
①有关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
| 化学键 | 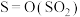 | 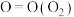 |  |
| 能量/kJ | 535 | 496 | 472 |

②反应Ⅱ、Ⅲ的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1____ ΔH2(填“>”、“<”或“=”,下同)。
(2)相同条件下,1 mol氮气和氢气反应断键吸收能量____ 形成2 mol氨气成键所放出的能量。
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1___ ΔH2。①P4(白磷,s)+5O2(g)= 2P2O5(s) ΔH1, ②4P(红磷,s)+5O2(g)= 2P2O5(s) ΔH2。
(4)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36 kJ热量,该反应的热化学方程式是_______ 。
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式是_______ 。
(6)已知:C(s)+O2(g)=CO2(g) △H=-437.3kJ•mol﹣1,H2(g)+ O2(g)=H2O(g) △H=-285.8kJ•mol﹣1,CO(g)+
O2(g)=H2O(g) △H=-285.8kJ•mol﹣1,CO(g)+ O2(g)=CO2(g) △H=-283.0kJ•mol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=
O2(g)=CO2(g) △H=-283.0kJ•mol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__ kJ•mol﹣1。
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1
(2)相同条件下,1 mol氮气和氢气反应断键吸收能量
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1
(4)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36 kJ热量,该反应的热化学方程式是
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式是
(6)已知:C(s)+O2(g)=CO2(g) △H=-437.3kJ•mol﹣1,H2(g)+
 O2(g)=H2O(g) △H=-285.8kJ•mol﹣1,CO(g)+
O2(g)=H2O(g) △H=-285.8kJ•mol﹣1,CO(g)+ O2(g)=CO2(g) △H=-283.0kJ•mol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=
O2(g)=CO2(g) △H=-283.0kJ•mol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)已知常温下红磷比白磷稳定,在下列反应中:
①4P(红磷,s)+5O2(g)=P4O10(s)△H=﹣Q1kJ•mol﹣1
②P4(白磷,s)+5O2(g)=P4O10(s)△H=﹣Q2kJ•mol﹣1
若Q1、Q2均大于零,则Q1和Q2的关系为_______(填字母序号)。
(2)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(中的ΔH表示生成1 mol产物的数据)。

根据上图回答下列问题:
红磷P(s)和Cl2(g)反应生成PCl5(g)的热化学方程式是_______ 。
(3)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,表示氢气燃烧热的热化学方程式是_______ 。
(4)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)的反应焓变△H4为_______ (用含△H1、△H2、△H3的式子表示)。
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g) +2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s) +O2(g) =CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g) + O2(g) =H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g) =H2O(l) ΔH3=-285.8 kJ·mol-1
则反应2C(s) +2H2(g) +O2(g)=CH3COOH(l)的焓变ΔH为_______
(1)已知常温下红磷比白磷稳定,在下列反应中:
①4P(红磷,s)+5O2(g)=P4O10(s)△H=﹣Q1kJ•mol﹣1
②P4(白磷,s)+5O2(g)=P4O10(s)△H=﹣Q2kJ•mol﹣1
若Q1、Q2均大于零,则Q1和Q2的关系为_______(填字母序号)。
| A.Q1>Q2 | B.Q1=Q2 | C.Q1<Q2 | D.无法确定 |

根据上图回答下列问题:
红磷P(s)和Cl2(g)反应生成PCl5(g)的热化学方程式是
(3)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,表示氢气燃烧热的热化学方程式是
(4)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)的反应焓变△H4为
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g) +2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s) +O2(g) =CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g) +
 O2(g) =H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g) =H2O(l) ΔH3=-285.8 kJ·mol-1则反应2C(s) +2H2(g) +O2(g)=CH3COOH(l)的焓变ΔH为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时电极反应式为负极:C6Li-xe-=C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)正极:Li1-xMO2+xLi++xe-=LiMO2(LiMO2表示含锂的过渡金属氧化物)。
(1)锂电池放电时电池的反应式为_______ 。
(2)假设放电过程中消耗负极材料5.6 g,转移的电子数目为_______ (NA为阿伏加德罗常数值)。
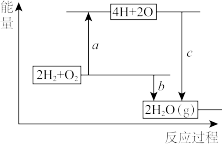
(3)已知破坏1 mol H-H键、1 mol O═O键、1mol H-O键时分别需要吸收436 kJ、498 kJ、465 kJ的能量。图表示H2、O2转化为水的反应过程能量变化,则b=_______ 。
(4)某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了如下平行实验:
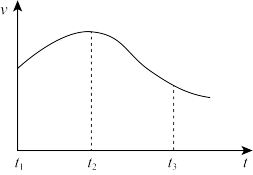
实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示。
实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
①试分析实验①中t1~t2速率增大的主要原因是_______ 。t2~t3速率减小的主要原因是_______ 。
②实验②放出氢气的量减少的原因是_______ 。
③某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?_______ (填“正确”或“不正确”)。请选择下列相应的a或b作答_______ 。
a.若不正确,请说明原因。
b.若正确则写出实验③中原电池的正极电极反应式。
(1)锂电池放电时电池的反应式为
(2)假设放电过程中消耗负极材料5.6 g,转移的电子数目为
(3)已知破坏1 mol H-H键、1 mol O═O键、1mol H-O键时分别需要吸收436 kJ、498 kJ、465 kJ的能量。图表示H2、O2转化为水的反应过程能量变化,则b=

(4)某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了如下平行实验:

实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示。
实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
①试分析实验①中t1~t2速率增大的主要原因是
②实验②放出氢气的量减少的原因是
③某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?
a.若不正确,请说明原因。
b.若正确则写出实验③中原电池的正极电极反应式。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】乙苯催化脱氢制苯乙烯反应:

(1)已知:
计算上述反应的△H=____________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________ (用含α等字母的代数式表示)。

(1)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ·molˉ1 | 412 | 348 | 612[ | 436 |
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某化学反应中,设反应物的总能量为E1,生成物的总能量为E2,
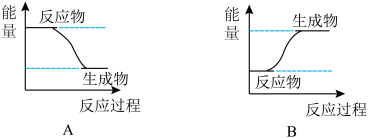
I.若E1>E2,则该反应为_____ (填“放热”或“吸热”)反应。该反应可用图____ (填“A”或“B”)表示。
II.若E1<E2,则该反应为______ (填“放热”或“吸热”)反应。该反应可用图_____ (填“A”或“B”)表示
III.下表中的数据是破坏1mol物质中的化学键所消耗的最小能量:
根据上述数据回答下列问题:
(1)下列物质本身具有的能量最低的是( )
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中最稳定的是( )
A.HCl B.HBr C.HI
(3)X2+H2===2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?_______ 。
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是_____ (填写化学式)。

I.若E1>E2,则该反应为
II.若E1<E2,则该反应为
III.下表中的数据是破坏1mol物质中的化学键所消耗的最小能量:
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 键能(kJ/mol) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(1)下列物质本身具有的能量最低的是
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中最稳定的是
A.HCl B.HBr C.HI
(3)X2+H2===2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是
您最近一年使用:0次



