化学反应的焓变通常用实验进行测定,也可理论推算,回答下列问题。
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式_______________________________________ 。
(2)已知某工业生产中甲烷与水蒸气存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用_____________ 反应的△H。(写化学方程式)
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+ Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1
CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=___________ kJ·mol-1
(1)实验测得,1 g CH3OH(l)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式
(2)已知某工业生产中甲烷与水蒸气存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) △H2
iii.CH4(g)=C(s)+2H2(g) △H3
……
Iii为积炭反应,利用△H1和△H2计算△H3时,还需要利用
(3)氯化氢转化为氯气的催化过程如下:
CuCl2(s)=CuCl(s)+
 Cl2(g) △H1=+83 kJ·mol-1
Cl2(g) △H1=+83 kJ·mol-1 CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) △H2=-20 kJ·mol-1
Cl2(g) △H2=-20 kJ·mol-1CuO(s)+2HCl(g)= CuCl2(s)+H2O(g) △H3=-121 kJ·mol-1
则4HCl(g)+ O2(g)= 2Cl2(g)+2H2O(g)的△H=
更新时间:2019-12-01 23:02:29
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】
(1)在101 kPa时,1 mol CH4完全燃烧生成CO2和液态H2O,放出890.3 kJ的热量,CH4的燃烧热为______ 。1120L CH4(标准状况)燃烧后所产生的热量为______
(2)已知0.5 mol甲烷与0.5 mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是:______
(1)在101 kPa时,1 mol CH4完全燃烧生成CO2和液态H2O,放出890.3 kJ的热量,CH4的燃烧热为
(2)已知0.5 mol甲烷与0.5 mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:___ .
(2)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)ΔH=+489.0 kJ·mol-1①
CO(g)+O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1②
C(石墨)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1③
则4Fe(s)+3O2(g)=2Fe2O3(s)的ΔH为___
(2)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)ΔH=+489.0 kJ·mol-1①
CO(g)+O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1②
C(石墨)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1③
则4Fe(s)+3O2(g)=2Fe2O3(s)的ΔH为
您最近一年使用:0次
【推荐3】(1)在含Mg2+、Al3+、H+、Cl-的混合溶液中滴加NaOH溶液,与OH-发生反应的顺序为:___ 、___ 、Mg2+和___ 。在NaOH滴加过量后的澄清溶液中,浓度最高的离子是___ 。
(2)加热条件下,一氧化碳与硫反应可生成硫氧化碳(COS)。
①写出S原子核外最外层电子排布式___ 。
②每摩尔COS气体中含电子___ NA(阿佛加得罗常数)个。
③写出COS的电子式。___ 。
(3)海水中含量较高的金属元素有Na、Mg、Ca等,地壳中含量最高的Al、Fe在海水中的含量却极低,以至食盐提纯过程一般无需考虑除Fe3+、Al3+或AlO2-。为什么海水中Al元素的含量极低?___ 。
(4)某些非金属单质可与水发生置换反应,如2F2+2H2O=4HF+O2。非金属单质与水发生置换反应的另一个熟知实例是(用热化学方程式表示,热值用Q表示,Q>0):___ 。
(5)一银制摆件因日久在表面生成硫化银而变黑。使银器复原的一种方法是利用原电池原理:在一铝锅中盛盐水,将该银器浸入,并与锅底接触,放置一段时间,黑色褪去。
①构成原电池负极的材料是___ 。
②操作后可闻盐水微有臭味,估计具有臭味的物质是___ 。
(2)加热条件下,一氧化碳与硫反应可生成硫氧化碳(COS)。
①写出S原子核外最外层电子排布式
②每摩尔COS气体中含电子
③写出COS的电子式。
(3)海水中含量较高的金属元素有Na、Mg、Ca等,地壳中含量最高的Al、Fe在海水中的含量却极低,以至食盐提纯过程一般无需考虑除Fe3+、Al3+或AlO2-。为什么海水中Al元素的含量极低?
(4)某些非金属单质可与水发生置换反应,如2F2+2H2O=4HF+O2。非金属单质与水发生置换反应的另一个熟知实例是(用热化学方程式表示,热值用Q表示,Q>0):
(5)一银制摆件因日久在表面生成硫化银而变黑。使银器复原的一种方法是利用原电池原理:在一铝锅中盛盐水,将该银器浸入,并与锅底接触,放置一段时间,黑色褪去。
①构成原电池负极的材料是
②操作后可闻盐水微有臭味,估计具有臭味的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
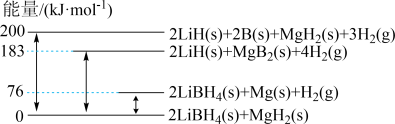
【推荐1】LiBH4是近年来常用的储氢材料。2LiBH4/MgH2体系放氢焓变示意图如下,则Mg(s)+2B(s)=MgB2(s) ΔH=_____ 。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
已知:
①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+ O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ O2 (g)=H2O(g) ΔH3=-242 kJ·mol-1
O2 (g)=H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为___________ kJ·mol-1。
(2)已知4.4 g CO2气体与H2经催化加氢生成CH3OH气体和水蒸气时放出4.95 kJ的能量。该反应的热化学方程式为:___________ 。
(3)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1___________ ΔH2(填“>”“<”或“=”,下同)。
(4)氨气是一种重要的物质,可用于制取化肥和硝酸等。已知H—H键、N—H键、N≡N键的键能分别是436 kJ·mol-1、391 kJ·mol-1、946 kJ·mol-1。写出合成氨的热化学方程式:___________ 。
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
已知:
①C4H10(g)=C4H8(g)+H2(g) ΔH1
②C4H10(g)+
 O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)=C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1③H2(g)+
 O2 (g)=H2O(g) ΔH3=-242 kJ·mol-1
O2 (g)=H2O(g) ΔH3=-242 kJ·mol-1反应①的ΔH1为
(2)已知4.4 g CO2气体与H2经催化加氢生成CH3OH气体和水蒸气时放出4.95 kJ的能量。该反应的热化学方程式为:
(3)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1
(4)氨气是一种重要的物质,可用于制取化肥和硝酸等。已知H—H键、N—H键、N≡N键的键能分别是436 kJ·mol-1、391 kJ·mol-1、946 kJ·mol-1。写出合成氨的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。已知25℃,100kPa时:
①1mol葡萄糖[C6H12O6(s)]完全燃烧生成CO2(g)和H2O(l),放出2804kJ热量。
②CO(g)+ O2(g)=CO2(g) ΔH=-283kJ·mol-1。
O2(g)=CO2(g) ΔH=-283kJ·mol-1。
(1)25℃时,CO2(g)与H2O(l)经光合作用生成葡萄糖[C6H12O6(s)]和O2(g)的热化学方程式为____ 。
(2)25℃,100kPa时,气态分子断开1mol化学键的焓变称为键焓。已知O=O、C≡O键的键焓分别为495kJ·mol-1、799kJ·mol-1,CO2(g)分子中碳氧键的键焓为____ kJ·mol-1。
①1mol葡萄糖[C6H12O6(s)]完全燃烧生成CO2(g)和H2O(l),放出2804kJ热量。
②CO(g)+
 O2(g)=CO2(g) ΔH=-283kJ·mol-1。
O2(g)=CO2(g) ΔH=-283kJ·mol-1。(1)25℃时,CO2(g)与H2O(l)经光合作用生成葡萄糖[C6H12O6(s)]和O2(g)的热化学方程式为
(2)25℃,100kPa时,气态分子断开1mol化学键的焓变称为键焓。已知O=O、C≡O键的键焓分别为495kJ·mol-1、799kJ·mol-1,CO2(g)分子中碳氧键的键焓为
您最近一年使用:0次



