硫、氮元素是高中化学学习的两种重要非金属元素,其价-类二维图分别如图。
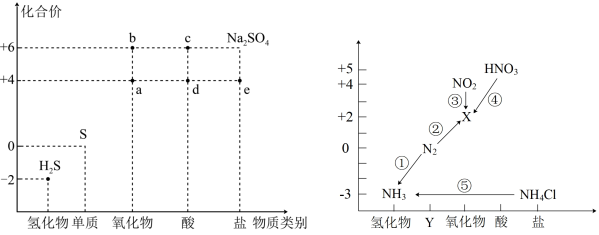
(1)图中物质“d”的化学式是___________ ;若不加任何其它试剂完成转化过程⑤,则⑤的反应为___________ 反应(填“吸热”或“放热”)。
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
(3)写出反应③的离子方程式___________ 。
(4)a的水溶液与H2S发生反应可观察到的实验现象是___________ 。
(5)若e为钾元素的正盐,能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O 被还原为Cr3+,请配平化学方程式:
被还原为Cr3+,请配平化学方程式:_________
___________K2SO3+___________K2Cr2O7+___________H2SO4=___________Cr2(SO4)3+___________K2SO4+___________H2O
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:
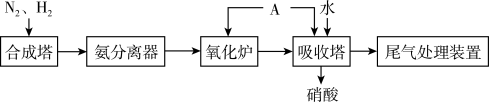
已知:用NaOH溶液进行尾气处理时的化学反应为: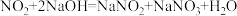 ,
,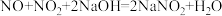 。
。
为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积必须满足的条件是:
___________ 。

(1)图中物质“d”的化学式是
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
| A.Ba(NO3)2溶液 | B.CaCl2溶液 | C.H2O2溶液 | D.Na2CO3溶液 |
(4)a的水溶液与H2S发生反应可观察到的实验现象是
(5)若e为钾元素的正盐,能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O
 被还原为Cr3+,请配平化学方程式:
被还原为Cr3+,请配平化学方程式:___________K2SO3+___________K2Cr2O7+___________H2SO4=___________Cr2(SO4)3+___________K2SO4+___________H2O
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:

已知:用NaOH溶液进行尾气处理时的化学反应为:
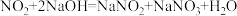 ,
,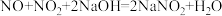 。
。为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积必须满足的条件是:

更新时间:2023-04-15 20:06:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】人体中含有铁元素,+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。
(1)误服亚硝酸盐会使人中毒,是因为二价铁被__ (填“氧化”或“还原”)成三价铁,此时服用维生素C可缓解亚硝酸盐中毒,维生素C在此过程中是作__ (填“氧化剂”或“还原剂”)。
(2)现有一瓶久置的FeSO4溶液,请设计实验检验其中是否含有Fe3+:___ 。Fe2+在空气中易发生氧化还原反应而变质,可加入__ (填化学式)来防止其变质,而又不会使溶液中有新的杂质。
(3)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaClO氧化Fe(OH)3来制备,请配平反应方程式:__ ClO-+___ Fe(OH)3+___ OH-=___ FeO +
+__ +__ Cl-
向制得的Na2FeO4溶液中加入适量的饱和KCl溶液会析出K2FeO4,写出该反应的化学方程式:__ 。
(1)误服亚硝酸盐会使人中毒,是因为二价铁被
(2)现有一瓶久置的FeSO4溶液,请设计实验检验其中是否含有Fe3+:
(3)高铁酸钾(K2FeO4)是水处理过程中使用的一种新型消毒剂。可在碱性条件下,用NaClO氧化Fe(OH)3来制备,请配平反应方程式:
 +
+向制得的Na2FeO4溶液中加入适量的饱和KCl溶液会析出K2FeO4,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】羰基硫( ,沸点:
,沸点: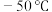 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:
(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:__________________________________ .
(2)以 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去):
 溶液
溶液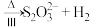
①反应Ⅰ中另一种产物是_____________ 。
②写出反应Ⅲ的离子方程式:_____________________________________________ 。
(3) 和
和 反应是制备
反应是制备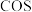 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入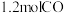 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含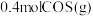 。
。
①平衡时, 的浓度为
的浓度为_____________  ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率_____________  。
。
②下列描述中能说明上述反应已达平衡状态的是_____________ (填字母)。
a.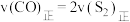
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
 ,沸点:
,沸点: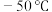 )又称氧硫化碳,其结构与
)又称氧硫化碳,其结构与 类似.回答下列问题:
类似.回答下列问题:(1)实验室中通常用粉状硫氰化钾、水和浓硫酸反应制备
 ,同时生成两种硫酸氢盐。写出该反应的化学方程式:
,同时生成两种硫酸氢盐。写出该反应的化学方程式:(2)以
 为原料制备其他含硫物质的流程如下(部分产物已略去):
为原料制备其他含硫物质的流程如下(部分产物已略去): 溶液
溶液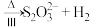
①反应Ⅰ中另一种产物是
②写出反应Ⅲ的离子方程式:
(3)
 和
和 反应是制备
反应是制备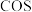 的另一种方法。恒温下,向体积为
的另一种方法。恒温下,向体积为 密闭容器中分别充入
密闭容器中分别充入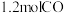 和
和 ,发生反应:
,发生反应: 后达到平衡状态,测得混合体系中含
后达到平衡状态,测得混合体系中含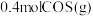 。
。①平衡时,
 的浓度为
的浓度为 ;
; 内用
内用 表示的化学反应速率
表示的化学反应速率 。
。②下列描述中能说明上述反应已达平衡状态的是
a.
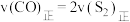
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器内气体压强保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】亚硝酸(HNO2)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多。回答下列问题:
(1)亚硝酸是一种中强酸,写出其电离方程式____________________________ 。
(2)HNO2及NaNO2均可将溶液中的I-氧化为I2,这个反应可用于分析测定。
①HNO2中,N元素的化合价为_________________ 。
②在酸性条件下,NaNO2与KI按物质的量之比l:1恰好完全反应,含氮产物为_______ (填化学式)。
③要得到稳定的HN02溶液,可以往冷的浓NaNO2溶液中加入或通入某种物质,下列物质中不适合使用的
是_________ (填序号)。
a.磷酸
b.二氧化碳
c.稀硫酸
d.二氧化硫
e.次氯酸
(3)HNO2的工业制法是:将二氧化氮和一氧化氮的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液。写出该反应的化学方程式:____________ 。
(4)亚硝酸盐对人体健康的损害不亚于农药。可采用电解法除去。电解含Ce3+、NO2- 的废水除去NO2- ,其次是再生Ce4+,其原理如图所示。
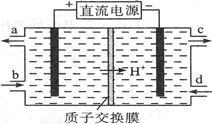
①Ce4+从电解槽的___________ (填字母序号)口流出。
②写出阴极的电极反应式_____________________ 。
(1)亚硝酸是一种中强酸,写出其电离方程式
(2)HNO2及NaNO2均可将溶液中的I-氧化为I2,这个反应可用于分析测定。
①HNO2中,N元素的化合价为
②在酸性条件下,NaNO2与KI按物质的量之比l:1恰好完全反应,含氮产物为
③要得到稳定的HN02溶液,可以往冷的浓NaNO2溶液中加入或通入某种物质,下列物质中不适合使用的
是
a.磷酸
b.二氧化碳
c.稀硫酸
d.二氧化硫
e.次氯酸
(3)HNO2的工业制法是:将二氧化氮和一氧化氮的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液。写出该反应的化学方程式:
(4)亚硝酸盐对人体健康的损害不亚于农药。可采用电解法除去。电解含Ce3+、NO2- 的废水除去NO2- ,其次是再生Ce4+,其原理如图所示。

①Ce4+从电解槽的
②写出阴极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】尽管氮元素在地壳中的含量较低(主要以硝酸盐的形式存在),但是大气中有丰富的氮气,这为氨和硝酸的广泛应用提供了可能。
(1)氮气的电子式为________ ,雷电作用能进行氮的固定,写出反应方程式________ 。
(2)食物蕴含的营养物质中,含氮的高分子化合物是_____ (填名称,下同),其水解的最终产物为________ 。
(3)土壤中的NH4+在硝化细菌的催化作用下可被氧化成NO3﹣,写出其离子方程式:________ 。
(4)某镁铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2L,再向溶液中加入过量氨水,充分反应后过滤.若沉淀质量为40.8g,则合金的质量为________ g。
(1)氮气的电子式为
(2)食物蕴含的营养物质中,含氮的高分子化合物是
(3)土壤中的NH4+在硝化细菌的催化作用下可被氧化成NO3﹣,写出其离子方程式:
(4)某镁铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2L,再向溶液中加入过量氨水,充分反应后过滤.若沉淀质量为40.8g,则合金的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请按要求回答下列问题:
(1)氨气极易溶于水,其水溶液显___________ (填“酸”、“碱”或“中”)性;
(2)加热时,浓硫酸可与碳发生反应:___________ 。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性;
(3)写出NH4HCO3受热分解的化学方程式:___________ ;
(4)写出NH4Cl和Ca(OH)2反应的化学方程式:___________ ;
(5)写出Cu与浓HNO3反应的化学方程式___________ 。
(1)氨气极易溶于水,其水溶液显
(2)加热时,浓硫酸可与碳发生反应:
(3)写出NH4HCO3受热分解的化学方程式:
(4)写出NH4Cl和Ca(OH)2反应的化学方程式:
(5)写出Cu与浓HNO3反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮元素是植物不可缺少的一种主要营养元素。游离态的N分子不能被大多数植物直接吸收,植物吸收和利用效果最好的是 和
和 。回答下列问题:
。回答下列问题:
(1)氮的固定包含人工固氮和___________ ;人工固氮中工业合成氨的化学方程式为___________ 。
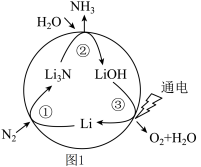
(2)一种新型人工固氮的原理如图1所示,这种固氮方式的总反应方程式为___________ (反应条件省略);反应①②③中属于氧化还原反应的是___________ (填编号)。
(3)碳酸氢铵作肥料时,要遵循“五不施”原则。其中有“烈日当空不施”,原因是___________ (用化学方程式表示)。
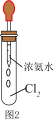
(4)自然界中的微生物也可将氮的化合态NH3转化为游离态的N2,在实验室可用Cl2实现此过程。如图2所示,试管中集满干燥的Cl2,迅速用胶塞塞紧,滴入足量浓氨水。开始时,试管内发生反应:2NH3+3Cl2=N2+6HCl,并产生白烟。白烟的化学式为___________ ,将反应后的试管浸入水中并倒立,在水下打开胶塞,最终进入试管内的水约占试管总体积的___________ 。
 和
和 。回答下列问题:
。回答下列问题:(1)氮的固定包含人工固氮和
(2)一种新型人工固氮的原理如图1所示,这种固氮方式的总反应方程式为

(3)碳酸氢铵作肥料时,要遵循“五不施”原则。其中有“烈日当空不施”,原因是
(4)自然界中的微生物也可将氮的化合态NH3转化为游离态的N2,在实验室可用Cl2实现此过程。如图2所示,试管中集满干燥的Cl2,迅速用胶塞塞紧,滴入足量浓氨水。开始时,试管内发生反应:2NH3+3Cl2=N2+6HCl,并产生白烟。白烟的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:

(1)Y的化学式为_________ ,检验Y所用的试剂是________________ 。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为__________________ 。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是_______ (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4d.SO2 + Na2SO4
(4)将X与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为__________ 。

(1)Y的化学式为
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4d.SO2 + Na2SO4
(4)将X与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
I.以下是硫元素形成的部分物质的价类二维图及相互转化的部分信息。
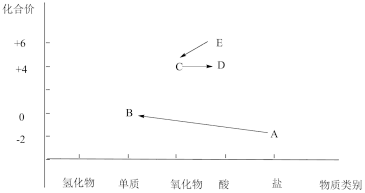
(1)A是一种钠盐,它的电离方程式是___________ 。加入氯水,可完成从A →B的转化,氯水起到的作用是___________ 。
(2)D的化学式是___________ ,写出C →D的化学方程式___________ 。
(3)写出E →C的化学方程式___________ 。
II.双碱法脱除烟气中SO2的过程如下图所示。
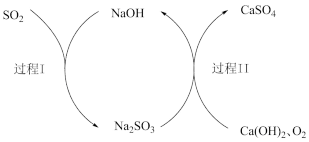
(4)过程I的化学方程式是___________ ,该反应中,含S元素物质发生了类别间的转化,具体来说是___________ 类物质向___________ 类物质的转化。
(5)过程II中含硫元素物质发生了___________ 反应 (填“氧化”或者“还原”),反应中氧化剂是___________ 。 写出该反应的化学方程式___________ 。
(6)该过程中可以循环利用的物质是___________ 。
I.以下是硫元素形成的部分物质的价类二维图及相互转化的部分信息。

(1)A是一种钠盐,它的电离方程式是
(2)D的化学式是
(3)写出E →C的化学方程式
II.双碱法脱除烟气中SO2的过程如下图所示。

(4)过程I的化学方程式是
(5)过程II中含硫元素物质发生了
(6)该过程中可以循环利用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某化学学习小组为了探究镁和二氧化硫的反应产物,进行如下实验。
Ⅰ.设计如图所示装置完成镁和二氧化硫的反应。
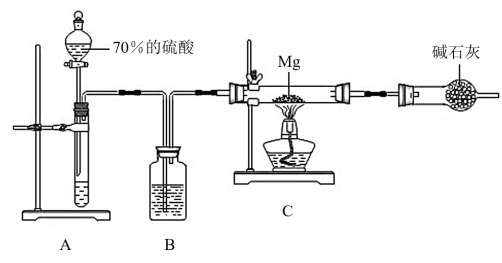
(1)实验室用亚硫酸钠与浓硫酸反应制备SO2,利用的是浓硫酸的___________
a.强氧化性 b.强酸性 c.脱水性 d.腐蚀性
(2)B装置中试剂的名称是_____________ ;E装置的作用是_________________ 。
Ⅱ.探究燃烧的反应产物
(3)反应后取C装置中的固体粉末于烧瓶F中,加入稀硫酸,有气体生成
①产生的气体中含有氢气,则可说明固体中含有______________
②将产生的气体通入硫酸铜溶液,出现黑色沉淀,这一现象的原因是______________ (用离子方程式表示)
(4)取出F装置烧瓶中的混合物,经过滤、干燥得到少量固体粉末,为了探究固体粉末的成分,选择下列装置进行实验:
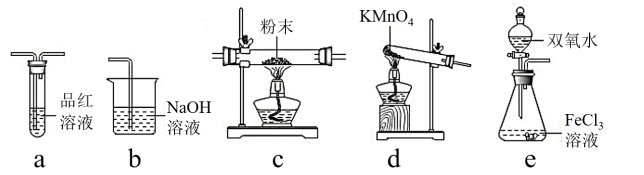
①按气体从左至右,选择所需装置,正确的连接顺序为______________ (字母 )
②能证明固体粉末是硫磺的实验现象是_____________________ 。
(5)经测定,镁在二氧化硫中燃烧生成产物中有硫化镁、硫和氧化镁。如果m(MgO):m(MgS):m(S)=20:7:4,写出镁与SO2在加热条件下反应的化学方程式:________________ 。
Ⅰ.设计如图所示装置完成镁和二氧化硫的反应。

(1)实验室用亚硫酸钠与浓硫酸反应制备SO2,利用的是浓硫酸的
a.强氧化性 b.强酸性 c.脱水性 d.腐蚀性
(2)B装置中试剂的名称是
Ⅱ.探究燃烧的反应产物
(3)反应后取C装置中的固体粉末于烧瓶F中,加入稀硫酸,有气体生成
①产生的气体中含有氢气,则可说明固体中含有
②将产生的气体通入硫酸铜溶液,出现黑色沉淀,这一现象的原因是
(4)取出F装置烧瓶中的混合物,经过滤、干燥得到少量固体粉末,为了探究固体粉末的成分,选择下列装置进行实验:

①按气体从左至右,选择所需装置,正确的连接顺序为
②能证明固体粉末是硫磺的实验现象是
(5)经测定,镁在二氧化硫中燃烧生成产物中有硫化镁、硫和氧化镁。如果m(MgO):m(MgS):m(S)=20:7:4,写出镁与SO2在加热条件下反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)我国酸雨危害十分严重,是世界三大酸雨区之一,且主要为硫酸型酸雨。形成硫酸型酸雨主要是由于空气中___________ 含量超标。形成硫酸型酸雨发生的主要反应的化学方程式为
途径一:_______________________________________ ;
途径二:_______________________________________ 。
(2)某校科技活动小组的同学采集酸雨样品,每隔一段时间测定样品的pH,得到下列数据:
请根据上述材料,回答下列有关问题:
酸雨放置时,pH发生变化的主要原因为___________________________________
(3)你认为减少酸雨产生的途径可采取的措施是_______________
A、用煤作燃料 B、把工厂烟囱造高 C、燃料脱硫 D、开发新能源
途径一:
途径二:
(2)某校科技活动小组的同学采集酸雨样品,每隔一段时间测定样品的pH,得到下列数据:
| 时间 | 开始 | 8 h后 | 16 h 后 | 24 h后 | 32 h后 | 4O h后 | 48 h后 |
| pH | 5.O | 4.8 | 4.5 | 4.3 | 4.2 | 4.O | 4.O |
请根据上述材料,回答下列有关问题:
酸雨放置时,pH发生变化的主要原因为
(3)你认为减少酸雨产生的途径可采取的措施是
A、用煤作燃料 B、把工厂烟囱造高 C、燃料脱硫 D、开发新能源
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成。2014年,习近平在北京考察时指出:应对雾霾污染、改善空气质量的首要任务是控制PM2.5,要从压减燃煤、严格控车、调整产业等方面采取重大举措。
(1)空气质量报告中不涉及的污染物是__________ ;
(2)在催化剂作用下,一氧化氮与一氧化碳反应,生成无毒物质,可解决汽车尾气对环境污染,其化学方程式是_______ ;反应类型是_______ (填“氧化还原反应”或“非氧化还原反应”);汽车燃油改燃气有利于环境保护,汽车最理想的清洁燃料是________ ;
(3)下列关于雾霾天气的说法,错误的是__________;
(1)空气质量报告中不涉及的污染物是__________ ;
| A.SO2 | B.NO2 | C.CO2 | D.可吸入颗粒物 |
(3)下列关于雾霾天气的说法,错误的是__________;
| A.可吸入颗粒物是加重雾霾天气污染的罪魁祸首 |
| B.霾可导致呼吸道疾病、脑血管疾病、鼻腔炎症等 |
| C.雾霾天外出最好戴过滤效果好的口罩 |
| D.发电厂的煤经脱硫处理对减少雾霾无影响 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如下:
(1)放置时,雨水样品酸性_______________ (填“增强”、“减弱”或“不变”)。
酸性变化的原因_________________________________ (用化学方程式表示)。
II.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(2) 写出一氧化碳与一氧化氮反应的化学方程式:__________________________ 。
(3) 在“催化转化器”转化后的气体中有CO2、SO2,下列不能鉴别这两种气体的是( )
A.KMnO4溶液 B.石灰水 C.BaCl2溶液 D.品红溶液
(4) 有效减少城市污染的方法可以有____________
A. 开发氢能源 B. 使用电动车 C. 植树造林 D. 戴上呼吸面具
时间 | 开始 | 8小时 | 16小时 | 24小时 | 32小时 | 40小时 | 48小时 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
酸性变化的原因
II.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(2) 写出一氧化碳与一氧化氮反应的化学方程式:
(3) 在“催化转化器”转化后的气体中有CO2、SO2,下列不能鉴别这两种气体的是
A.KMnO4溶液 B.石灰水 C.BaCl2溶液 D.品红溶液
(4) 有效减少城市污染的方法可以有
A. 开发氢能源 B. 使用电动车 C. 植树造林 D. 戴上呼吸面具
您最近一年使用:0次



