已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为_______ 。(选序号)写出4g H2燃烧的热化学方程式_______ ;
(2)24g C完全燃烧,放出的热量为_______ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。
(1)C燃烧热的热化学方程式为
(2)24g C完全燃烧,放出的热量为
(3)液态水的稳定性
更新时间:2022-10-01 15:17:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列反应的热化学方程式。
(1)沼气是一种能源,它的主要成分是CH4,常温下,0.5 mol CH4完全燃烧生成CO2(g)和液态水时,放出445 kJ热量,则热化学方程式为_______ 。
(2)已知H2S(g)完全燃烧生成SO2(g)和H2O(l),H2S的燃烧热为a kJ·mol-1,写出H2S的燃烧热的热化学方程式_______ 。
(3)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH1,相关物质的燃烧热数据如下表所示:
则ΔH1=_______ kJ·mol-1。
(4)已知: ①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
试写出HF电离的热化学方程式_______ 。
(5)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
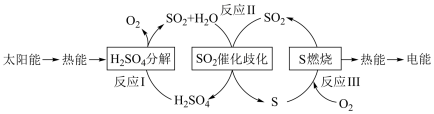
反应 I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应 III:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应II的热化学方程式:_______ 。
(1)沼气是一种能源,它的主要成分是CH4,常温下,0.5 mol CH4完全燃烧生成CO2(g)和液态水时,放出445 kJ热量,则热化学方程式为
(2)已知H2S(g)完全燃烧生成SO2(g)和H2O(l),H2S的燃烧热为a kJ·mol-1,写出H2S的燃烧热的热化学方程式
(3)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH1,相关物质的燃烧热数据如下表所示:
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热ΔH/ ( kJ·mol-1) | -1 560 | -1 411 | -286 |
(4)已知: ①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
试写出HF电离的热化学方程式
(5)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应 I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应 III:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应II的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
Ⅰ.已知:
 ,现用下图所示装置测定中和热。
,现用下图所示装置测定中和热。
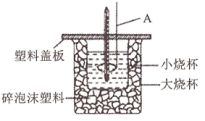
回答下列问题:
(1)碎泡沫塑料的作用是___________ ;若将A换为“铜丝搅拌棒”测得的 将
将___________ (填“偏大”、“偏小”或“不变”)。
(2)若用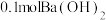 配制成稀溶液,与足量的稀硝酸反应,放出的热量为
配制成稀溶液,与足量的稀硝酸反应,放出的热量为___________ kJ。
Ⅱ.2021年5月29日天舟二号货运飞船成功发射,为中国空间站进一步开展在轨建造奠定了坚实基础,该飞船由长征七号遥三运载火箭搭载。长征七号遥三运载火箭使用煤油为燃料
(3)煤油的主要成分为 ,已知
,已知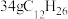 完全燃烧生成气态水时放出1386.2kJ热量;
完全燃烧生成气态水时放出1386.2kJ热量;
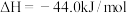 。则表示煤油燃烧热的热化学方程式为
。则表示煤油燃烧热的热化学方程式为___________ 。
(4)前期的火箭曾用液态肼(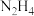 )与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为
)与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为___________ 。
Ⅲ.将氧化铁还原为铁的技术在人类文明进步中占据十分重要的地位。高炉炼铁中发生的部分反应为:
①
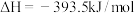
②

(5)已知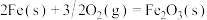
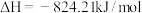 。则高炉内
。则高炉内 被CO还原为Fe的热化学方程式为
被CO还原为Fe的热化学方程式为___________ 。
(6)碳(s)在氧气不足的情况下燃烧,会生成CO,但同时也有部分生成 ,因此无法通过实验直接测得反应:
,因此无法通过实验直接测得反应: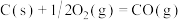 的
的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有___________ 。若根据上述信息可计算出该反应的
___________ kJ/mol。
Ⅰ.已知:

 ,现用下图所示装置测定中和热。
,现用下图所示装置测定中和热。
回答下列问题:
(1)碎泡沫塑料的作用是
 将
将(2)若用
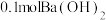 配制成稀溶液,与足量的稀硝酸反应,放出的热量为
配制成稀溶液,与足量的稀硝酸反应,放出的热量为Ⅱ.2021年5月29日天舟二号货运飞船成功发射,为中国空间站进一步开展在轨建造奠定了坚实基础,该飞船由长征七号遥三运载火箭搭载。长征七号遥三运载火箭使用煤油为燃料
(3)煤油的主要成分为
 ,已知
,已知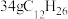 完全燃烧生成气态水时放出1386.2kJ热量;
完全燃烧生成气态水时放出1386.2kJ热量;
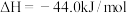 。则表示煤油燃烧热的热化学方程式为
。则表示煤油燃烧热的热化学方程式为(4)前期的火箭曾用液态肼(
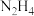 )与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为
)与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为Ⅲ.将氧化铁还原为铁的技术在人类文明进步中占据十分重要的地位。高炉炼铁中发生的部分反应为:
①

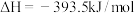
②


(5)已知
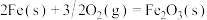
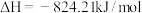 。则高炉内
。则高炉内 被CO还原为Fe的热化学方程式为
被CO还原为Fe的热化学方程式为(6)碳(s)在氧气不足的情况下燃烧,会生成CO,但同时也有部分生成
 ,因此无法通过实验直接测得反应:
,因此无法通过实验直接测得反应: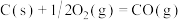 的
的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知H2(g)+ O2(g)=H2O(l)ΔH=-285.8kJ•mol-1。蒸发1mol液态水需要吸收的能量为44kJ,其它相关数据如下表:
O2(g)=H2O(l)ΔH=-285.8kJ•mol-1。蒸发1mol液态水需要吸收的能量为44kJ,其它相关数据如下表:
则表中x的大小为______________ ;
(2)已知7.8g乙炔气体充分燃烧时生成CO2和液态水,放出390kJ的热量,则表示乙炔燃烧热的热化学方程式为______________ 。
 O2(g)=H2O(l)ΔH=-285.8kJ•mol-1。蒸发1mol液态水需要吸收的能量为44kJ,其它相关数据如下表:
O2(g)=H2O(l)ΔH=-285.8kJ•mol-1。蒸发1mol液态水需要吸收的能量为44kJ,其它相关数据如下表:| H2(g) | O2(g) | H2O(g) | |
| 1mol分子断裂化学键时需要吸收的能量/kJ | 436 | x | 926 |
则表中x的大小为
(2)已知7.8g乙炔气体充分燃烧时生成CO2和液态水,放出390kJ的热量,则表示乙炔燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化。
(1)已知几种化学键的键能如表所示:
则反应Cl2(g)+ 3F2(g) 2ClF3(g) 的△H=
2ClF3(g) 的△H=_____________ kJ·mol—1 。
(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。
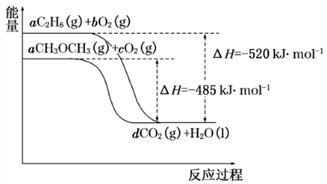
请回答下列问题:
①乙烷的燃烧热ΔH=____ kJ·mol-1。
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量__ (填“多”或“少”)。
③根据题图写出二甲醚完全燃烧时的热化学方程式_____________ 。
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量____ (填“相等”或“不相等”,忽略实验本身误差,下同),所求中和热_____ (填“相等”或“不相等”,)。
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会___ (填“偏大”“偏小”或“无影响”)。
(1)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)
 2ClF3(g) 的△H=
2ClF3(g) 的△H=(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
①乙烷的燃烧热ΔH=
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量
③根据题图写出二甲醚完全燃烧时的热化学方程式
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学在生产生活中有广泛的应用,请用所学的知识填空:
(1)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解液为 KOH 溶液,则氢氧燃料电池的负极反应式为______ 。
(2)泡沫灭火器内盛有 Al2(SO4)3、NaHCO3溶液,写出其反应的离子方程式______ 。
(3)金属铍(Be)是高效率的火箭燃料,燃烧时放出巨大的能量,已知 1 g 铍完全燃烧放出的热量为 62. 70 kJ,则表示铍的燃烧热的热化学方程式为: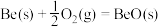 ∆H=
∆H=______ kJ·mol-1.
(4)FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的最后一步是在常温下调节溶液 pH=5,此时 c(Fe3+)=______ mol·L-1(已知:Ksp[Fe(OH)3]= 4.0×10-38)。
(1)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解液为 KOH 溶液,则氢氧燃料电池的负极反应式为
(2)泡沫灭火器内盛有 Al2(SO4)3、NaHCO3溶液,写出其反应的离子方程式
(3)金属铍(Be)是高效率的火箭燃料,燃烧时放出巨大的能量,已知 1 g 铍完全燃烧放出的热量为 62. 70 kJ,则表示铍的燃烧热的热化学方程式为:
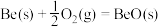 ∆H=
∆H=(4)FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的最后一步是在常温下调节溶液 pH=5,此时 c(Fe3+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求完成下列问题:
(1)在1.01×105 Pa时,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示氢气燃烧热的热化学方程式为___________ 。
(2)在1.01×105 Pa时,16 g S在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则表示S燃烧热的热化学方程式为____________ 。
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水。已知室温下1 g甲硅烷自燃放出44.6 kJ热量,其热化学方程式为______ 。
(1)在1.01×105 Pa时,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示氢气燃烧热的热化学方程式为
(2)在1.01×105 Pa时,16 g S在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则表示S燃烧热的热化学方程式为
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水。已知室温下1 g甲硅烷自燃放出44.6 kJ热量,其热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)在高温、高压、催化剂作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量,则___________ (选填“石墨”或“金刚石”)更稳定。
(2)用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:
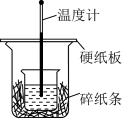
①从实验装置上看,图中缺少的一种实验仪器名称是___________ 。
②使用如图所示装置测得中和热
___________ (填“偏大、偏小、无影响”)。
(3)在25℃、101 kPa下,1 g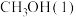 完全燃烧生成
完全燃烧生成 和液态水时放热22.68 kJ。写出表示
和液态水时放热22.68 kJ。写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式___________ 。
(4)用 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:
①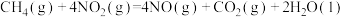
 kJ·mol-1
kJ·mol-1
②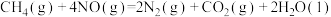
 kJ·mol-1
kJ·mol-1
据此,写出 将
将 还原为
还原为 的热化学方程式:
的热化学方程式:___________ 。
(1)在高温、高压、催化剂作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量,则
(2)用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:

①从实验装置上看,图中缺少的一种实验仪器名称是
②使用如图所示装置测得中和热

(3)在25℃、101 kPa下,1 g
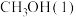 完全燃烧生成
完全燃烧生成 和液态水时放热22.68 kJ。写出表示
和液态水时放热22.68 kJ。写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(4)用
 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:①
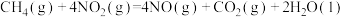
 kJ·mol-1
kJ·mol-1②
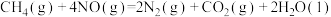
 kJ·mol-1
kJ·mol-1据此,写出
 将
将 还原为
还原为 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应的过程,既有物质的转化过程,也是化学能与热等其他形式能量的转化过程。
Ⅰ.已知某反应 过程中的能量变化如图所示,回答问题。
过程中的能量变化如图所示,回答问题。
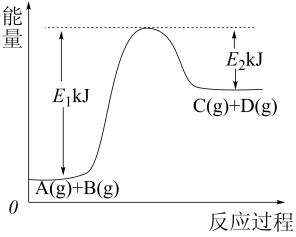
(1)该反应是___________ (填“吸热”或“放热”)反应,该反应的 =
=___________ kJ/mol(用含E1、E2的代数式表示)。
(2)1mol气体A和1mol气体B具有的总能量___________ (填“>”“<”或“=”)1mol气体C和1mol气体D具有的总能量。
Ⅱ.发射卫星时可用肼(N2H4)作为燃料,用二氧化氮作为氧化剂,两者反应生成氮气和气态水。
已知: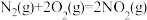
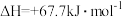

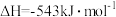
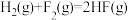
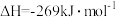
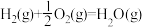
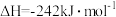
(3)N2H4 (g)和NO2(g)反应的热化学方程式为___________ ;
(4)有人认为若用氟单质代替二氧化氮作为氧化剂,则反应释放能量更多,N2H4 (g)和F2(g)反应的热化学方程式为___________ 。
Ⅲ.有机物通常能发生燃烧,对应的反应往往都有重要用途。
(5)在25℃、101k Pa条件下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程为___________ 。
(6)用NA表示阿伏加德罗常数的值,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。则该反应的热化学方程式为___________ 。
Ⅰ.已知某反应
 过程中的能量变化如图所示,回答问题。
过程中的能量变化如图所示,回答问题。
(1)该反应是
 =
=(2)1mol气体A和1mol气体B具有的总能量
Ⅱ.发射卫星时可用肼(N2H4)作为燃料,用二氧化氮作为氧化剂,两者反应生成氮气和气态水。
已知:
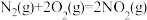
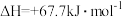

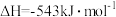
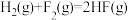
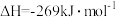
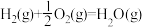
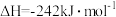
(3)N2H4 (g)和NO2(g)反应的热化学方程式为
(4)有人认为若用氟单质代替二氧化氮作为氧化剂,则反应释放能量更多,N2H4 (g)和F2(g)反应的热化学方程式为
Ⅲ.有机物通常能发生燃烧,对应的反应往往都有重要用途。
(5)在25℃、101k Pa条件下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程为
(6)用NA表示阿伏加德罗常数的值,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。则该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)甲醇(CH3OH,常温下为液态)是一种常用的能源物质。
①甲醇的热值为23 kJ · g-1。写出甲醇燃烧热的热化学方程式:_________________________ 。
②以甲醇为原料设计成燃料电池:若以熔融Na2CO3作为电解质,一极充入甲醇,另一极充入空气和CO2气体。回答下列问题:
充入空气和CO2气体的电极为__________ 极,该电池的总反应式:_____________________ ,充入甲醇电极的反应式:______________________________________ 。
③若用该燃料电池为电源,用石墨电极电解250 mL CuSO4溶液。则与充入空气和CO2气体的电极相连的是电解池的_______ 极;与甲醇电极相连的电极反应式为______________________ ;若燃料电池中消耗0.05 mol甲醇,电解池中共产生标准状况下气体2.24 L, 则原 CuSO4溶液浓度为________ mol·L-1(假设电解前后溶液体积不变)。
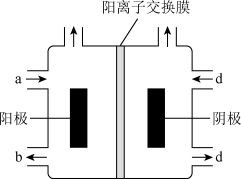
(2)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。写出该电解的总反应_________________________________ 。
①甲醇的热值为23 kJ · g-1。写出甲醇燃烧热的热化学方程式:
②以甲醇为原料设计成燃料电池:若以熔融Na2CO3作为电解质,一极充入甲醇,另一极充入空气和CO2气体。回答下列问题:
充入空气和CO2气体的电极为
③若用该燃料电池为电源,用石墨电极电解250 mL CuSO4溶液。则与充入空气和CO2气体的电极相连的是电解池的
(2)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。写出该电解的总反应

您最近一年使用:0次



