按要求完成下列问题:
(1)在1.01×105 Pa时,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示氢气燃烧热的热化学方程式为___________ 。
(2)在1.01×105 Pa时,16 g S在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则表示S燃烧热的热化学方程式为____________ 。
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水。已知室温下1 g甲硅烷自燃放出44.6 kJ热量,其热化学方程式为______ 。
(1)在1.01×105 Pa时,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示氢气燃烧热的热化学方程式为
(2)在1.01×105 Pa时,16 g S在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则表示S燃烧热的热化学方程式为
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水。已知室温下1 g甲硅烷自燃放出44.6 kJ热量,其热化学方程式为
更新时间:2019-12-23 11:43:28
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) ΔH=-285kJ·mol-1
O2(g)=H2O(l) ΔH=-285kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241kJ·mol-1
O2(g)=H2O(g) ΔH=-241kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110kJ·mol-1
O2(g)=CO(g) ΔH=-110kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为___ kJ·mol-1;C的燃烧热为___ kJ·mol-1。
(2)燃烧10gH2生成液态水,放出的热量为___ kJ。
(3)写出表示CO燃烧热的热化学方程式___ 。
①H2(g)+
 O2(g)=H2O(l) ΔH=-285kJ·mol-1
O2(g)=H2O(l) ΔH=-285kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241kJ·mol-1
O2(g)=H2O(g) ΔH=-241kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110kJ·mol-1
O2(g)=CO(g) ΔH=-110kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为
(2)燃烧10gH2生成液态水,放出的热量为
(3)写出表示CO燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知下列热化学方程式:①H2(g)+ O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+
O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+ O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+
O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+  O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
(1)上述反应中属于放热反应的是_______ 。(填序号)
(2)H2的燃烧热为___ ;C的燃烧热为____ 。
(3)燃烧4g H2生成液态水,放出的热量为_______ 。
(4)根据盖斯定律可知CO的燃烧热为_____ ;其热化学方程式为_____ 。
(5)比较下列各组热化学方程式中△H的大小:
①C(s)+O2(g)=CO2(g)△H1 C(s)+ O2(g)=CO(g) △H2 △H1
O2(g)=CO(g) △H2 △H1 ____ △H2
②S(s)+O2(g)=SO2(g)△H3 S(g)+O2(g)=SO2(g) △H4 △H3__ △H4
 O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+
O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+ O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+
O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+  O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
O2(g)=CO(g)ΔH=―110.4 kJ/mol ④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧4g H2生成液态水,放出的热量为
(4)根据盖斯定律可知CO的燃烧热为
(5)比较下列各组热化学方程式中△H的大小:
①C(s)+O2(g)=CO2(g)△H1 C(s)+
 O2(g)=CO(g) △H2 △H1
O2(g)=CO(g) △H2 △H1 ②S(s)+O2(g)=SO2(g)△H3 S(g)+O2(g)=SO2(g) △H4 △H3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。
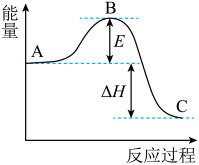
(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示____ 、____ ,E的大小对该反应的反应热____ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点____ (填“变大”、“变小”或“不变”)。
(2)图中ΔH=____ kJ·mol-1。
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式____ 。
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=____ 。

(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示
(2)图中ΔH=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=
您最近一年使用:0次
【推荐1】已知25℃、101kpa时,一些物质的燃烧热为:
请回答下列问题:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:______________________ 。
(2)根据盖斯定律完成下列反应的热化学方程式:CO(g)+2H2(g)=CH3OH(l);△H=_________________ 。
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:___________ 。
A.1∶1 B.1∶3 C.1∶4 D.2∶3
| 化学式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 | -890.3 |
请回答下列问题:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:
(2)根据盖斯定律完成下列反应的热化学方程式:CO(g)+2H2(g)=CH3OH(l);△H=
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:
A.1∶1 B.1∶3 C.1∶4 D.2∶3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
由此计算ΔH1=______ kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=_______ kJ·mol-1。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1 275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式_________________ 。
(3)已知常温时红磷比白磷稳定,已知:
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
比较反应中ΔH的大小:ΔH1_______ ΔH2(填“>”、“<”或“=”)。
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)===H2O(l)ΔH=﹣57.3 kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量_____ 57.3 kJ(填“>”、“<”或“=”)。
①CO(g)+2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1 076 | 465 | 413 |
由此计算ΔH1=
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1 275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)已知常温时红磷比白磷稳定,已知:
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
比较反应中ΔH的大小:ΔH1
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)===H2O(l)ΔH=﹣57.3 kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)适量 在1mol
在1mol 中完全燃烧,生成2mol
中完全燃烧,生成2mol ,放出571.6kJ的热量。请写出表示
,放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式______ 。
(2)电解稀的氢氧化钠溶液:阳极反应式为______ 。
(3)若向氨水中加入稀硫酸至溶液的 ,此时溶液中
,此时溶液中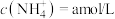 ,则
,则 =
=______ 。
(4)写出基态As原子的简化电子排布式和价层电子的轨道表示式:______ 。
(1)适量
 在1mol
在1mol 中完全燃烧,生成2mol
中完全燃烧,生成2mol ,放出571.6kJ的热量。请写出表示
,放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(2)电解稀的氢氧化钠溶液:阳极反应式为
(3)若向氨水中加入稀硫酸至溶液的
 ,此时溶液中
,此时溶液中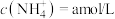 ,则
,则 =
=(4)写出基态As原子的简化电子排布式和价层电子的轨道表示式:
您最近一年使用:0次



