回答下列问题
(1)适量 在1mol
在1mol 中完全燃烧,生成2mol
中完全燃烧,生成2mol ,放出571.6kJ的热量。请写出表示
,放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式______ 。
(2)电解稀的氢氧化钠溶液:阳极反应式为______ 。
(3)若向氨水中加入稀硫酸至溶液的 ,此时溶液中
,此时溶液中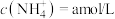 ,则
,则 =
=______ 。
(4)写出基态As原子的简化电子排布式和价层电子的轨道表示式:______ 。
(1)适量
 在1mol
在1mol 中完全燃烧,生成2mol
中完全燃烧,生成2mol ,放出571.6kJ的热量。请写出表示
,放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(2)电解稀的氢氧化钠溶液:阳极反应式为
(3)若向氨水中加入稀硫酸至溶液的
 ,此时溶液中
,此时溶液中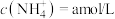 ,则
,则 =
=(4)写出基态As原子的简化电子排布式和价层电子的轨道表示式:
更新时间:2023-01-10 10:23:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为___________ 。(选数字)
(2)燃烧1gH2生成液态水,放出的热量为_________________ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。。
(1)H2燃烧热的热化学方程式为
(2)燃烧1gH2生成液态水,放出的热量为
(3)液态水的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求书写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_____________________________________________________________________ 。
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式____________________________________________________________________ 。
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g) =CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+1/2O2(g) =H2O(l) ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式______________________________________________________________________ 。
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g) =CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+1/2O2(g) =H2O(l) ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知某反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答问题。
C(g)+D(g)过程中的能量变化如图所示,回答问题。

该反应是____ (填“吸热”或“放热”)反应,该反应的ΔH=_____ kJ· mol-1(用含E1、E2的代数式表示)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l) =H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式___________________________ 。
(3)已知:H2(g)+Cl2(g)==2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为______ kJ。
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是_________________ 。
 C(g)+D(g)过程中的能量变化如图所示,回答问题。
C(g)+D(g)过程中的能量变化如图所示,回答问题。
该反应是
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l) =H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)已知:H2(g)+Cl2(g)==2HCl(g) ΔH=-185 kJ/mol,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列五种溶液:盐酸、NH3·H2O、NH4HSO4、NaOH、CH3COOH。回答下列问题:
(1)将1 L pH=2的HCl溶液分别与0.01 mol· L-1的NH3· H2O溶液x L、0.01 mol· L-1的NaOH溶液y L充分反应至中性,x、y大小关系为: y_____ x(填“>”“<”或“=”)。
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是_____ (填写序号)。
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
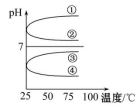
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的______ 曲线(填写序号)。
(4)室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加0.01 mol·L-1 NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+)______ 2c(SO42- )(填“>”“=”或“<”);用NH4HSO4与氢氧化钡溶液制取硫酸钡,若溶液中SO42- 完全沉淀,则反应后溶液的pH______ 7(填“>”“=”或“<”),该反应的离子方程式为_______________ 。
(5)25 ℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是________________ (用离子方程式表示)。向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将_______ (填“正向”“不”或“逆向”)移动。
(1)将1 L pH=2的HCl溶液分别与0.01 mol· L-1的NH3· H2O溶液x L、0.01 mol· L-1的NaOH溶液y L充分反应至中性,x、y大小关系为: y
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的

(4)室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加0.01 mol·L-1 NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+)
(5)25 ℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】溶液中的反应大多都是离子反应,请按要求回答下列问题:
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是___ (填字母标号)。
(2)泡沫灭火器的反应原理是盐类水解,请写出其离子方程式:___ 。
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是___ 。
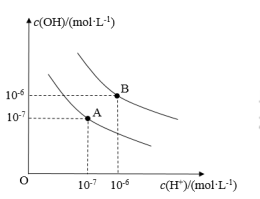
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为___ 。
(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是___ (用a、b、c表示,下同)。
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为___ 。
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是
| A.甲学生:在醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是吸热的 |
| B.乙学生:将硝酸铵晶体溶于水,水温下降,说明硝酸铵水解是吸热的 |
| C.丙学生:在盐酸中加入同温度的氨水,混合液温度下降,说明盐类水解是吸热的 |
| D.丁学生:在醋酸钠溶液中加入醋酸钠晶体,溶液温度下降,说明盐类水解是吸热的 |
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为

(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在常温下,下列五种溶液:
①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4 ③0.1 mol·L-1 NH4HSO4 ④1 L含0.1 mol NH3·H2O和0.1mol NH4Cl混合液 ⑤0.1 mol·L-1 NH3·H2O
请根据要求填写下列空白:
(1)①、③、④、⑤pH由小到大的顺序为___________ ;(填序号,下同)
(2)①、②、③、⑤中c(NH )由小到大的顺序为
)由小到大的顺序为___________ 。
(3)写出④中c(NH3) +c(NH3•H2O) +c(NH )=
)=___________ 。
(4)常温下,测得溶液②的pH=7,此溶液中水的电离程度___________ 该温度下纯水的电离程度(填“>”、“<”或“=”)
(5)取适量溶液⑤,加入少量氯化铵固体,此时溶液中的 值
值___________ (填“增大”、“减小”或“不变”)
(6)常温下,将⑤与a mol/L盐酸等体积混合(不考虑溶液体的变化),反应后溶液恰好呈中性,用a表示NH3·H2O的电离平衡常数为___________ 。
①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4 ③0.1 mol·L-1 NH4HSO4 ④1 L含0.1 mol NH3·H2O和0.1mol NH4Cl混合液 ⑤0.1 mol·L-1 NH3·H2O
请根据要求填写下列空白:
(1)①、③、④、⑤pH由小到大的顺序为
(2)①、②、③、⑤中c(NH
 )由小到大的顺序为
)由小到大的顺序为(3)写出④中c(NH3) +c(NH3•H2O) +c(NH
 )=
)=(4)常温下,测得溶液②的pH=7,此溶液中水的电离程度
(5)取适量溶液⑤,加入少量氯化铵固体,此时溶液中的
 值
值(6)常温下,将⑤与a mol/L盐酸等体积混合(不考虑溶液体的变化),反应后溶液恰好呈中性,用a表示NH3·H2O的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
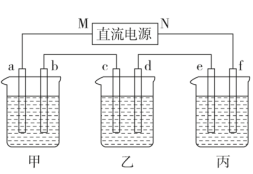
接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图。据此回答下列问题:
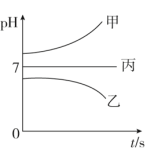
(1)M为电源的___________ (填“正”或“负”)极,电极b上发生的电极反应为___________ 。
(2)电极e上生成的气体在标准状况下的体积为___________ 。
(3)写出乙烧杯中的电解反应:___________ 。
(4)若电解过程中,乙烧杯中的B溶液中的金属离子全部析出,此时电解仍继续进行,原因___________ 。
(5)若直流电源换为甲烷氧气燃料(电解质溶液是KOH溶液)电池,那么甲烷燃料电池负极的电极反应为___________ 。
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO 、OH- 、OH- |
在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。

接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图。据此回答下列问题:

(1)M为电源的
(2)电极e上生成的气体在标准状况下的体积为
(3)写出乙烧杯中的电解反应:
(4)若电解过程中,乙烧杯中的B溶液中的金属离子全部析出,此时电解仍继续进行,原因
(5)若直流电源换为甲烷氧气燃料(电解质溶液是KOH溶液)电池,那么甲烷燃料电池负极的电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硼酸溶于水、酒精、甘油、醚类及香精油中,水溶液呈弱酸性。大量用于玻璃(光学玻璃、耐酸玻璃、耐热玻璃、绝缘材料用玻璃纤维)工业,可以改善玻璃制品的耐热、透明性能,提高机械强度,缩短熔融时间。H3BO3可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图。

(1)请书写M室发生的电极反应式:__________________ 。
(2)N室中a%和b%的大小关系为:___________ 。
(3)b膜为___________ 离子交换膜。
(4)理论上每生成1mol产品,阴极室可生成标准状况下气体的体积为___________ 。

(1)请书写M室发生的电极反应式:
(2)N室中a%和b%的大小关系为:
(3)b膜为
(4)理论上每生成1mol产品,阴极室可生成标准状况下气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】CuSO4溶液是一种较重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究。
i. 下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。

①该原电池的正极为____ ,其外电路中的电子是从____ 极(填“Zn”或“Cu”)流出。
②电解质溶液乙是______ 溶液,Zn极的电极反应式是_______ 。
③如果盐桥中的成分是K2SO4溶液,则盐桥中向左侧烧杯中移动的离子主要是_____ 。
ii. 下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。
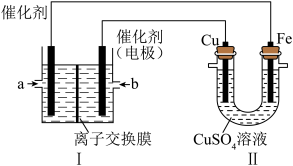
①同学想在Ⅱ中实现铁上镀铜,则Cu作____ 极,电极反应式为______ ,当线路中有0.1mol电子通过时,阴极增重_____ g。Ⅰ中消耗氧气体积是_____ L(标况下)。
②a处通入的是____ (填“CH4”或“O2”),b处电极上发生的电极反应式是___ 。Ⅰ中的总反应方程式为___ 。
③该同学若将Ⅱ中的两个电极都换成铂电极,当线路中有0.1mol电子通过时,测得溶液pH=______ (100mL的CuSO4溶液),则Ⅱ中的总反应方程式为 _______ 。
i. 下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。

①该原电池的正极为
②电解质溶液乙是
③如果盐桥中的成分是K2SO4溶液,则盐桥中向左侧烧杯中移动的离子主要是
ii. 下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。

①同学想在Ⅱ中实现铁上镀铜,则Cu作
②a处通入的是
③该同学若将Ⅱ中的两个电极都换成铂电极,当线路中有0.1mol电子通过时,测得溶液pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请按要求回答以下问题:
(1)基态F原子的核外电子轨道表达式为___________ 。
(2)25Mn原子核外电子排布式为___________ 。
(3)菱锌矿ZnCO3中基态30Zn原子价电子排布式___________ ,基态C原子的核外电子占据的最高能级电子云轮廓为___________ ,基态O原子有___________ 种运动状态不同的电子。
(4)常温下,0.1mol·L-1NaHCO3溶液中,c( )<c(H2CO3),则溶液显
)<c(H2CO3),则溶液显___________ 性。
(1)基态F原子的核外电子轨道表达式为
(2)25Mn原子核外电子排布式为
(3)菱锌矿ZnCO3中基态30Zn原子价电子排布式
(4)常温下,0.1mol·L-1NaHCO3溶液中,c(
 )<c(H2CO3),则溶液显
)<c(H2CO3),则溶液显
您最近一年使用:0次
【推荐2】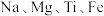 等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2) 原子的核外电子,有
原子的核外电子,有___________ 种空间运动状态。
(3) 元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
(4) 原子位于元素周期表中的
原子位于元素周期表中的___________ 区,其价电子排布式为___________ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为___________ 。
(5) 与
与 的离子半径大小关系为
的离子半径大小关系为
___________  (填“大于”或“小于)。
(填“大于”或“小于)。
(6)下列各组多电子原子的能级能量比较不正确的是___________。
① ②
② ③
③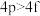 ④
④
(7)很多金属及其化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识解释产生此现象的原因是___________ 。
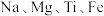 等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)
 原子的核外电子,有
原子的核外电子,有(3)
 元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。A.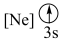 | B.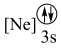 | C.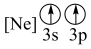 | D.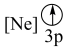 |
(4)
 原子位于元素周期表中的
原子位于元素周期表中的 同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为(5)
 与
与 的离子半径大小关系为
的离子半径大小关系为
 (填“大于”或“小于)。
(填“大于”或“小于)。(6)下列各组多电子原子的能级能量比较不正确的是___________。
①
 ②
② ③
③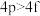 ④
④
| A.①④ | B.③④ | C.①③ | D.②③ |
(7)很多金属及其化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识解释产生此现象的原因是
您最近一年使用:0次
【推荐3】依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
(2)基态V原子中具有_______ 种不同能量的电子,具有_______ 种不同空间运动状态的电子,具有_______ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为_______ ,基态Se原子的价电子轨道表示式为_______ ,基态Mn2+的价电子排布式为_______ 。
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为_______ kJ·mol-1,O=O键键能为_______ kJ·mol-1。
(1)下列有关说法错误的是_______。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为
您最近一年使用:0次



