回答下列问题
(1)在高温、高压、催化剂作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量,则___________ (选填“石墨”或“金刚石”)更稳定。
(2)用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:
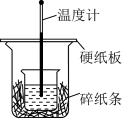
①从实验装置上看,图中缺少的一种实验仪器名称是___________ 。
②使用如图所示装置测得中和热
___________ (填“偏大、偏小、无影响”)。
(3)在25℃、101 kPa下,1 g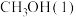 完全燃烧生成
完全燃烧生成 和液态水时放热22.68 kJ。写出表示
和液态水时放热22.68 kJ。写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式___________ 。
(4)用 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:
①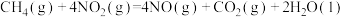
 kJ·mol-1
kJ·mol-1
②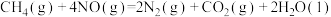
 kJ·mol-1
kJ·mol-1
据此,写出 将
将 还原为
还原为 的热化学方程式:
的热化学方程式:___________ 。
(1)在高温、高压、催化剂作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量,则
(2)用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:

①从实验装置上看,图中缺少的一种实验仪器名称是
②使用如图所示装置测得中和热

(3)在25℃、101 kPa下,1 g
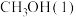 完全燃烧生成
完全燃烧生成 和液态水时放热22.68 kJ。写出表示
和液态水时放热22.68 kJ。写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(4)用
 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:①
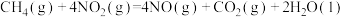
 kJ·mol-1
kJ·mol-1②
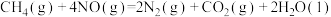
 kJ·mol-1
kJ·mol-1据此,写出
 将
将 还原为
还原为 的热化学方程式:
的热化学方程式:
更新时间:2023-10-09 16:04:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组要完成中和反应反应热的测定实验。
(1)实验桌上备有量热计、胶头滴管、玻璃搅拌器、 盐酸、
盐酸、 氢氧化钠溶液,实验尚缺少的玻璃用品是
氢氧化钠溶液,实验尚缺少的玻璃用品是_______ 。
(2)实验中能否用环形铜丝搅拌器代替玻璃搅拌器_______ (填“能”或“否”),其原因是_______ 。
(3)他们记录的实验数据如下:
已知: ,反应后溶液的比热容c为
,反应后溶液的比热容c为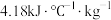 ,各物质的密度均为
,各物质的密度均为 。
。
①计算完成上表(保留1位小数)_______ 。
②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:_______ 。
(4)若用氢氧化钾代替氢氧化钠,对测定结果_______ (填“有”或“无”,下同)影响;若用醋酸代替盐酸做实验,对测定结果_______ 影响。
(1)实验桌上备有量热计、胶头滴管、玻璃搅拌器、
 盐酸、
盐酸、 氢氧化钠溶液,实验尚缺少的玻璃用品是
氢氧化钠溶液,实验尚缺少的玻璃用品是(2)实验中能否用环形铜丝搅拌器代替玻璃搅拌器
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 生成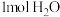 放出的热量 放出的热量 | |||
 |  | ||||
| a |  溶液 溶液 | 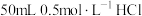 溶液 溶液 | 20℃ | 23.3℃ | _______kJ |
| b |  溶液 溶液 | 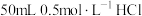 溶液 溶液 | 20℃ | 23.5℃ | |
 ,反应后溶液的比热容c为
,反应后溶液的比热容c为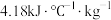 ,各物质的密度均为
,各物质的密度均为 。
。①计算完成上表(保留1位小数)
②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:
(4)若用氢氧化钾代替氢氧化钠,对测定结果
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)已知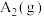 和
和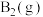 反应生成1mol
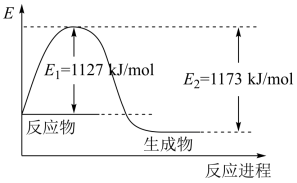
反应生成1mol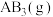 过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为_______ kJ/mol。
(2)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。
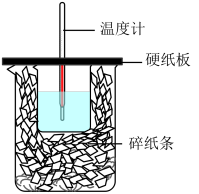
①从实验装置上看,图中缺少的一种玻璃仪器是_______ 。烧杯间填满碎纸条的作用是_______ 。若大烧杯上不盖硬纸板,求得的中和反应反应热
_______ (填“偏大”“偏小”或“无影响”)。
②甲同学用50mL 盐酸与50mL
盐酸与50mL NaOH溶液进行中和反应,通过计算得到
NaOH溶液进行中和反应,通过计算得到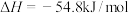 ,该结果与
,该结果与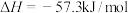 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是_______ (填字母)。
A.用温度计测量盐酸起始温度后直接测量NaOH溶液的温度
B.一次性把NaOH溶液倒入盛有盐酸的小烧杯中
C.实验装置保温、隔热效果差
③若改用60mL 盐酸与60mL
盐酸与60mL NaOH溶液进行反应,与②中实验相比,所放出的热量
NaOH溶液进行反应,与②中实验相比,所放出的热量_______ (填“相等”或“不相等”);若用50mL
 溶液代替盐酸进行②中实验,测得反应前后温度的变化值
溶液代替盐酸进行②中实验,测得反应前后温度的变化值_______ (填“偏大”“偏小”或“不受影响”)。
(1)已知
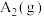 和
和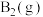 反应生成1mol
反应生成1mol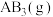 过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
| 化学键 |  | B—B |
| 键能(kJ/mol) | 946 | 436 |

①从实验装置上看,图中缺少的一种玻璃仪器是

②甲同学用50mL
 盐酸与50mL
盐酸与50mL NaOH溶液进行中和反应,通过计算得到
NaOH溶液进行中和反应,通过计算得到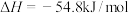 ,该结果与
,该结果与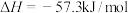 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是A.用温度计测量盐酸起始温度后直接测量NaOH溶液的温度
B.一次性把NaOH溶液倒入盛有盐酸的小烧杯中
C.实验装置保温、隔热效果差
③若改用60mL
 盐酸与60mL
盐酸与60mL NaOH溶液进行反应,与②中实验相比,所放出的热量
NaOH溶液进行反应,与②中实验相比,所放出的热量
 溶液代替盐酸进行②中实验,测得反应前后温度的变化值
溶液代替盐酸进行②中实验,测得反应前后温度的变化值
您最近一年使用:0次
【推荐3】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_______(填字母)。
(2)向 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、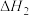 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为_______ 。
(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。
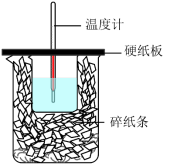
从实验装置上看,图中缺少的一种玻璃仪器是_______ 。若大烧杯上不盖硬纸板,求得的中和反应反应热
_______ (填“偏大”“偏小”或“无影响”)。
(4)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得:2H2(g)+O2(g)=2H2O(g) ΔH=_______ 。
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应ΔH=_______ 。
(5)硝酸厂的尾气直接排放将污染空气,日前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为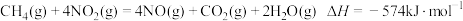

则甲烷直接将 还原为
还原为 的热化学方程式为
的热化学方程式为_______ 。
(1)下列反应中,属于放热反应的是_______(填字母)。
| A.碳与水蒸气反应 | B.铝和氧化铁反应 |
| C.CaCO3受热分解 | D.锌与盐酸反应 |
 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、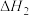 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。

从实验装置上看,图中缺少的一种玻璃仪器是

(4)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 | H-H | O=O | O-H |
| 键能/kJ·mol-1 | 436 | 496 | 463.4 |
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应ΔH=
(5)硝酸厂的尾气直接排放将污染空气,日前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
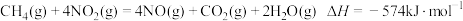

则甲烷直接将
 还原为
还原为 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】丙烯( )是仅次于乙烯(
)是仅次于乙烯( )的重要基本有机原料,工业上常利用丙烷(
)的重要基本有机原料,工业上常利用丙烷( )催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
)催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
①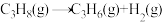 ;
;
②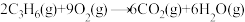 ;
;
③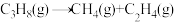 。
。
已知各物质的燃烧热如表,请计算反应①的反应热
_______ 。
 )是仅次于乙烯(
)是仅次于乙烯( )的重要基本有机原料,工业上常利用丙烷(
)的重要基本有机原料,工业上常利用丙烷( )催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:
)催化脱氢氧化制取丙烯。丙烷脱氢过程主要包含以下3个反应:①
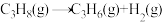 ;
;②
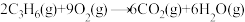 ;
;③
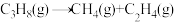 。
。已知各物质的燃烧热如表,请计算反应①的反应热

| 物质 |  |  |  |  |  |
燃烧热/( ) ) | 285.8 | 891.0 | 1411.0 | 2013.4 | 2217.8 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)下列变化过程,属于放热反应的是_______
①浓H2SO4稀释;②酸碱中和反应;③H2在Cl2中燃烧;④固体NaOH溶于水;⑤液态水变成水蒸气;⑥碳高温条件下还原CO2。
(2)实验测得,标准状况下11.2 L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出 的热量,试写出表示甲烷燃烧热的热化学方程式:
的热量,试写出表示甲烷燃烧热的热化学方程式:_______ ;
(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和 已经被用作工业捕碳剂,它们与CO2可发生如下反应:
已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ: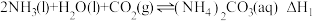
反应Ⅱ:
反应Ⅲ: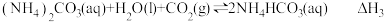
则 与
与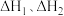 与之间的关系为
与之间的关系为
_______ ;
(4)已知反应 ,试根据表中所列键能数据估算a的值
,试根据表中所列键能数据估算a的值_______ 。
(1)下列变化过程,属于放热反应的是
①浓H2SO4稀释;②酸碱中和反应;③H2在Cl2中燃烧;④固体NaOH溶于水;⑤液态水变成水蒸气;⑥碳高温条件下还原CO2。
(2)实验测得,标准状况下11.2 L甲烷在氧气中充分燃烧生成液态水和二氧化碳气体时释放出
 的热量,试写出表示甲烷燃烧热的热化学方程式:
的热量,试写出表示甲烷燃烧热的热化学方程式:(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和
 已经被用作工业捕碳剂,它们与CO2可发生如下反应:
已经被用作工业捕碳剂,它们与CO2可发生如下反应:反应Ⅰ:
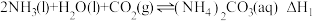
反应Ⅱ:

反应Ⅲ:
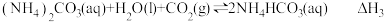
则
 与
与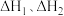 与之间的关系为
与之间的关系为
(4)已知反应
 ,试根据表中所列键能数据估算a的值
,试根据表中所列键能数据估算a的值| 化学键 |  |  |  |
键能/ | 436 | 391 | 945 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】NH3(g)燃烧生成NO2(g)和H2O(g),已知
①2H2(g)+O2(g)===2H2O(g) ΔH1=-480 kJ·mol-1
②N2(g)+2O2(g)===2NO2(g) ΔH2=68 kJ·mol-1
③N2(g)+3H2(g)===2NH3(g) ΔH3=-92 kJ·mol-1
NH3(g)燃烧生成NO2(g)和H2O(g) 的热化学方程式为________________________________ 。
①2H2(g)+O2(g)===2H2O(g) ΔH1=-480 kJ·mol-1
②N2(g)+2O2(g)===2NO2(g) ΔH2=68 kJ·mol-1
③N2(g)+3H2(g)===2NH3(g) ΔH3=-92 kJ·mol-1
NH3(g)燃烧生成NO2(g)和H2O(g) 的热化学方程式为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)直接排放含SO2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO2气体。1molCH4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示: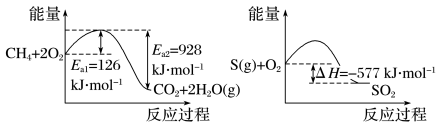
在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:___________ 。
(2)合成氨在工业生产中具有重要意义。在合成氨工业中I2O5常用于定量测定CO的含量。已知2I2(s)+5O2(g)=2I2O5(s) ΔH=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1.则该测定反应的热化学方程式为___________ 。
(3)化学反应原理研究物质转化过程中的规律并在生产生活中有广泛的应用。汽车排气管内的催化转化器可实现尾气无毒处理。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
CO2(g)=C(s)+O2(g) ΔH=+393.5kJ·mol-1
则反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的ΔH=___________ kJ·mol-1。
(4)氮及其化合物与人类生产、生活密切相关。氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用CO还原NO2至N2,当消耗标准状况下3.36LCO时,放出的热量为___________ kJ(用含有a和b的代数式表示)。
(1)直接排放含SO2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO2气体。1molCH4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示:

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:
(2)合成氨在工业生产中具有重要意义。在合成氨工业中I2O5常用于定量测定CO的含量。已知2I2(s)+5O2(g)=2I2O5(s) ΔH=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1.则该测定反应的热化学方程式为
(3)化学反应原理研究物质转化过程中的规律并在生产生活中有广泛的应用。汽车排气管内的催化转化器可实现尾气无毒处理。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
CO2(g)=C(s)+O2(g) ΔH=+393.5kJ·mol-1
则反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的ΔH=
(4)氮及其化合物与人类生产、生活密切相关。氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用CO还原NO2至N2,当消耗标准状况下3.36LCO时,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】温室气体的利用是当前环境和能源领域的研究热点。CH4与CO2重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
反应①CH4(g) + CO2(g)⇌2CO(g)+2H2 (g) ΔH1
反应②CO2 (g)+ H2 (g)⇌CO(g) + H2O(g) ΔH2= +41.2 kJ·mol-1
反应③CH4 (g)+ O2(g)⇌CO(g) + 2H2(g) ΔH3 = -35.6 kJ·mol-1
O2(g)⇌CO(g) + 2H2(g) ΔH3 = -35.6 kJ·mol-1
已知: O 2(g)+H2(g)= H2O(g) ΔH = -241.8 kJ·mol-1,则ΔH1 =
O 2(g)+H2(g)= H2O(g) ΔH = -241.8 kJ·mol-1,则ΔH1 =___________ kJ·mol-1。
反应①CH4(g) + CO2(g)⇌2CO(g)+2H2 (g) ΔH1
反应②CO2 (g)+ H2 (g)⇌CO(g) + H2O(g) ΔH2= +41.2 kJ·mol-1
反应③CH4 (g)+
 O2(g)⇌CO(g) + 2H2(g) ΔH3 = -35.6 kJ·mol-1
O2(g)⇌CO(g) + 2H2(g) ΔH3 = -35.6 kJ·mol-1已知:
 O 2(g)+H2(g)= H2O(g) ΔH = -241.8 kJ·mol-1,则ΔH1 =
O 2(g)+H2(g)= H2O(g) ΔH = -241.8 kJ·mol-1,则ΔH1 =
您最近一年使用:0次



