化学在生产生活中有广泛的应用,请用所学的知识填空:
(1)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解液为 KOH 溶液,则氢氧燃料电池的负极反应式为______ 。
(2)泡沫灭火器内盛有 Al2(SO4)3、NaHCO3溶液,写出其反应的离子方程式______ 。
(3)金属铍(Be)是高效率的火箭燃料,燃烧时放出巨大的能量,已知 1 g 铍完全燃烧放出的热量为 62. 70 kJ,则表示铍的燃烧热的热化学方程式为: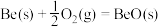 ∆H=
∆H=______ kJ·mol-1.
(4)FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的最后一步是在常温下调节溶液 pH=5,此时 c(Fe3+)=______ mol·L-1(已知:Ksp[Fe(OH)3]= 4.0×10-38)。
(1)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解液为 KOH 溶液,则氢氧燃料电池的负极反应式为
(2)泡沫灭火器内盛有 Al2(SO4)3、NaHCO3溶液,写出其反应的离子方程式
(3)金属铍(Be)是高效率的火箭燃料,燃烧时放出巨大的能量,已知 1 g 铍完全燃烧放出的热量为 62. 70 kJ,则表示铍的燃烧热的热化学方程式为:
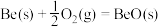 ∆H=
∆H=(4)FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的最后一步是在常温下调节溶液 pH=5,此时 c(Fe3+)=
更新时间:2021-01-30 20:35:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为_______ 。(选序号)写出4g H2燃烧的热化学方程式_______ ;
(2)24g C完全燃烧,放出的热量为_______ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。
(1)C燃烧热的热化学方程式为
(2)24g C完全燃烧,放出的热量为
(3)液态水的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。
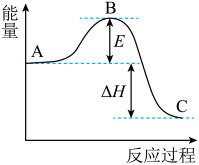
(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示____ 、____ ,E的大小对该反应的反应热____ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点____ (填“变大”、“变小”或“不变”)。
(2)图中ΔH=____ kJ·mol-1。
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式____ 。
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=____ 。

(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示
(2)图中ΔH=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】泡沫式灭火器内盛放Al2(SO4)3溶液(约1mol·L-1)、 NaHCO3溶液(约1mol·L-1)及起泡剂。使用时发生反应的化学方程式是____________________________ ,Al2(SO4)3溶液和 NaHCO3溶液的体积比约是______________ ;若用等体积等物质的量浓度的Na2CO3溶液代替 NaHCO3溶液,在使用时喷不出泡沫,这是因为______________________ 。泡沫灭火器玻璃筒里盛放Al2(SO4)3溶液,铁筒里存放 NaHCO3溶液,不能把Al2(SO4)3溶液盛放在铁筒里的原因是________________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列10种物质:①钠 ②明矾 ③ ④小苏打粉末 ⑤KOH ⑥
④小苏打粉末 ⑤KOH ⑥ 溶液 ⑦稀硫酸 ⑧
溶液 ⑦稀硫酸 ⑧ 固体 ⑨乙醇 ⑩盐酸
固体 ⑨乙醇 ⑩盐酸
回答下列问题:
(1)上述物质中属于电解质的有_____ (填序号)。
(2)将②的溶液和④的溶液混合,反应的离子方程式为_____ 。
(3)用 饱和溶液制取氢氧化铁胶体反应的化学方程式为
饱和溶液制取氢氧化铁胶体反应的化学方程式为_____ 。
(4)写出⑧ 固体在熔融时的电离方程式:
固体在熔融时的电离方程式:_____ 。
 ④小苏打粉末 ⑤KOH ⑥
④小苏打粉末 ⑤KOH ⑥ 溶液 ⑦稀硫酸 ⑧
溶液 ⑦稀硫酸 ⑧ 固体 ⑨乙醇 ⑩盐酸
固体 ⑨乙醇 ⑩盐酸回答下列问题:
(1)上述物质中属于电解质的有
(2)将②的溶液和④的溶液混合,反应的离子方程式为
(3)用
 饱和溶液制取氢氧化铁胶体反应的化学方程式为
饱和溶液制取氢氧化铁胶体反应的化学方程式为(4)写出⑧
 固体在熔融时的电离方程式:
固体在熔融时的电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】NaOH溶液可用于多种气体的处理.
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3.
①Na2CO3俗称纯碱,因CO32﹣水解而使其水溶液呈碱性,可用于除油污,写出CO32﹣水解的离子方程式_______________________ 。
②泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式_______________________ 。
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmol•L﹣1CH3COONa溶液,则两份溶液中
c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为_____ (已知HNO2的电离常数Ka=7.1×10﹣4mol•L﹣1,CH3COOH的电离常数Ka=1.7×10﹣5mol•L﹣1)。可使溶液A和溶液B的 pH相等的方法是___ 。
A 向溶液A中加适量NaOH B 向溶液A中加适量水
C 向溶液B中加适量NaOH D 向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过裎中,溶液中H2SO3、HSO3﹣、SO32﹣三者所占物质的量分数(a)随pH变化的关系如图所示:
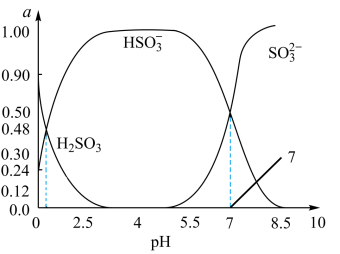
①图中pH=7时,溶液中离子浓度关系正确的是______ 。
A.c(Na+)>2c(SO32-)>c(HSO3-)
B.c(Na+)=c(SO32﹣) +c(HSO3﹣)+c(H2SO3)
C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO3﹣)
D.c(Na+)>c(HSO3﹣)>c(SO32﹣)> c(H+)=c(OH﹣)
②利用如图中数据,求H2SO3 H++ HSO3﹣的平衡常数的数值
H++ HSO3﹣的平衡常数的数值_____ (保留两位小数)。
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3.
①Na2CO3俗称纯碱,因CO32﹣水解而使其水溶液呈碱性,可用于除油污,写出CO32﹣水解的离子方程式
②泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmol•L﹣1CH3COONa溶液,则两份溶液中
c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为
A 向溶液A中加适量NaOH B 向溶液A中加适量水
C 向溶液B中加适量NaOH D 向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过裎中,溶液中H2SO3、HSO3﹣、SO32﹣三者所占物质的量分数(a)随pH变化的关系如图所示:

①图中pH=7时,溶液中离子浓度关系正确的是
A.c(Na+)>2c(SO32-)>c(HSO3-)
B.c(Na+)=c(SO32﹣) +c(HSO3﹣)+c(H2SO3)
C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO3﹣)
D.c(Na+)>c(HSO3﹣)>c(SO32﹣)> c(H+)=c(OH﹣)
②利用如图中数据,求H2SO3
 H++ HSO3﹣的平衡常数的数值
H++ HSO3﹣的平衡常数的数值
您最近一年使用:0次
【推荐1】回答下列问题。
(1)某小组同学探究饱和NaClO和 溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和
溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和 溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
溶液,产生大量的白色胶状沉淀。出现上述现象的原因是_________ (请用反应的离子方程式表示)。
(2) 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
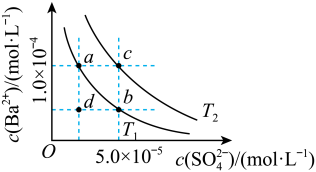
①T1_____ T2(填“<”“>”或“=”), 温度时
温度时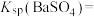
___________ 。
②根据 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是______ (填标号)。
A.加入 固体可由a点变为b点
固体可由a点变为b点
B. 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点
D.升温可由b点变为d点
③ 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7 mol/L)处理。若使
溶液(浓度为1.7 mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理_______ 次。
[提示: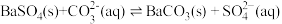 ,
,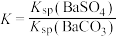 ,
,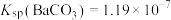 ]
]
(1)某小组同学探究饱和NaClO和
 溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和
溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和 溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
溶液,产生大量的白色胶状沉淀。出现上述现象的原因是(2)
 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
①T1
 温度时
温度时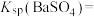
②根据
 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 固体可由a点变为b点
固体可由a点变为b点B.
 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为
 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点D.升温可由b点变为d点
③
 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7 mol/L)处理。若使
溶液(浓度为1.7 mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理[提示:
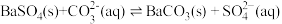 ,
,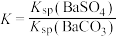 ,
, ]
]
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)实验室在配制氯化铁溶液时,常出现少许浑浊,原因离子方程式表示为______ 。为防止出现这样的现象,在配制时常加入______
(2)根据下列2个热化学反应方程式:
FeO(s)+CO(g)= Fe(s)+CO2(g) △H= ―218kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学反应方程式:______
(4)常温下,等物质的量的浓度的①氨水 ②NH4HSO4 ③NH4Cl ④(NH4)2CO3⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为______ (填序号)
(2)根据下列2个热化学反应方程式:
FeO(s)+CO(g)= Fe(s)+CO2(g) △H= ―218kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学反应方程式:
(4)常温下,等物质的量的浓度的①氨水 ②NH4HSO4 ③NH4Cl ④(NH4)2CO3⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知K、Ka、KW、Ksp分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是__ 。
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
(2)25℃时将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合所得溶液中c(NH4+)=c(Cl-),则溶液显__ (填“酸”、“碱”或“中”)性;用含a的代数式表示NH3•H2O的电离平衡常数Kb=__ 。
(3)已知25℃时CH3COOH和NH3.H2O电离常数相等,则该温度下CH3COONH4溶液中水电离的H+浓度为__ ,溶液中离子浓度大小关系为__ 。
(4)25℃时,H2SO3=HSO3-+H+的电离常数Ka=1×10-2mol•L-1,则该温度下pH=3、c(HSO3-)=0.1mol•L-1的NaHSO3溶液中c(H2SO3)=__ 。
(5)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10-38、1.0×10-11,向浓度均为0.1mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是__ 。(已知lg2=0.3)
(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
(2)25℃时将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合所得溶液中c(NH4+)=c(Cl-),则溶液显
(3)已知25℃时CH3COOH和NH3.H2O电离常数相等,则该温度下CH3COONH4溶液中水电离的H+浓度为
(4)25℃时,H2SO3=HSO3-+H+的电离常数Ka=1×10-2mol•L-1,则该温度下pH=3、c(HSO3-)=0.1mol•L-1的NaHSO3溶液中c(H2SO3)=
(5)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10-38、1.0×10-11,向浓度均为0.1mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氢能是一种极具发展潜力的清洁能源。3月29日,长城汽车氢能战略全球发布会推出氢能技术,并计划今年推出全球首款C级氢燃料电池SUV。关于氢能,根据要求回答问题:
I.制备氢气
制备氢气常采用以下方法:
①电解水法:2H2O 2H2↑+O2↑
2H2↑+O2↑
②水煤气法:C+H2O(g) CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2↑
CO2+H2↑
③太阳能光催化分解水法:2H2O 2H2↑+O2↑
2H2↑+O2↑
(1)三种方法中最节能的是___________ (填标号)。
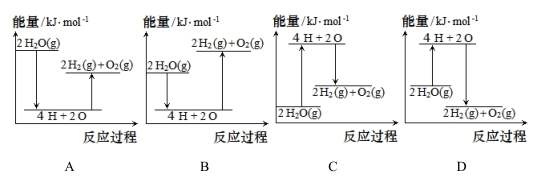
(2)已知拆开1 mol H -H、1 mol O=O和 1 mol H-О分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每3.6 gH2O(g)完全分解,需___________ (填“放出”或“吸收")能量___________ kJ。下列能正确表示该过程的能量变化示意图的是___________ (填标号)。
II.氢燃料电池
(3)氢燃料电池具有清洁高效等优点,其简易装置如下图所示。
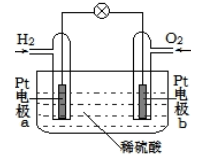
该电池正极反应式为___________ ;反应过程中将___________ 能转化为___________ 能。
I.制备氢气
制备氢气常采用以下方法:
①电解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑②水煤气法:C+H2O(g)
 CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2↑
CO2+H2↑③太阳能光催化分解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑(1)三种方法中最节能的是
(2)已知拆开1 mol H -H、1 mol O=O和 1 mol H-О分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每3.6 gH2O(g)完全分解,需

II.氢燃料电池
(3)氢燃料电池具有清洁高效等优点,其简易装置如下图所示。

该电池正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略混合后溶液的体积变化),实验数据如下表:
请回答:
(1)HA溶液和KOH溶液反应的离子方程式为_____ 。
(2)下列关于反应后的溶液说法不正确的是____ (填字母)。
a.实验②反应后溶液中只存在着两个平衡
b.实验②反应后溶液中:c(A-)+c(HA)>0.1mol·L-1
c.实验②反应后溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
d. 实验①反应后的溶液中由水电离出的c(OH-)=10-9mol·L-1;x>0.2mol·L-1
Ⅱ.已知2H2(g)+O2(g)=2H2O(1) ΔH=-572kJ·mol-1。某氢氧燃料电池以疏松多孔石墨棒为电极,KOH溶液为电解质溶液。
(3)写出该电池工作时负极的电极反应式____ 。
(4)若该氢氧燃料电池每释放228.8kJ电能时,会生成1mol液态水,则该电池的能量转化率为____ 。
| 实验序号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
(1)HA溶液和KOH溶液反应的离子方程式为
(2)下列关于反应后的溶液说法不正确的是
a.实验②反应后溶液中只存在着两个平衡
b.实验②反应后溶液中:c(A-)+c(HA)>0.1mol·L-1
c.实验②反应后溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
d. 实验①反应后的溶液中由水电离出的c(OH-)=10-9mol·L-1;x>0.2mol·L-1
Ⅱ.已知2H2(g)+O2(g)=2H2O(1) ΔH=-572kJ·mol-1。某氢氧燃料电池以疏松多孔石墨棒为电极,KOH溶液为电解质溶液。
(3)写出该电池工作时负极的电极反应式
(4)若该氢氧燃料电池每释放228.8kJ电能时,会生成1mol液态水,则该电池的能量转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.如图为原电池装置示意图。

(1)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,写出B电极反应式:__________ 。该电池在工作时,A电极的质量将_______ (填“增加”“减小”或“不变”),若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为________ 。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:_____________________________ 。该电池在工作一段时间后,溶液的碱性将________ (填“增强”“减弱”或“不变”)。
Ⅱ.现用图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。
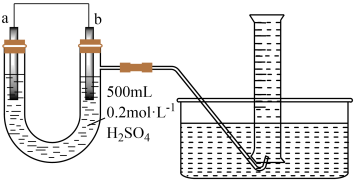
(3)b电极材料为________ ,其电极反应式为_________________________ 。
(4)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为________ mol,此时a电极质量________ (填“增加”或“减少”)________ g。
(5)如果将a、b两电极的电极材料对调,U形管中将出现的现象是_____________ 。

(1)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,写出B电极反应式:
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:
Ⅱ.现用图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。

(3)b电极材料为
(4)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为
(5)如果将a、b两电极的电极材料对调,U形管中将出现的现象是
您最近一年使用:0次

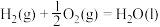
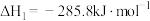
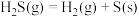
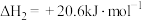


 由
由 和
和 组成的混合气体在足量氧气中充分燃烧,共放出
组成的混合气体在足量氧气中充分燃烧,共放出 的热量。
的热量。 。若用
。若用 溶液完全吸收生成的
溶液完全吸收生成的 ,则消耗
,则消耗 ~
~

