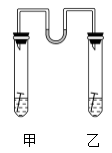
某小组按下图所示的装置探究铁的吸氧腐蚀。
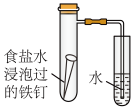
(1)写出正、负极反应的方程式。正极:_______ ,负极:_______ 。
(2)按图装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是_______ 。
a.用纯氧气代替具支试管内的空气
b.用纯铁代替铁钉
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(3)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施_______ (填“可行”或“不行”),原因是_______ 。

(1)写出正、负极反应的方程式。正极:
(2)按图装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.用纯铁代替铁钉
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(3)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施
更新时间:2023-12-27 11:45:19
|
相似题推荐
【推荐1】根据要求,回答下列问题:
Ⅰ.原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池的工作原理示意图。
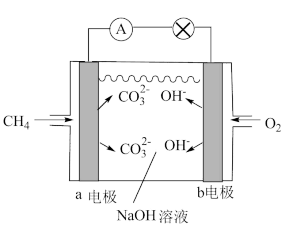
①电池的负极是__ 电极(填“a”或“b”),该极的电极反应为__ 。
②电池工作一段时间后,电解质溶液的pH__ (填“增大”“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应为CO+CO -2e-=2CO2。
-2e-=2CO2。
①正极反应是__ 。
②总反应是__ 。
Ⅱ.防止或减少钢铁的腐蚀有多种方法,如制成耐腐蚀合金,表面“烤蓝”,电镀另一种金属以及电化学保护等方法。
(3)钢铁的腐蚀主要是吸氧腐蚀。钢铁发生吸氧腐蚀时,负极反应为___ ,正极反应为___ 。
(4)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的___ 极(填“正”或“负”)相连,把镀层金属铬作___ 极(填“阳”或“阴”)。电镀铬时,不能用含有CrO 或Cr2O
或Cr2O 的溶液作电镀液,原因是
的溶液作电镀液,原因是___ 。
(5)利用如图装置,可以模拟铁的电化学保护。
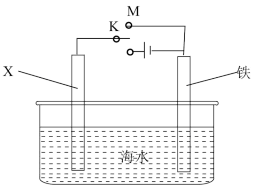
若X为碳棒,为减缓铁的腐蚀,开关K应置于___ 处(填“M”或“N”)。若X为锌,开关K置于M处,该电化学保护法称为__ 。
Ⅰ.原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池的工作原理示意图。

①电池的负极是
②电池工作一段时间后,电解质溶液的pH
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应为CO+CO
 -2e-=2CO2。
-2e-=2CO2。①正极反应是
②总反应是
Ⅱ.防止或减少钢铁的腐蚀有多种方法,如制成耐腐蚀合金,表面“烤蓝”,电镀另一种金属以及电化学保护等方法。
(3)钢铁的腐蚀主要是吸氧腐蚀。钢铁发生吸氧腐蚀时,负极反应为
(4)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的
 或Cr2O
或Cr2O 的溶液作电镀液,原因是
的溶液作电镀液,原因是(5)利用如图装置,可以模拟铁的电化学保护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】取6根铁钉,6支干净的试管及其他材料,如图所示。
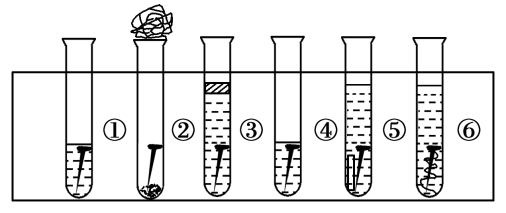
试管①放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管②在试管底部放入硅胶(是一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触;
试管③先放入一根铁钉,趁热倒入煮沸的蒸馏水(已赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触;
试管④中放入铁钉注入食盐水,使铁钉和空气及食盐水接触;
试管⑤放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片;
试管⑥放入相连的铁钉和铜丝,注入自来水,浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况。
(1)上述实验中铁钉发生了电化学腐蚀的是____ (填试管序号);在电化学腐蚀中,负极反应是____ ,正极反应是______ 。
(2)从铁钉被腐蚀的情况可知引起和促进铁钉被腐蚀的条件是_________ 。
(3)为防止铁的锈蚀,工业上普遍采用的方法是____________ (答两种方法)。

试管①放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管②在试管底部放入硅胶(是一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触;
试管③先放入一根铁钉,趁热倒入煮沸的蒸馏水(已赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触;
试管④中放入铁钉注入食盐水,使铁钉和空气及食盐水接触;
试管⑤放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片;
试管⑥放入相连的铁钉和铜丝,注入自来水,浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况。
(1)上述实验中铁钉发生了电化学腐蚀的是
(2)从铁钉被腐蚀的情况可知引起和促进铁钉被腐蚀的条件是
(3)为防止铁的锈蚀,工业上普遍采用的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
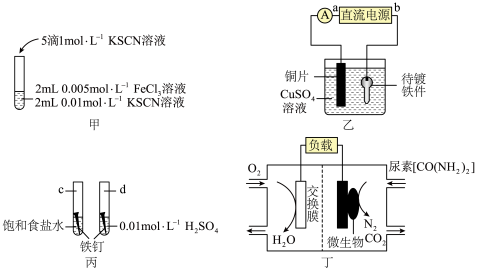
【推荐3】根据下列装置图,回答有关问题:___________ ,该反应为可逆反应,其离子方程式为___________ 。
(2)装置乙中,直流电源a为___________ 极(填“正”或“负”),阳极反应式为___________ 。
(3)装置丙中,d试管内铁钉除发生化学腐蚀外,还发生了___________ (填“析氢腐蚀”或“吸氧腐蚀”),其腐蚀速率比c试管中铁钉的腐蚀速率___________ (“快”“慢”或“相等”),c试管内正极的电极反应式为___________ 。
(4)装置丁中,从交换膜右侧向左侧迁移的离子是___________ ,负极的电极反应式为___________ 。
(2)装置乙中,直流电源a为
(3)装置丙中,d试管内铁钉除发生化学腐蚀外,还发生了
(4)装置丁中,从交换膜右侧向左侧迁移的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电化学与我们的生活有着密切的联系,请结合电化学知识回答下列有关问题。
(1)炒过菜的铁锅未及时洗净(残液中含有NaCl),不久便会因腐蚀而出现红棕色锈斑。试回答:
铁锅的锈蚀应属于________________ (填“析氢腐蚀”或“吸氧腐蚀”),铁锅锈蚀的负极反应式为:__________________ ;正负极反应产物会继续发生反应,最终生成的红棕色锈斑的主要成分是________________ (填化学式)。
(2)下图是一个电化学过程的示意图。
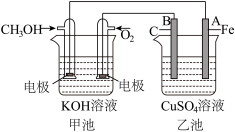
已知甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
①甲池是_______ 装置,通O2一极的电极反应式为____________________ 。
②乙池中反应的化学方程式为_____________________________ 。如果开始加入的CuSO4溶液足量,当乙池中A(Fe)极的质量增加3.2 g时,甲池中消耗O2_________ mL(标准状况下)。
(1)炒过菜的铁锅未及时洗净(残液中含有NaCl),不久便会因腐蚀而出现红棕色锈斑。试回答:
铁锅的锈蚀应属于
(2)下图是一个电化学过程的示意图。

已知甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
①甲池是
②乙池中反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】市场上出售的“热敷袋”其主要成分是铁屑、炭粉和少量的NaCl、水等。热敷袋在启用前用塑料袋使之与空气隔绝,启用时,打开塑料袋轻轻揉搓,就会放出热量,使用完后,会发现袋内有许多铁锈生成。回答:
(1)热敷袋放出的热量来源于_________ 放出的热量。
(2)炭粉的作用是________________________ 。
(3)加入NaCl的作用是________________________ 。
(4)写出有关电极反应式和化学方程式________________ 。
(1)热敷袋放出的热量来源于
(2)炭粉的作用是
(3)加入NaCl的作用是
(4)写出有关电极反应式和化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2018年7月至9月,国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。
已知:正常海水呈弱碱性。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为______ 。
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船水下遗址进行了处理。
① 考古队员贴在舰体上的材料块可以是______ (填字母序号)。
a.铝锌合金 b.石墨 c.铅 d.铜
② 采用“牺牲阳极的阴极保护法”后,水下舰体上正极的电极反应式为______ 。
(3)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施防止文物继续被腐蚀。从电化学原理的角度分析“脱盐、干燥”的防腐原理:______ 。
已知:正常海水呈弱碱性。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船水下遗址进行了处理。
① 考古队员贴在舰体上的材料块可以是
a.铝锌合金 b.石墨 c.铅 d.铜
② 采用“牺牲阳极的阴极保护法”后,水下舰体上正极的电极反应式为
(3)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施防止文物继续被腐蚀。从电化学原理的角度分析“脱盐、干燥”的防腐原理:
您最近一年使用:0次
【推荐1】化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.压强对化学平衡的影响。
(1)如图所示,用50 mL注射器吸入20 mLNO2和N2O4的混合气体(使注射器的活塞位于Ⅰ处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色变化为_____ 。

Ⅱ.沉淀的转化
(2)向盛有2 mL0.1 mol/LKI溶液的试管中滴加2滴0.1 mol/LAgNO3溶液,观察到的现象为_____ ,振荡试管,然后再向其中滴加8滴0.1 mol Na2S溶液,发生反应的离子方程式为_____ ,观察到的现象为_____ 。
Ⅲ.金属的腐蚀。
(3)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入如图所示的装置中,仪器a的名称为_____ ,几分钟后,观察导管中水柱的变化为______ ,引起这种变化的原因为_____ 。

Ⅰ.压强对化学平衡的影响。
(1)如图所示,用50 mL注射器吸入20 mLNO2和N2O4的混合气体(使注射器的活塞位于Ⅰ处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色变化为

Ⅱ.沉淀的转化
(2)向盛有2 mL0.1 mol/LKI溶液的试管中滴加2滴0.1 mol/LAgNO3溶液,观察到的现象为
Ⅲ.金属的腐蚀。
(3)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入如图所示的装置中,仪器a的名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】金属腐蚀在生活中随处可见,常见的有化学腐蚀和电化学腐蚀.
I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计(完成表中空格):
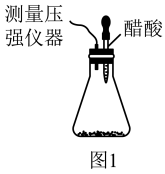
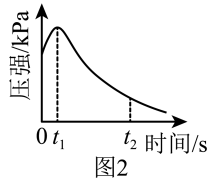
(2)编号①实验测得容器中压强随时间变化如图2。 时,容器中压强明显小于起始压强,其原因是铁发生了
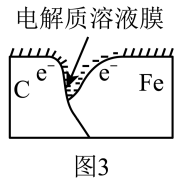
时,容器中压强明显小于起始压强,其原因是铁发生了________________ (填“吸氧”或“析氢”)腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动的方向________ ;此时,炭粉表面发生了________ (填“氧化”或“还原”)反应,其电极反应式是_______ 。
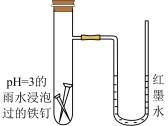
(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是_______ 。
(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
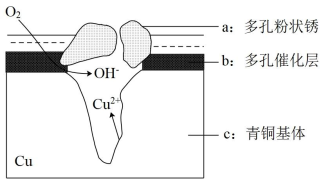
①腐蚀过程中,负极是______ (填“a”“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 ,其离子方程式为
,其离子方程式为____________ 。
I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计(完成表中空格):
| 编号 | 实验目的 | 炭粉质量/g | 铁粉质量/g | 醋酸质量分数/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |

(2)编号①实验测得容器中压强随时间变化如图2。
 时,容器中压强明显小于起始压强,其原因是铁发生了
时,容器中压强明显小于起始压强,其原因是铁发生了

(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是

(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次