金属腐蚀在生活中随处可见,常见的有化学腐蚀和电化学腐蚀.
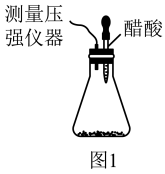
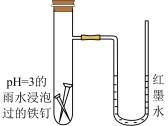
I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计(完成表中空格):
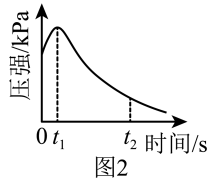
(2)编号①实验测得容器中压强随时间变化如图2。 时,容器中压强明显小于起始压强,其原因是铁发生了
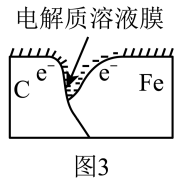
时,容器中压强明显小于起始压强,其原因是铁发生了________________ (填“吸氧”或“析氢”)腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动的方向________ ;此时,炭粉表面发生了________ (填“氧化”或“还原”)反应,其电极反应式是_______ 。
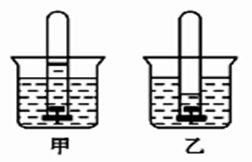
(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是_______ 。
(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
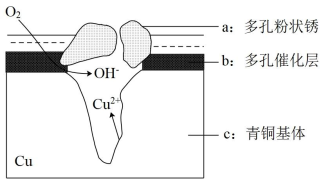
①腐蚀过程中,负极是______ (填“a”“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 ,其离子方程式为
,其离子方程式为____________ 。
I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计(完成表中空格):
| 编号 | 实验目的 | 炭粉质量/g | 铁粉质量/g | 醋酸质量分数/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |

(2)编号①实验测得容器中压强随时间变化如图2。
 时,容器中压强明显小于起始压强,其原因是铁发生了
时,容器中压强明显小于起始压强,其原因是铁发生了

(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是

(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 ,其离子方程式为
,其离子方程式为
21-22高二下·山西吕梁·阶段练习 查看更多[5]
山西省吕梁市临县第一中学2021-2022学年高二下学期5月月考化学试题(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)4.3 金属的腐蚀与防护-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(15-19)(已下线)考点20 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2022-05-29 09:21:36
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】钢铁工业是国家工业的支柱,每年钢铁生锈让国家损失大量资金,请回答钢铁腐蚀与防护过程中的有关问题。在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图为:
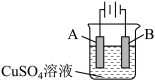
(1)A电极对应的金属是________ (写元素名称),B电极的电极反应式是________ ;
(2)若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为________ ;
(3)镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因________

(1)A电极对应的金属是
(2)若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为
(3)镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
您最近一年使用:0次
【推荐2】I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1) 铁锅的锈蚀是___________ 腐蚀(填“析氢”或“吸氧”);
(2) 写出铁锅腐蚀正极的电极反应式:___________ ;
(3) 关于铁的腐蚀随处可见,例如海水中船体的外壳易生锈,为此可在船体外壳设备上装上锌块以减缓金属的腐蚀,则该保护措施称___________ 法。
II.在如下图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色无味气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题:
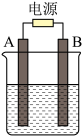
(1) A接的是电源的___________ 极;
(2) 写出电解时反应的总离子方程式___________ ;
(3) 电解后溶液的pH为___________ ;要使电解后溶液恢复到电解前的状态,则需加入___________ ,其质量为___________ (假设电解前后溶液的体积不变)。
(1) 铁锅的锈蚀是
(2) 写出铁锅腐蚀正极的电极反应式:
(3) 关于铁的腐蚀随处可见,例如海水中船体的外壳易生锈,为此可在船体外壳设备上装上锌块以减缓金属的腐蚀,则该保护措施称
II.在如下图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色无味气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题:

(1) A接的是电源的
(2) 写出电解时反应的总离子方程式
(3) 电解后溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)据中新社2017年6月29日电,也门遭世界最严重霍乱疫情 1400人死亡疑20余万人感染。霍乱是由霍乱弧菌引起的急性肠道传染病,患者常出现呕吐、腹泻、脱水和高烧等症状,重症和延误治疗可致死亡。据联合国儿童基金会专家表示,正常情况下,霍乱可以预防并且治愈率很高,但由于也门基础设施被完全损坏,将很难控制疾病传播。
请根据此信息和题意回答下列问题(填字母,下同)。
a.蛋白质 b.氨基酸 c.葡萄糖 d.变性 e.盐析
①霍乱弧菌中的主要成分中含有____________ ;该成分经水解后变为__________ ;
②为了预防霍乱,该疫情地区普遍采用喷洒消毒水进行消毒,对所接触到的器具均采用高温灭菌处理,这是因为在高温条件下病毒和细菌都发生了__________ 。
(2)化学与材料密切相关,材料是人类生存和发展的物质基础。
①在快中子反应堆中得以广泛应用的钠钾合金在常温下呈液态,这个事实说明合金的熔点比其成分金属的熔点_______ (填“高”或者“低”)。
②有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料而是一种线型高分子化合物,它具有_____________ 性(选填“热塑”或“热固”)。
③据报道,每年我国因金属腐蚀造成的损失占国民生产总值(GDP)的4%。钢铁在潮湿的空气中发生________ 腐蚀时,负极的电极反应为 ______________ 。
(3)化学与环境紧密联系。
①空气质量报告的各项指标可以反映出各地空气的质量。下列物质不属于空气污染物的是______ (填字母)
a.SO2 b.NO2 c.PM2.5 d.CO2
② 天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是__________________ ;加入明矾后, Al3+水解的离子方程式是 ________________ 。
③为减少SO2的排放量,可向煤中加入适量__________ (填名称);也可以将煤气化,即在高温条件下与水蒸气反应转化为水煤气,该反应方程式为___________________ 。
请根据此信息和题意回答下列问题(填字母,下同)。
a.蛋白质 b.氨基酸 c.葡萄糖 d.变性 e.盐析
①霍乱弧菌中的主要成分中含有
②为了预防霍乱,该疫情地区普遍采用喷洒消毒水进行消毒,对所接触到的器具均采用高温灭菌处理,这是因为在高温条件下病毒和细菌都发生了
(2)化学与材料密切相关,材料是人类生存和发展的物质基础。
①在快中子反应堆中得以广泛应用的钠钾合金在常温下呈液态,这个事实说明合金的熔点比其成分金属的熔点
②有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料而是一种线型高分子化合物,它具有
③据报道,每年我国因金属腐蚀造成的损失占国民生产总值(GDP)的4%。钢铁在潮湿的空气中发生
(3)化学与环境紧密联系。
①空气质量报告的各项指标可以反映出各地空气的质量。下列物质不属于空气污染物的是
a.SO2 b.NO2 c.PM2.5 d.CO2
② 天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是
③为减少SO2的排放量,可向煤中加入适量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学腐蚀分类
由于条件不同,钢铁的腐蚀可以分为析氢腐蚀和吸氧腐蚀两种类型。
(1)析氢腐蚀:在酸性环境中,由于腐蚀过程中不断有H2放出,所以叫做析氢腐蚀。
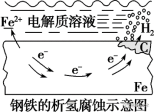
有关反应如下:
负极:___________ 。
正极:___________ 。
总反应:___________ 。
(2)吸氧腐蚀:如果钢铁表面吸附的水膜酸性很弱或呈中性,但溶有一定量的氧气,此时就发生吸氧腐蚀。
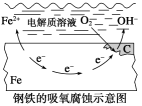
有关反应如下:
负极:___________ 。
正极:___________ 。
总反应:___________ 。
在空气中Fe(OH)2被进一步氧化成Fe(OH)3,Fe(OH)3失去部分水后生成Fe2O3·xH2O,它是铁锈的主要成分。
由于条件不同,钢铁的腐蚀可以分为析氢腐蚀和吸氧腐蚀两种类型。
(1)析氢腐蚀:在酸性环境中,由于腐蚀过程中不断有H2放出,所以叫做析氢腐蚀。

有关反应如下:
负极:
正极:
总反应:
(2)吸氧腐蚀:如果钢铁表面吸附的水膜酸性很弱或呈中性,但溶有一定量的氧气,此时就发生吸氧腐蚀。

有关反应如下:
负极:
正极:
总反应:
在空气中Fe(OH)2被进一步氧化成Fe(OH)3,Fe(OH)3失去部分水后生成Fe2O3·xH2O,它是铁锈的主要成分。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钢铁很容易生锈腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。因此,该小组同学又进行了钢铁腐蚀探究,希望能找到防止钢铁腐蚀的好办法。如图,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。红墨水柱两边液面变为:左低、右高。
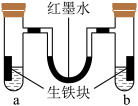
(1)请猜测a试管中铁发生的是________ (填“析氢”或“吸氧”)腐蚀。
(2)b管中生铁中碳上发生的电极反应式________________________ 。

(1)请猜测a试管中铁发生的是
(2)b管中生铁中碳上发生的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。

(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
正极__________ ,负极________ 。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸门上的固体材料R可以采用________ 。
A 铜 B 钠 C 锌 D 石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________ 极。

(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:
正极
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸门上的固体材料R可以采用
A 铜 B 钠 C 锌 D 石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铜在潮湿的空气中也能发生电化学腐蚀。
(1)铜___ (填“能”或“不能”)发生析氢腐蚀,原因是________________________________ 。
(2)若铜在中性或碱性环境中发生电化学腐蚀,则负极反应为________ ,正极反应为________ ,总反应为________ 。得到的产物还可与空气中的CO2继续反应,得到铜绿[Cu2(OH)2CO3],化学方程式是____________ 。
(3)若铜在酸性环境中发生电化学腐蚀,则正极反应为________ ,总反应为___________ 。
(4)工业上制取硫酸铜就是利用(3)的原理。试计算1 t铜理论上可以制得多少吨无水硫酸铜_____ ?
(1)铜
(2)若铜在中性或碱性环境中发生电化学腐蚀,则负极反应为
(3)若铜在酸性环境中发生电化学腐蚀,则正极反应为
(4)工业上制取硫酸铜就是利用(3)的原理。试计算1 t铜理论上可以制得多少吨无水硫酸铜
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。当燃料气为C2H4时,其正极、负极反应式分别为
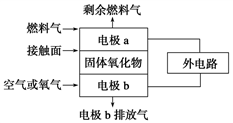
正极:______________________ ;
负极:____________________ 。
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为__________________ ;除去甲醇的离子方程式为___________ 。
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
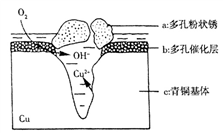
①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为______________________ ;
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为___________ L(标准状况)。

正极:
负极:
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,水槽中试管内有一枚铁钉,放置数天观察:

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生___ 腐蚀,正极反应式:___ 。
(3)若试管内液面下降,正极反应式:___ 。

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生
(3)若试管内液面下降,正极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.铝合金和钢铁是国家重要的金属材料。回答下列问题:
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有___________ (填序号)。A变为D所需的能量为E1,D变为E所需的能量为E2,则E1___________ E2(填“>”“<”或“=”),理由是___________ 。
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
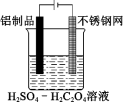
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为___________ 。
Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

通过上述实验分析回答:
(3)上述实验①、②探究___________ 对铁的腐蚀快慢的影响,写出实验②碳电极上的电极反应式___________ ;
(4)上述四个实验中___________ (用编号表示)发生吸氧腐蚀,上述四个实验铁腐蚀由快到慢的顺序为___________ (用编号表示)。
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为

Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

| 编号 | ① | ② | ③ | ④ |
| A | 100 mL饱和NaCl溶液 | 100 mL饱和NaCl溶液 | 100 mLpH = 2 CH3COOH | 100 mLpH = 5 H2SO4 |
| B | m g铁粉 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 |
| 锥形瓶中压强随时间变化 | 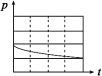 | 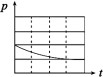 | 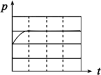 |  |
通过上述实验分析回答:
(3)上述实验①、②探究
(4)上述四个实验中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某小组按图1所示的装置探究铁的吸氧腐蚀。
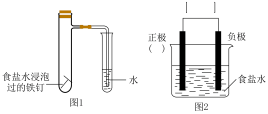
(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式_________ ;在方括号内用箭头表示出电子流动的方向___________ 。
(2)正极反应式为_____________________ ,负极反应式为__________________ 。
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是________ 。
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水

(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式
(2)正极反应式为
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
您最近一年使用:0次