某小组按图1所示的装置探究铁的吸氧腐蚀。
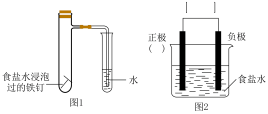
(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式_________ ;在方括号内用箭头表示出电子流动的方向___________ 。
(2)正极反应式为_____________________ ,负极反应式为__________________ 。
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是________ 。
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水

(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式
(2)正极反应式为
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
更新时间:2019-11-03 17:23:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】控制适合的条件,将反应2Fe3++2I-  2Fe2++I2设计成如图所示的原电池。回答下列问题:
2Fe2++I2设计成如图所示的原电池。回答下列问题:
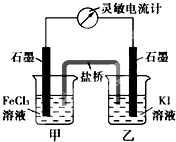
(1)反应开始时,乙中石墨电极上发生________ 反应(填“氧化”或“还原”),盐桥中的阴离子移向________ (填“甲”或“乙”)烧杯。
(2)反应开始时,甲中石墨电极上的电极反应式为________ 。
(3)反应达到化学平衡状态时,电流计指针________ 偏转。(填“是”或“否”)。
(4)反应达到平衡状态后,在甲中溶入FeCl2固体,乙中石墨电极为________ 极。
 2Fe2++I2设计成如图所示的原电池。回答下列问题:
2Fe2++I2设计成如图所示的原电池。回答下列问题:
(1)反应开始时,乙中石墨电极上发生
(2)反应开始时,甲中石墨电极上的电极反应式为
(3)反应达到化学平衡状态时,电流计指针
(4)反应达到平衡状态后,在甲中溶入FeCl2固体,乙中石墨电极为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为验证不同化合价铁的氧化能力,用下列电池装置进行实验:
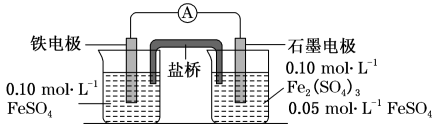
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(U∞)应尽可能地相近。根据下表数据,盐桥中应选择___________ 作为电解质。
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入___________ 电极溶液中。

(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(U∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | U∞×108/(m2∙s-1∙V-1) | 阴离子 | U∞×108/(m2∙s-1∙V-1) |
| Li+ | 4.07 |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl— | 7.91 |
| K+ | 7.62 |  | 8.27 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,请回答下列问题:
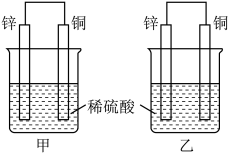
(1)下列说法正确的是________ 。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲____ 乙(填“>”、“<“或“=”)。
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为__________ 。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为______ 。
(5)利用下列反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电流方向,写出电极反应式。___

_______ 是正极,正极反应式:_____________ ;
________ 是负极,负极反应式:____________
(6)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂一碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中__ 作正极,负极的电极反应为_______ 。

(1)下列说法正确的是
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
(5)利用下列反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电流方向,写出电极反应式。

(6)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂一碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学与环境保护、人体健康、建筑材料等息息相关。
(1)天然水中杂质较多.常需加入明矾、ClO2等物质处理后才能饮用。加入ClO2 的作用是__ :加入明矾后,Al3+水解的离子方程式是_________________________ 。
(2)服装面料种类繁多。下列面料中不属于天然纤维的是__________ (填序号)。
a、棉和麻 b、丝和毛 c、涤纶和锦纶
(3)金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中更容易腐蚀,主要原因是钢铁里的铁和碳构成许多微小的___________ ,发生电化学腐蚀。
(4)“玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金。镁铝合金的优点是_________ :a.强度大 b.密度大 c.绝缘性好 d.耐腐蚀
(1)天然水中杂质较多.常需加入明矾、ClO2等物质处理后才能饮用。加入ClO2 的作用是
(2)服装面料种类繁多。下列面料中不属于天然纤维的是
a、棉和麻 b、丝和毛 c、涤纶和锦纶
(3)金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中更容易腐蚀,主要原因是钢铁里的铁和碳构成许多微小的
(4)“玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金。镁铝合金的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示三套实验装置,分别回答下列问题。
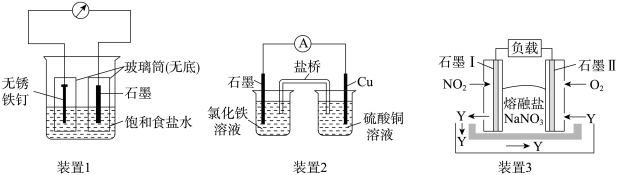
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被___________ (填“氧化”或“还原”);向插入石墨的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应式为___________ 。
(2)装置2中的石墨作___________ (填“正”或“负”)极,该装置发生的总反应的离子方程式为___________ 。
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为___________ (填化学式);石墨II极的电极反应式为:___________ ;当石墨I极中有1molNO2参加反应时,石墨II极消耗的O2的体积___________ (标准状况下)。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被
(2)装置2中的石墨作
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示,甲、乙两U形管各盛有100mL溶液,请回答下列问题:
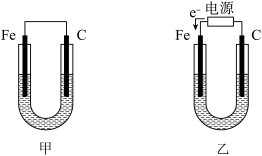
(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生_____________ 腐蚀(填“析氢”或“吸氧”),碳棒上电极反应式__________________________ ;
②甲池铁棒腐蚀的速率比乙池铁棒_____ (填“快”、“慢”或“相等”)。
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式___________________________________ ;
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为___________ mol·L-1。

(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生
②甲池铁棒腐蚀的速率比乙池铁棒
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.铝合金和钢铁是国家重要的金属材料。回答下列问题:
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有___________ (填序号)。A变为D所需的能量为E1,D变为E所需的能量为E2,则E1___________ E2(填“>”“<”或“=”),理由是___________ 。
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为___________ 。
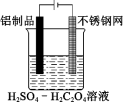
Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

通过上述实验分析回答:
(3)上述实验①、②探究___________ 对铁的腐蚀快慢的影响,写出实验②碳电极上的电极反应式___________ ;
(4)上述四个实验中___________ (用编号表示)发生吸氧腐蚀,上述四个实验铁腐蚀由快到慢的顺序为___________ (用编号表示)。
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为

Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

| 编号 | ① | ② | ③ | ④ |
| A | 100 mL饱和NaCl溶液 | 100 mL饱和NaCl溶液 | 100 mLpH = 2 CH3COOH | 100 mLpH = 5 H2SO4 |
| B | m g铁粉 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 |
| 锥形瓶中压强随时间变化 | 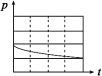 | 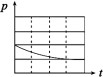 | 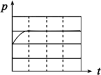 |  |
通过上述实验分析回答:
(3)上述实验①、②探究
(4)上述四个实验中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某小组按下图所示的装置探究铁的吸氧腐蚀。
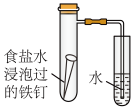
(1)写出正、负极反应的方程式。正极:_______ ,负极:_______ 。
(2)按图装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是_______ 。
a.用纯氧气代替具支试管内的空气
b.用纯铁代替铁钉
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(3)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施_______ (填“可行”或“不行”),原因是_______ 。

(1)写出正、负极反应的方程式。正极:
(2)按图装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.用纯铁代替铁钉
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(3)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施
您最近一年使用:0次




