(1)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。当燃料气为C2H4时,其正极、负极反应式分别为
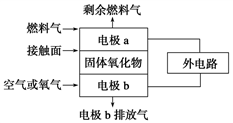
正极:______________________ ;
负极:____________________ 。
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为__________________ ;除去甲醇的离子方程式为___________ 。
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
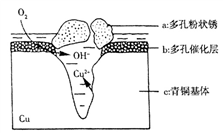
①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为______________________ ;
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为___________ L(标准状况)。

正极:
负极:
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为
更新时间:2017-03-07 14:46:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】发生化学反应时,物质变化的同时常常伴随有能量变化。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为_____ 能。
(2)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是_____ 。
②解释Cu片表面产生气泡的原因:_____ 。
(3)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
当H2和O2化合生成2molH2O(g)时,放出_____ kJ的能量。
(4)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
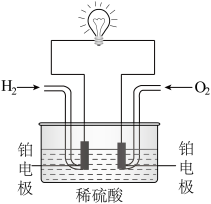
①通入O2的电极是电池的_____ (填“正”或“负”)极。
②通入H2的电极反应式是_____ 。
(1)将锌片放入盛有稀硫酸的烧杯中,用温度计测量。随反应进行,温度升高,说明化学能转变为
(2)将Zn片和Cu片用导线连接,并串联一个电流表,插入稀硫酸中,如图所示。

①证实化学能转化为电能的现象是
②解释Cu片表面产生气泡的原因:
(3)已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
| 化学键 | H-H | O=O | H-O |
| 键能/kJ•mol-1 | 436 | 498 | 463 |
当H2和O2化合生成2molH2O(g)时,放出
(4)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。

①通入O2的电极是电池的
②通入H2的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】科学家预言,燃料电池将是21世纪获得电力的重要途径,美国已计划将甲醇燃料电池用于军事目的。一种甲醇(CH3OH)燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气。回答下列问题:
(1)这种电极放电时发生的总反应是______________________________________ 。
(2)此电极的正极发生的电极反应式是__________________________ ;
负极发生的电极反应式是_______________________________ 。
(3)电解液中的H+离子向_________ 极(正极或负极)移动;通入正极的气体是________ .
(1)这种电极放电时发生的总反应是
(2)此电极的正极发生的电极反应式是
负极发生的电极反应式是
(3)电解液中的H+离子向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。
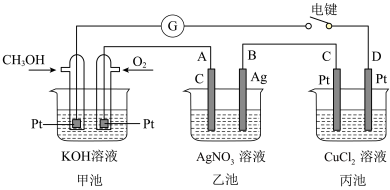
请回答下列问题:
(1)通入 电极的电极反应式为
电极的电极反应式为_______ 。
(2)乙池中A(石墨)电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),乙池总反应式为_______ 。
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗 的体积为
的体积为_______ mL(标准状况下),丙池中_______ 极析出_______ g铜。
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将_______ (填“增大”“减小”或“不变”;丙中溶液的pH将_______ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)通入
 电极的电极反应式为
电极的电极反应式为(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗
 的体积为
的体积为(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)可利用甲醇燃烧反应设计一个燃料电池。如图1所示,用 作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。

①写出燃料电池负极的电极反应式:_______ 。
②若利用该燃料电池作电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是_______ 极(填“A”或“B”);当铁件的质量增加 时,燃料电池中消耗标准状况下氧气的体积为
时,燃料电池中消耗标准状况下氧气的体积为_______ L。
(2)电解法可消除甲醇对水质造成的污染,原理为通电后 转化为
转化为 ,然后
,然后 将甲醇氧化成
将甲醇氧化成 和
和 (用石墨烯除去
(用石墨烯除去 )。现用如图2所示装置模拟上述过程,则
)。现用如图2所示装置模拟上述过程,则 在阳极的电极反应式为
在阳极的电极反应式为_______ 。除去甲醇的离子方程式为_______ 。
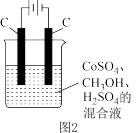
(3)一种用铅蓄电池进行电絮凝净水装置如图3所示,回答下列问题:

①装置Ⅰ中Y电极的电极材料是_______ (填化学式),工作时 向
向_______ (填“X”或“Y”)电极移动;Y电极的电极反应式为_______ 。
②装置Ⅱ中 电极的电极反应式为
电极的电极反应式为_______ 。
③每消耗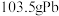 ,装置的电流效率为
,装置的电流效率为 ,则理论上电解池阴极上生成
,则理论上电解池阴极上生成_______  。
。
(1)可利用甲醇燃烧反应设计一个燃料电池。如图1所示,用
 作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
①写出燃料电池负极的电极反应式:
②若利用该燃料电池作电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是
 时,燃料电池中消耗标准状况下氧气的体积为
时,燃料电池中消耗标准状况下氧气的体积为(2)电解法可消除甲醇对水质造成的污染,原理为通电后
 转化为
转化为 ,然后
,然后 将甲醇氧化成
将甲醇氧化成 和
和 (用石墨烯除去
(用石墨烯除去 )。现用如图2所示装置模拟上述过程,则
)。现用如图2所示装置模拟上述过程,则 在阳极的电极反应式为
在阳极的电极反应式为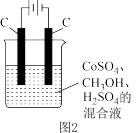
(3)一种用铅蓄电池进行电絮凝净水装置如图3所示,回答下列问题:

①装置Ⅰ中Y电极的电极材料是
 向
向②装置Ⅱ中
 电极的电极反应式为
电极的电极反应式为③每消耗
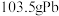 ,装置的电流效率为
,装置的电流效率为 ,则理论上电解池阴极上生成
,则理论上电解池阴极上生成 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:_
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置______ (填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请指出正、负极______
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入____________ 极(填a或b,下同),电子从__________ 极流出。a极发生电极反应式为:_________________________

(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.下列物质:①16O和18O ②红磷和白磷 ③CH3CH3和CH3CH2CH2CH3 ④CH3CH2CH2CH3 和CH3CH (CH3) 2 ⑤O2和O3 ⑥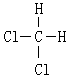 和
和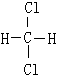
(1)属于同素异形体的是(填序号,下同)_______ ,
(2)属于同系物的是_____________ 。
II.乙烯的产量可以用来衡量一个国家的石油化工发展水平.请回答:
(1)乙烯的结构式是___________ .
(2)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为______ .
(3)可以用来除去乙烷中混有的乙烯的试剂是______ .(填序号)
①水 ②氢气 ③溴水 ④酸性高锰酸钾溶液
(4)在一定条件下,乙烯能与水反应生成有机物A,A的结构简式是______ ,其反应类型是______ 反应(填“取代”或“加成”).
(5)下列化学反应原理相同的是______ (填序号).
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②SO2使溴水和酸性高锰酸钾溶液褪色
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色
Ⅲ.如图所示为CH4燃料电池的装置(A、B为多孔碳棒):
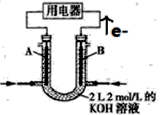
(1)_____ (填A或B)处电极入口通甲烷,其电极反应式为______________ ;
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,消耗KOH的质量为_______ g。
IV.铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极的电极反应为____________________ 。
 和
和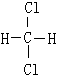
(1)属于同素异形体的是(填序号,下同)
(2)属于同系物的是
II.乙烯的产量可以用来衡量一个国家的石油化工发展水平.请回答:
(1)乙烯的结构式是
(2)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为
(3)可以用来除去乙烷中混有的乙烯的试剂是
①水 ②氢气 ③溴水 ④酸性高锰酸钾溶液
(4)在一定条件下,乙烯能与水反应生成有机物A,A的结构简式是
(5)下列化学反应原理相同的是
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②SO2使溴水和酸性高锰酸钾溶液褪色
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色
Ⅲ.如图所示为CH4燃料电池的装置(A、B为多孔碳棒):

(1)
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,消耗KOH的质量为
IV.铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极的电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮的化合物合成、应用及氮的固定一直是科学研究的热点。
(1) 以CO2与NH3为原料合成化肥尿素的主要反应如下:
① 2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol−1
② NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);ΔH=a kJ·mol−1
③ 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol−1
则a为____ 。
(2) 尿素可用于湿法烟气脱氮工艺,其反应原理为:NO+NO2+H2O=2HNO2;2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
① 当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)=____ (空气中氧气的体积含量大约为20%)。
② 如图表示尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为____ %。
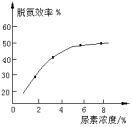
(3)用稀硝酸吸收NOx,得到HNO3和HNO2(弱酸)的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:____ 。
(4)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图所示。
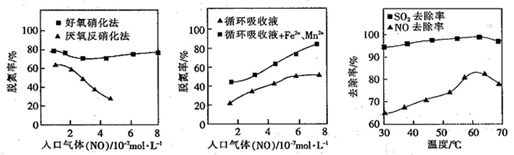
① 由图知,当废气中的NO含量增加时,宜选用____ 法提高脱氮的效率。
② 图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为____ 。
(5)研究表明:NaClO/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为____ 。
(1) 以CO2与NH3为原料合成化肥尿素的主要反应如下:
① 2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol−1
② NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);ΔH=a kJ·mol−1
③ 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol−1
则a为
(2) 尿素可用于湿法烟气脱氮工艺,其反应原理为:NO+NO2+H2O=2HNO2;2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
① 当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)=
② 如图表示尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为

(3)用稀硝酸吸收NOx,得到HNO3和HNO2(弱酸)的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:
(4)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图所示。

① 由图知,当废气中的NO含量增加时,宜选用
② 图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为
(5)研究表明:NaClO/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学能与电能之间的相互转化与人的生活实际密切相关,在生产、生活中有重要的应用,同时也是学生形成化学学科素养的重要组成部分。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池(如图1),反应原理为:2Na+FeCl2 Fe+2NaCl,该电池放电时,正极反应式为
Fe+2NaCl,该电池放电时,正极反应式为_____ :
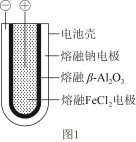
充电时,_____ (写物质名称)电极接电源的负极;该电池的电解质为_____ 。
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液(如图2),一段时间停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:
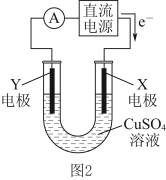
①Y电极材料是_____ ,发生_____ (填“氧化或还原”)反应。
②电解过程中X电极上发生的电极反方应式是:_____
③若在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是_____
(3)常温时,BaSO4的Ksp=1.08×10−10,现将等体积的BaCl2溶液与2.0×10−3 mol∙L−1的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为_____ 。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池(如图1),反应原理为:2Na+FeCl2
 Fe+2NaCl,该电池放电时,正极反应式为
Fe+2NaCl,该电池放电时,正极反应式为
充电时,
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液(如图2),一段时间停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:

①Y电极材料是
②电解过程中X电极上发生的电极反方应式是:
③若在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是
(3)常温时,BaSO4的Ksp=1.08×10−10,现将等体积的BaCl2溶液与2.0×10−3 mol∙L−1的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示3套实验装置,分别回答下列问题。
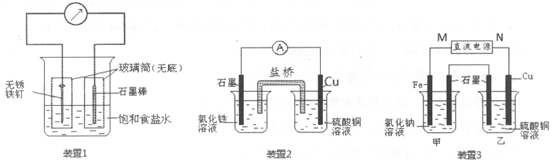
(1)装置1为铁的吸氧腐蚀实验,一段时间后,玻璃筒内的石墨电极上的电极反应式为_________ 。
(2)装置2中的石墨是_______ 极,该电极反应式为___________ 。
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为________ 极;甲烧杯中铁电极的电极反应为_________________ 。
②乙烧杯中电解的总方程式为_______________ 。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为________ mL。

(1)装置1为铁的吸氧腐蚀实验,一段时间后,玻璃筒内的石墨电极上的电极反应式为
(2)装置2中的石墨是
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为
②乙烧杯中电解的总方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)依据反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如下图甲所示。

①电极X的材料是_________________ ;
②外电路中的电子是从___ 电极流向__ 电极(填电极材料名称或符号)。
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是___________ (填离子符号)。
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:____________________ 。
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用__________ (填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的____ 极。
(3)蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2+ Fe + 2H2O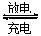 Fe(OH)2+ Ni(OH)2。
Fe(OH)2+ Ni(OH)2。
①若此蓄电池放电时,该电池某一电极发生还原反应的物质是__ (填序号)。
A.NiO2B.Fe C.Fe(OH)2D.Ni(OH)2
②该电池放电时,正极附近溶液的pH________ (填增大、减小、不变)
③充电时该电池阳极的电极反应式___________________________ 。

①电极X的材料是
②外电路中的电子是从
③在电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向CuSO4溶液一端扩散的离子是
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀。炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈。请写出铁锅生锈过程的正极反应式:
②为了减缓某水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的
(3)蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2+ Fe + 2H2O
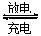 Fe(OH)2+ Ni(OH)2。
Fe(OH)2+ Ni(OH)2。①若此蓄电池放电时,该电池某一电极发生还原反应的物质是
A.NiO2B.Fe C.Fe(OH)2D.Ni(OH)2
②该电池放电时,正极附近溶液的pH
③充电时该电池阳极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁的腐蚀和防护与生产、生活密切相关。已知:氢氧化物开始和完全沉淀的pH如下表(开始沉淀时,金属离子的浓度为1.0mol/L)。完成下列问题。
(1)研究铁的腐蚀。将一定量铁粉和碳粉混合后置于一密闭容器中,加入NaCl和盐酸的混合溶液。测得溶液的pH和压强随时间变化的曲线如图所示。

①容器内压强先增大后减小,除温度影响外的原因是___________ 。
②反应过程中,混合液里先生成的Fe2+会被氧化生成Fe(OH)3,反应的离子方程式为___________ 。
③700s后pH略下降,原因是___________ 。
(2)研究铁的防护。在铁表面镀锌可有效防止铁被腐蚀。
已知:溶液中Zn2+与NH3可发生反应:Zn2++nNH3 [ Zn(NH3)n]2+(n= 1~4)。某镀锌废液中含有Zn2+(<1mol/L)、Fe2+、Fe3+、
[ Zn(NH3)n]2+(n= 1~4)。某镀锌废液中含有Zn2+(<1mol/L)、Fe2+、Fe3+、 、H+等阳离子。请设计利用该电镀废液回收ZnCl2-NH4Cl溶液的实验方案:
、H+等阳离子。请设计利用该电镀废液回收ZnCl2-NH4Cl溶液的实验方案:___________ 。(实验中可选用试剂:30%H2O2、1.0mol/LNaOH溶液、1.0mol/L氨水)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀时的pH | 3.2 | 8.8 | 8.0 |

①容器内压强先增大后减小,除温度影响外的原因是
②反应过程中,混合液里先生成的Fe2+会被氧化生成Fe(OH)3,反应的离子方程式为
③700s后pH略下降,原因是
(2)研究铁的防护。在铁表面镀锌可有效防止铁被腐蚀。
已知:溶液中Zn2+与NH3可发生反应:Zn2++nNH3
 [ Zn(NH3)n]2+(n= 1~4)。某镀锌废液中含有Zn2+(<1mol/L)、Fe2+、Fe3+、
[ Zn(NH3)n]2+(n= 1~4)。某镀锌废液中含有Zn2+(<1mol/L)、Fe2+、Fe3+、 、H+等阳离子。请设计利用该电镀废液回收ZnCl2-NH4Cl溶液的实验方案:
、H+等阳离子。请设计利用该电镀废液回收ZnCl2-NH4Cl溶液的实验方案:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某小组按图1所示的装置探究铁的吸氧腐蚀。
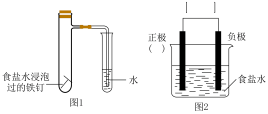
(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式_________ ;在方括号内用箭头表示出电子流动的方向___________ 。
(2)正极反应式为_____________________ ,负极反应式为__________________ 。
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是________ 。
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水

(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式
(2)正极反应式为
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
您最近一年使用:0次



