葡萄糖(分子式为 )是人体内最重要的供能物质。
)是人体内最重要的供能物质。
(1)正常的血液中葡萄糖(简称血糖)的浓度在0.70~1.15g/L之间,下表是某同学的血液检测单的部分内容:
葡萄糖的摩尔质量为___________ ,该同学1mL血液中含有的葡萄糖为___________ 毫克,其血糖含量___________ (填“正常”、“偏高”或“偏低”)。
(2)50%葡萄糖注射液风于高糖溶液,在医疗上具有广泛的用途。50%葡萄糖注射液是指每100mL葡萄糖注射液中含有50g葡萄糖,某同学使用称好的葡萄糖固体在实验室中配制220mL该葡萄糖注射液,所需的定量仪器是___________ 。
(3)病人输液时,通常采用一定浓度的葡萄糖注射液。小附同学欲利用上述50%葡萄糖注射液在实验室中配制80mL 0.250mol/L的葡萄糖溶液。
①需要用量筒量取50%葡萄糖注射液的体积是___________ mL。
②下列操作会导致所配溶液的物质的量浓度偏低的是___________ (填选项)。
A.没有将洗涤液转移到容量瓶 B.量取50%葡萄糖注射液时俯视
C.容量瓶洗净后未干燥 D.定容时俯视
 )是人体内最重要的供能物质。
)是人体内最重要的供能物质。(1)正常的血液中葡萄糖(简称血糖)的浓度在0.70~1.15g/L之间,下表是某同学的血液检测单的部分内容:
| 项目名称 | 钾 | 葡萄糖 | 低密度脂蛋白 |
| 血液中的含量(mmol/L) | 3.91 | 3.00 | 2.96 |
(2)50%葡萄糖注射液风于高糖溶液,在医疗上具有广泛的用途。50%葡萄糖注射液是指每100mL葡萄糖注射液中含有50g葡萄糖,某同学使用称好的葡萄糖固体在实验室中配制220mL该葡萄糖注射液,所需的定量仪器是
(3)病人输液时,通常采用一定浓度的葡萄糖注射液。小附同学欲利用上述50%葡萄糖注射液在实验室中配制80mL 0.250mol/L的葡萄糖溶液。
①需要用量筒量取50%葡萄糖注射液的体积是
②下列操作会导致所配溶液的物质的量浓度偏低的是
A.没有将洗涤液转移到容量瓶 B.量取50%葡萄糖注射液时俯视
C.容量瓶洗净后未干燥 D.定容时俯视
更新时间:2023-12-27 13:40:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学研究性学习小组欲配制含有 、
、 、
、 、
、 的植物培养液450mL,且要求该培养液中
的植物培养液450mL,且要求该培养液中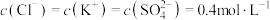 '。实验室提供的药品有:
'。实验室提供的药品有: 、KCl、
、KCl、 、
、 和蒸馏水;提供的实验仪器有:①药匙、②烧杯、③玻璃棒、④胶头滴管、⑤量筒、⑥称量纸。请回答下列问题:
和蒸馏水;提供的实验仪器有:①药匙、②烧杯、③玻璃棒、④胶头滴管、⑤量筒、⑥称量纸。请回答下列问题:
(1)该植物培养液中, 的物质的量浓度为
的物质的量浓度为_________ 。
(2)该研究小组配制该植物培养液时,还须用到的实验仪器有_________ 。
(3)甲同学用KCl和 两种物质进行配制,则需称取
两种物质进行配制,则需称取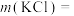
_________ g,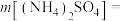
_________ g。
(4)乙同学用所提供药品中的三种进行配制,请帮助该同学选用三种物质:_________ 、_________ 、_________ 。(填化学式)
(5)本实验中玻璃棒的作用有_________ 、_________ 。
(6)请将下列实验步骤按照先后顺序排列:_________ 。
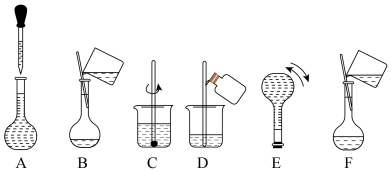
(7)请用恰当的文字描述上图A操作的过程:_________ 。
(8)若配制该培养液的其他操作均正确,则下列错误操作将使所配制溶液的浓度偏低的是_________ (填字母)。
a.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
b.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶
c.用胶头滴管向容量瓶中加水时,溶液的凹液面高于容量瓶刻度线
d.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线
 、
、 、
、 、
、 的植物培养液450mL,且要求该培养液中
的植物培养液450mL,且要求该培养液中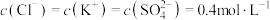 '。实验室提供的药品有:
'。实验室提供的药品有: 、KCl、
、KCl、 、
、 和蒸馏水;提供的实验仪器有:①药匙、②烧杯、③玻璃棒、④胶头滴管、⑤量筒、⑥称量纸。请回答下列问题:
和蒸馏水;提供的实验仪器有:①药匙、②烧杯、③玻璃棒、④胶头滴管、⑤量筒、⑥称量纸。请回答下列问题:(1)该植物培养液中,
 的物质的量浓度为
的物质的量浓度为(2)该研究小组配制该植物培养液时,还须用到的实验仪器有
(3)甲同学用KCl和
 两种物质进行配制,则需称取
两种物质进行配制,则需称取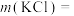
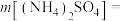
(4)乙同学用所提供药品中的三种进行配制,请帮助该同学选用三种物质:
(5)本实验中玻璃棒的作用有
(6)请将下列实验步骤按照先后顺序排列:

(7)请用恰当的文字描述上图A操作的过程:
(8)若配制该培养液的其他操作均正确,则下列错误操作将使所配制溶液的浓度偏低的是
a.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
b.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶
c.用胶头滴管向容量瓶中加水时,溶液的凹液面高于容量瓶刻度线
d.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
(1)该“84消毒液”的物质的浓度约为___________ mol/L。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=___________ mol/L。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是___________(填字母)。
(4)一瓶上述“威露士”牌“84消毒液”能吸收空气中___________ L的CO2(标准状况)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8g·cm-3)的浓硫酸配制100mL物质的量浓度为0.8mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为___________ mol/L
②需要用量筒取___________ mL上述浓硫酸进行配制。
③为配制上述稀硫酸,除了量筒、烧杯、玻璃棒外,还缺少的玻璃仪器是___________ 、___________ 。
④在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是___________ (填序号)。
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出
f.未洗涤稀释浓硫酸的烧杯
| 84消毒液 有效成分 NaClO 规格 1000mL 质量分数 25% 密度 1.19g/cm3 |
(1)该“84消毒液”的物质的浓度约为
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是___________(填字母)。

| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.利用购买的商品NaClO来配制可能导致结果偏低 |
| D.需要称量NaClO固体的质量为142.8g |
(4)一瓶上述“威露士”牌“84消毒液”能吸收空气中
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8g·cm-3)的浓硫酸配制100mL物质的量浓度为0.8mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为
②需要用量筒取
③为配制上述稀硫酸,除了量筒、烧杯、玻璃棒外,还缺少的玻璃仪器是
④在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出
f.未洗涤稀释浓硫酸的烧杯
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室需要0.1mol•L-1NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填序号),配制上述溶液还需用到的玻璃仪器是___________ (填仪器名称)。

(2)根据计算用托盘天平称取NaOH的质量为___________ g。
(3)由计算得知,所需质量分数为98%、密度为1.84g•cm-3的浓硫酸的体积为___________ mL(计算结果保留一位小数)。如果实验室有15mL、20mL、50mL量筒,应选用___________ mL量筒最好。
(4)在配制稀H2SO4的过程中,下列情况对硫酸溶液物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)?
①未经冷却趁热将溶液注入容量瓶中:___________ 。
②定容时仰视观察液面:___________ 。
③用量筒量取浓硫酸时俯视:___________ 。
(1)如图所示的仪器中配制溶液肯定不需要的是

(2)根据计算用托盘天平称取NaOH的质量为
(3)由计算得知,所需质量分数为98%、密度为1.84g•cm-3的浓硫酸的体积为
(4)在配制稀H2SO4的过程中,下列情况对硫酸溶液物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)?
①未经冷却趁热将溶液注入容量瓶中:
②定容时仰视观察液面:
③用量筒量取浓硫酸时俯视:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学用NaOH固体配制250mL 2.0mol/L的NaOH溶液,并进行有关实验。请回答下列问题:
(1)需要称取NaOH固体__________ g。
(2)配制该NaOH溶液时使用的仪器除托盘天平(砝码、镊子)、药匙、量筒、250mL容量瓶、胶头滴管外,还必须用到的仪器有_____ 、_____ 等。
(3)取所配制的NaOH溶液100mL,与一定质量的铝充分反应,铝全部溶解后,生成的气体在标准状况下的体积为3.36L,则参加反应的铝的质量为___ g,设反应后溶液的体积仍为100mL,则反应后溶液中OH-的物质的量浓度为(不考虑水解)__ mol/L。
(1)需要称取NaOH固体
(2)配制该NaOH溶液时使用的仪器除托盘天平(砝码、镊子)、药匙、量筒、250mL容量瓶、胶头滴管外,还必须用到的仪器有
(3)取所配制的NaOH溶液100mL,与一定质量的铝充分反应,铝全部溶解后,生成的气体在标准状况下的体积为3.36L,则参加反应的铝的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。回答下列问题:

(1)该“84消毒液”的物质的量浓度约为____ (结果精确到0.1)mol•L-1。
(2)某同学取100mL该“84消毒液”,稀释100倍后用于消毒,稀释后的溶液中c(Na+)=____ mol•L-1。
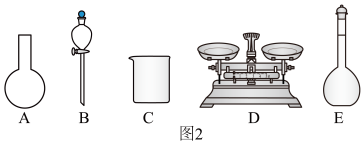
(3)该同学参阅此“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是____ (填字母)。
(4)若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)
①定容时仰视容量瓶刻度线____ 。
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面____ 。
③容量瓶在使用前刚刚配制完一定物质的量浓度的“84消毒液”而未洗净____ 。
④定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线____ 。
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组用98%(ρ=1.84g•cm-3)的浓硫酸配制2L2.3mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力,需用浓硫酸的体积为____ mL。

(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100mL该“84消毒液”,稀释100倍后用于消毒,稀释后的溶液中c(Na+)=
(3)该同学参阅此“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是

| A.如图2所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.需要称量NaClO固体的质量为123.0g |
| D.配制该溶液的操作顺序:计算→称量→溶解→移液→洗涤→定容→摇匀 |
①定容时仰视容量瓶刻度线
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面
③容量瓶在使用前刚刚配制完一定物质的量浓度的“84消毒液”而未洗净
④定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组用98%(ρ=1.84g•cm-3)的浓硫酸配制2L2.3mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力,需用浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】已知某84消毒液瓶体部分标签如图,请回答下列问题。
(1)该“84消毒液”中c(NaClO)=______ mol∙L-1(结果保留两位小数);
若实验室中需要480 mL标签所示浓度的84消毒液,则需要用电子天平称量NaClO固体______ g。将称好的固体加水溶解,待______ 后将溶液沿______ 转移入______ 加蒸馏水至液面距刻度______ cm时,改用______ 滴加水,直至凹液面的最低处与刻度线相切。
(2)取100 mL 4.0 mol∙L-1 “84消毒液”稀释100倍(体积比)后用于消毒,稀释后的溶液中c(NaClO)=______ mol∙L-1(结果保留两位小数)。
(3)若出现以下情况,所配制溶液浓度将偏高的是______。
| 84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】25% 【密度】1.19 g·cm-3 |
若实验室中需要480 mL标签所示浓度的84消毒液,则需要用电子天平称量NaClO固体
(2)取100 mL 4.0 mol∙L-1 “84消毒液”稀释100倍(体积比)后用于消毒,稀释后的溶液中c(NaClO)=
(3)若出现以下情况,所配制溶液浓度将偏高的是______。
| A.定容时仰视容量瓶刻度线 |
| B.洗涤后的容量瓶未干燥 |
| C.溶解后未冷却就进行下一步操作 |
| D.容量瓶在使用前刚刚配制完一定物质的量浓度的84消毒液而未洗净 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图:
请回答下列问题:
(1)配制溶液时,一般可以分为以下几个主要步骤,其正确的操作顺序为_______ (填序号)。
①量取②计算③溶解④定容⑤转移⑥洗涤⑦装瓶
(2)实验室只有100mL、250mL、500mL三种规格的容量瓶,实验室需要480mL0.50mol/L的稀硫酸,需取该浓硫酸_______ mL。
(3)接下来完成此实验将用到的仪器有20mL量筒、烧杯、玻璃棒、胶头滴管、_______ 。
(4)下列操作会使所配溶液浓度偏低的是_______ (填字母)。
A.用量筒量取浓硫酸,读数时仰视刻度线
B.转移溶液时未洗涤烧杯
C.容量瓶用蒸馏水洗净后仍残留有蒸馏水
D.定容时俯视容量瓶的刻度线
E.定容摇匀后,发现液面低于刻度线,再加水至刻度线
(5)用锌与足量的该硫酸反应得到标况下11. 2L H2 ,则消耗锌的质量为_______ g。
| 硫酸化学纯(CP) (500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g ·cm-3 质量分数:98% |
(1)配制溶液时,一般可以分为以下几个主要步骤,其正确的操作顺序为
①量取②计算③溶解④定容⑤转移⑥洗涤⑦装瓶
(2)实验室只有100mL、250mL、500mL三种规格的容量瓶,实验室需要480mL0.50mol/L的稀硫酸,需取该浓硫酸
(3)接下来完成此实验将用到的仪器有20mL量筒、烧杯、玻璃棒、胶头滴管、
(4)下列操作会使所配溶液浓度偏低的是
A.用量筒量取浓硫酸,读数时仰视刻度线
B.转移溶液时未洗涤烧杯
C.容量瓶用蒸馏水洗净后仍残留有蒸馏水
D.定容时俯视容量瓶的刻度线
E.定容摇匀后,发现液面低于刻度线,再加水至刻度线
(5)用锌与足量的该硫酸反应得到标况下11. 2L H2 ,则消耗锌的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】“84消毒液”能有效杀灭新冠病毒,某同学购买了一瓶84消毒液,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
(1)该“84消毒液”的物质的量浓度约为_______ mol·L-1。
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是_______(填字母)。
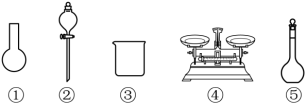
(3)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是_______(填字母)。
(4)一瓶上述“威露士”牌“84消毒液”能吸收空气中_______ L的CO2(标准状况)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用18mol·L-1的浓硫酸配制100mL物质的量浓度为0.9mol·L-1的稀硫酸用于增强84消毒液的消毒能力。
①需要用量筒量取_______ mL上述浓硫酸进行配制。
②为配制上述稀硫酸,除了量筒、烧杯、玻璃棒外,还缺少的玻璃仪器是_______ 、_______ 。
③在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是_______ (填序号)。
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出
f.未洗涤稀释浓硫酸的烧杯
| 84消毒液 有效成分NaClO 规格1000mL 质量分数25% 密度1.19g·cm-3 |
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是_______(填字母)。

| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.利用购买的商品NaClO来配制可能导致结果偏低 |
| D.需要称量NaClO固体的质量为142.8g |
| A.溶液中NaClO的摩尔质量 | B.溶液的浓度 |
| C.溶液中NaClO的物质的量 | D.溶液的密度 |
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用18mol·L-1的浓硫酸配制100mL物质的量浓度为0.9mol·L-1的稀硫酸用于增强84消毒液的消毒能力。
①需要用量筒量取
②为配制上述稀硫酸,除了量筒、烧杯、玻璃棒外,还缺少的玻璃仪器是
③在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出
f.未洗涤稀释浓硫酸的烧杯
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室需要配制0.50mol/LNaCl溶液480mL,现使用NaCl固体配制,按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、______ 、_______ 以及等质量的两片纸片。
(2)计算。配制该溶液需取NaCl晶体_______ g。
(3)配置过程。
①天平调零。
②称量过程中NaCl晶体应放于天平的_______ (填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
④溶解、冷却,该步实验中需要使用玻璃棒,目的是________ 。
⑤转移、洗涤。在转移时应使用_____ 引流,需要洗涤烧杯2-3次是为了______ 。
⑥定容、摇匀。
⑦将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度。
(4)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会______ (填“高”、“偏低”或“无影响”)。

(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、
(2)计算。配制该溶液需取NaCl晶体
(3)配置过程。
①天平调零。
②称量过程中NaCl晶体应放于天平的
③称量完毕,将药品倒入烧杯中。
④溶解、冷却,该步实验中需要使用玻璃棒,目的是
⑤转移、洗涤。在转移时应使用
⑥定容、摇匀。
⑦将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度。
(4)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶84消毒液。查阅相关资料和消毒液包装说明得到如图信息:
(1)该84消毒液NaClO物质的量浓度为_______ 。
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是_______ (填字母)。

A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.计算出需要称量的NaClO固体的质量约为88.7g
E.容量瓶用蒸馏水洗净后,须烘干后再使用
(3)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因_______ ,某消毒小组人员用 的浓硫酸配制500mL4.6 mol∙L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的浓硫酸配制500mL4.6 mol∙L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为_______ mL。
(4)在配制过程中,下列操作中能使所配溶液的浓度偏高的有_______ (填代号)。
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
| 84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】14.9% 【密度】  |
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是

A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.计算出需要称量的NaClO固体的质量约为88.7g
E.容量瓶用蒸馏水洗净后,须烘干后再使用
(3)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因
 的浓硫酸配制500mL4.6 mol∙L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的浓硫酸配制500mL4.6 mol∙L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为(4)在配制过程中,下列操作中能使所配溶液的浓度偏高的有
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室需要90mL1.0mol•L-1稀硫酸,现用质量分数为98%、密度为1.84g/mL的浓硫酸配制,根据实验事实需要配制情况回答下列问题。
(1)需量取浓硫酸的体积为___ mL。
(2)在如图所示仪器中,配制上述溶液肯定不需要的是___ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是____ 。
A. B.
B. C.
C. D.
D. E.
E.
(3)在容量瓶的使用方法中,下列操作不正确的是____ (多选题)
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)配制过程中,下列情况会使配制结果偏高的是(填序号)____ ,偏低的是___ 不影响的是____
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(1)需量取浓硫酸的体积为
(2)在如图所示仪器中,配制上述溶液肯定不需要的是
A.
 B.
B. C.
C. D.
D. E.
E.
(3)在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)配制过程中,下列情况会使配制结果偏高的是(填序号)
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】欲配制0.80 mol/L的NaOH溶液480 mL,现有以下仪器:
①烧杯 ②100 mL量筒 ③托盘天平(带砝码) ④玻璃棒 ⑤胶头滴管
(1)用托盘天平 称取氢氧化钠固体的质量为___ 克。
(2)使用容量瓶前必须进行的一步操作是___ 。
(3)配制溶液时,一般可以分为以下几个步骤,正确的操作顺序是:___ 。
A.用水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用天平称取所需的NaOH,然后放入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液而恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(4)下列哪些操作会引起所配溶液浓度偏大___ (填写字母)。
A.容量瓶底部有蒸馏水未干燥即用来配制溶液
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
①烧杯 ②100 mL量筒 ③托盘天平(带砝码) ④玻璃棒 ⑤胶头滴管
(1)用
(2)使用容量瓶前必须进行的一步操作是
(3)配制溶液时,一般可以分为以下几个步骤,正确的操作顺序是:
A.用水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用天平称取所需的NaOH,然后放入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液而恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(4)下列哪些操作会引起所配溶液浓度偏大
A.容量瓶底部有蒸馏水未干燥即用来配制溶液
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
您最近一年使用:0次



