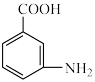
Fenton氧化技术因其方法简单、氧化电位高、无选择性氧化有机物、反应速率快等优点,广泛应用于污水处理工艺中,用于降解废水中的持久性有机污染物,其电化学工作原理及工作10min时,Fe2+、H2O2电极产生量(mmol/L)与电流强度关系如下图所示:
下列说法错误的是

下列说法错误的是
A.电解一段时间后, 电极附近 电极附近 减小 减小 |
B.羟基自由基产生原理为: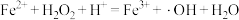 |
C.根据图b可判断合适的电流强度约为 |
D.若需处理 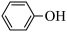 ,理论上 ,理论上 电极消耗标准状况下 电极消耗标准状况下 |
更新时间:2023-12-28 09:57:15
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.高温条件下,16.8gFe与足量水蒸气反应,生成H2分子数目为0.4NA |
| B.电解精炼铜时,阴极得到0.2NA个电子时,阳极粗铜质量一定减少6.4g |
C.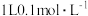 的 的 溶液中 溶液中 和 和 的离子数之和为0.1NA 的离子数之和为0.1NA |
| D.标准状况下,0.1molCl2被足量NaOH溶液完全吸收,转移的电子数目为0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是( )
| A.铁表面镀铜时,将铁与电源的正极相连,铜与电源的负极相连 |
| B.0.01 mol Cl2通入足量水中,转移电子的数目为6.02×1021 |
| C.反应3C(s)+CaO(s)===CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的ΔH>0 |
| D.加水稀释0.1 mol·L-1CH3COOH溶液,溶液中所有离子的浓度均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】对固体电解质体系的研究是电化学研究的重要领域之一、用离子交换膜H+/ 型 Nafion膜作电解质,在一定条件下实现了常温常压下电化学合成氨,原理如下图所示。下列说法不正确的是
型 Nafion膜作电解质,在一定条件下实现了常温常压下电化学合成氨,原理如下图所示。下列说法不正确的是
 型 Nafion膜作电解质,在一定条件下实现了常温常压下电化学合成氨,原理如下图所示。下列说法不正确的是
型 Nafion膜作电解质,在一定条件下实现了常温常压下电化学合成氨,原理如下图所示。下列说法不正确的是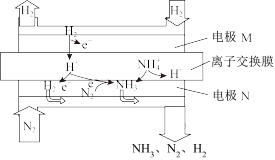
| A.电极M接电源的正极 |
B.离子交换膜中H+、 浓度均保持不变 浓度均保持不变 |
C.H+/ 型离子交换膜具有较高的传导质子能力 型离子交换膜具有较高的传导质子能力 |
| D.阴极的电极反应式:N2+6e-+6H+=2NH3,2H++2e-=H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高压直流电线路的瓷绝缘子经常出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,防护原理如图所示。下列说法错误的是( )
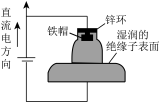

| A.断电时,牺牲阳极保护法使铁帽不被腐蚀 |
| B.通电时,阳极上的电极反应为Zn-2e-=Zn2+ |
| C.断电时,锌环上的电极反应为Zn-2e-=Zn2+ |
| D.铁帽上加铜环也能防止铁被腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用如图电化学装置可以处理含 的碱性废水,同时还可以淡化海水。下列说法错误的是
的碱性废水,同时还可以淡化海水。下列说法错误的是
 的碱性废水,同时还可以淡化海水。下列说法错误的是
的碱性废水,同时还可以淡化海水。下列说法错误的是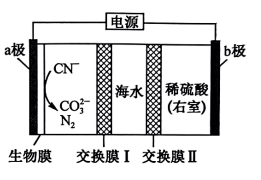
A.a极电极反应式为 |
B.电解池工作一段时间后,右室溶液中的 增大 增大 |
| C.交换膜I为阴离子交换膜,交换膜II为阳离子交换膜 |
D.若有11.2L 生成时,理论上可除去NaCl的质量为292.5g 生成时,理论上可除去NaCl的质量为292.5g |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】处理烟气中的SO2可以采用碱吸—电解法,其流程如图1所示。其中过程Ⅱ的模拟装置如图2所示。下列有关叙述正确的是
 |  |
图1 | 图2 |
| A.膜1为阳离子交换膜,膜2为阴离子交换膜 |
| B.a极的电极反应式为2H2O-4e-=4H++O2↑ |
| C.若用铅酸蓄电池为电源,b极与铅电极相连 |
| D.若收集22.4 L的P,则转移电子的物质的量为2 mol |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
解题方法
【推荐1】利用富磺酸盐修饰锌碘二次电池,总反应为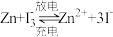 ,其装置如下。
,其装置如下。
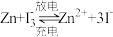 ,其装置如下。
,其装置如下。
| A.a为阳极 |
B. 向b极移动的原因是电场作用 向b极移动的原因是电场作用 |
C.理论上消耗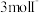 转移电子数目为 转移电子数目为 |
| D.富磺酸盐的作用是减缓b电极的腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上常用三种方法制氢。(1)绿氢:电解水制氢气(添加NaOH溶液或稀硫酸增强导电性);(2)蓝氢:利用天然气在高温下与水蒸气反应[CH4(g)+H2O(g) CO(g)+3H2(g)];(3)灰氢:利用焦炭在高温下与水蒸气反应[C(s)+H2O(g)
CO(g)+3H2(g)];(3)灰氢:利用焦炭在高温下与水蒸气反应[C(s)+H2O(g) CO(g)+H2(g)]。NA伏加德罗常数的值。下列说法正确的是
CO(g)+H2(g)]。NA伏加德罗常数的值。下列说法正确的是
 CO(g)+3H2(g)];(3)灰氢:利用焦炭在高温下与水蒸气反应[C(s)+H2O(g)
CO(g)+3H2(g)];(3)灰氢:利用焦炭在高温下与水蒸气反应[C(s)+H2O(g) CO(g)+H2(g)]。NA伏加德罗常数的值。下列说法正确的是
CO(g)+H2(g)]。NA伏加德罗常数的值。下列说法正确的是| A.制备蓝氢时,16gCH4与足量水蒸气反应可制备H2分子数为3NA |
| B.在常温常压下,制备44.8L“灰氢”时断裂极性键数为4NA |
| C.北京冬奥会利用“绿电”制绿氢,阳极产生amol气体时转移电子数为4aNA |
| D.制绿氢时,1L0.01mol·L-1NaOH溶液中水电离的OH-数为0.01NA |
您最近一年使用:0次


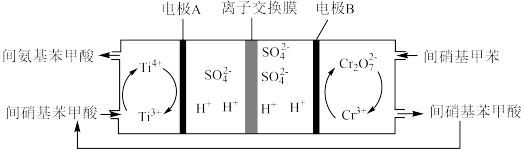
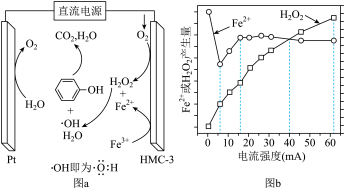
 )为原料,采用间接成对电解合成间氨基苯甲酸
)为原料,采用间接成对电解合成间氨基苯甲酸 装置如图所示(离子交换膜只允许离子通过),下列说法中错误的是
装置如图所示(离子交换膜只允许离子通过),下列说法中错误的是