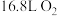盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用向两侧电极分别通入NO和H2,以盐酸为电解质来进行制备,其电池装置(图1)和含Fe的催化电极反应机理(图2)如图。不考虑溶液体积的变化,下列说法正确的是

| A.电池工作时,含Fe的催化电极为正极,发生还原反应 |
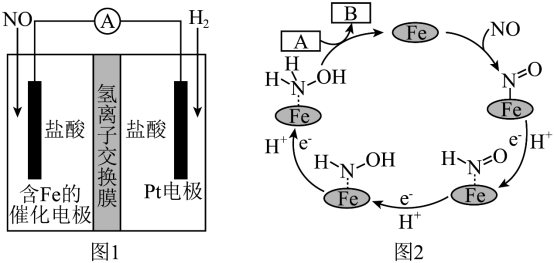
B.图2中,A为H+和e-,B为 |
| C.电池工作时,每消耗标况下2.24LNO,左室溶液质量增加3.0g |
| D.电池工作一段时间后,正、负极区溶液的pH均下降 |
23-24高三上·江西南昌·期中 查看更多[3]
江西省南昌市2023-2024学年高三上学期11月期中三校联考化学试题(已下线)寒假收官卷02-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
更新时间:2023-12-26 11:36:32
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。碱性锌锰电池与锌锰干电池在反应过程中,锌均会被逐渐消耗,不可重复使用。以氢氧化钾溶液为电解质溶液的碱性锌锰电池,电池总反应式为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.电池工作时,锌电极附近的溶液碱性增强 |
| B.电池工作时,外电路中每通过1mol电子,消耗65gZn |
C.电池正极的电极反应式为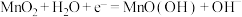 |
| D.碱性锌锰电池为二次电池 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】阿伏加德罗常数是联系宏观和微观的桥梁,用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.在锌、铜和稀硫酸形成的原电池装置中,负极消耗6.5g,则溶液中有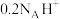 向锌片移动 向锌片移动 |
B.常温下,5.6g铁片与足量浓硝酸反应转移的电子数目为 |
C.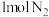 与足量 与足量 充分反应,转移的电子数为 充分反应,转移的电子数为 |
D.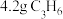 和 和 的混合气体中含有极性共价键数目为 的混合气体中含有极性共价键数目为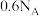 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一种新型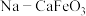 可充电电池,其工作原理如图所示.下列说法正确的是
可充电电池,其工作原理如图所示.下列说法正确的是
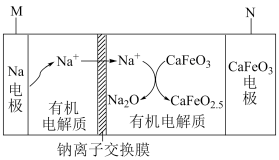
 可充电电池,其工作原理如图所示.下列说法正确的是
可充电电池,其工作原理如图所示.下列说法正确的是
A.放电时,钠电极电势高于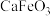 电极 电极 |
| B.充电时,M应与电源的正极相连接 |
C.放电时,每生成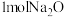 ,转移电子数为 ,转移电子数为 |
D.电极材料中,单位质量放出的电能: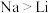 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】我国科学家设计了水/有机混合高能锂硫电池,其工作原理如图所示。下列说法正确的是
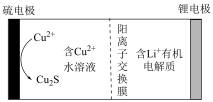
| A.硫电极为负极 |
B. 通过阳离子交换膜向锂电极方向迁移 通过阳离子交换膜向锂电极方向迁移 |
C.硫电极上发生的反应为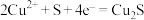 |
D.理论上,每消耗1mol  ,同时消耗2 mol ,同时消耗2 mol  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】镁-空气电池的工作原理如图所示,电池反应方程式为:2Mg+O2+2H2O=2Mg(OH)2.有关该电池的说法正确的是
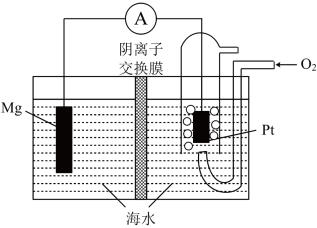

| A.通入氧气的电极为负极 |
| B.电池工作时,溶液中Na+由负极移向正极 |
| C.负极的电极反应为Mg-2e-+2OH-=Mg(OH)2 |
| D.当参加反应的O2为0.01mol时,流经电解液的电子为0.04 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以Mg片和Al片为电极,并用导线连接,同时插入NaOH溶液中,下列说法正确的是
| A.Al片上有气泡产生 |
| B.Mg片作负极,电极反应:Mg-2e-=Mg2+ |
| C.电子从Mg电极沿导线流向Al电极 |
D.Al片作负极,电极反应:Al+4OH--3e-=AlO +2H2O +2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在 存在下利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如图所示。下列说法正确的是( )
存在下利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如图所示。下列说法正确的是( )

 存在下利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如图所示。下列说法正确的是( )
存在下利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如图所示。下列说法正确的是( )
| A.M极为电源负极,苯酚被氧化 |
B.工作一段时间后 浓度增大 浓度增大 |
C.M极的电极反应为  |
D.处理 时,有 时,有 从阴离子交换膜左侧向右侧移动 从阴离子交换膜左侧向右侧移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
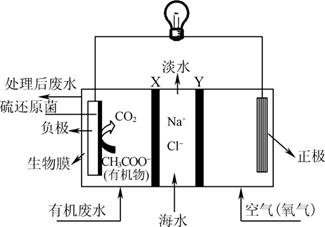
 等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
| A.该装置可以在高温下工作 |
| B.X为阳离子交换膜,Y为阴离子交换膜 |
C.负极反应为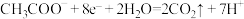 |
D.当负极产生 时,海水(不考虑 时,海水(不考虑 以外的溶质)理论上除盐58.5g 以外的溶质)理论上除盐58.5g |
您最近一年使用:0次

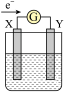
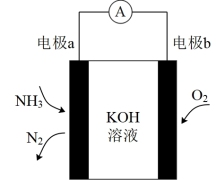
 的含量,其工作原理示意图如下。下列说法错误的是
的含量,其工作原理示意图如下。下列说法错误的是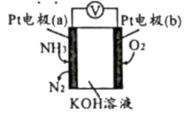
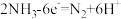
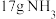 时,理论上电极b消耗标准状况下
时,理论上电极b消耗标准状况下