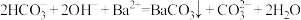下列反应的离子方程式书写正确的是
| A.用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.向CaCl2溶液中通入CO2:Ca2++CO2+H2O=CaCO3↓+2H+ |
| C.向FeI2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
D.澄清石灰水与过量NaHCO3溶液反应:2 +Ca2++2OH-=CaCO3↓+2H2O+ +Ca2++2OH-=CaCO3↓+2H2O+ |
更新时间:2023-12-28 21:07:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列解释实验事实的方程式正确的是
A. 溶液滴加氨水产生白色胶状沉淀: 溶液滴加氨水产生白色胶状沉淀: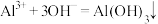 |
B. 时,测得纯水中 时,测得纯水中 : :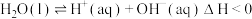 |
C.除去 中少量的 中少量的 的方法是加入足量饱和的 的方法是加入足量饱和的 溶液中充分搅拌、过滤、洗涤: 溶液中充分搅拌、过滤、洗涤: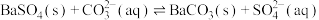 |
D.碳酸钠溶液滴入酚酞变红: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写正确的是
| A.氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
| B.将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-=2Fe2++S↓ |
| C.次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| D.向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2+ + HCO3—+ OH-=CaCO3↓+H2O |
您最近一年使用:0次
【推荐1】我国科学家设计如下图所示“电子转移链”过程,实现了低温条件下氧化 高效制
高效制 。下列说法正确的是
。下列说法正确的是

 高效制
高效制 。下列说法正确的是
。下列说法正确的是
A. 的电子通过四个反应最终传递给 的电子通过四个反应最终传递给 |
B.理论上, 不能被 不能被 直接氧化 直接氧化 |
C.参加Ⅲ、Ⅳ反应的 和 和 的物质的量之比为1:2 的物质的量之比为1:2 |
D.可通过 的水解制取 的水解制取 |
您最近一年使用:0次
【推荐2】已知有如下反应:①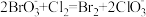 ②
②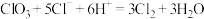 ③
③ 根据上述反应,判断下列结论中错误的是
根据上述反应,判断下列结论中错误的是
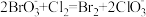 ②
②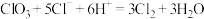 ③
③ 根据上述反应,判断下列结论中错误的是
根据上述反应,判断下列结论中错误的是A. 在反应①中作还原剂 在反应①中作还原剂 |
B. 在反应②中既是氧化产物又是还原产物 在反应②中既是氧化产物又是还原产物 |
C.氧化性的由强到弱的顺序: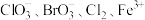 |
D.溶液中可发生反应: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NA是阿伏加德罗常数的值,下列说法正确的是
A.1 molNH4NO3完全溶于稀氨水中,溶液呈中性,溶液中 的数目为NA 的数目为NA |
| B.将Cl2通入FeBr2溶液中,有1 molBr2生成时,转移的电子数为2NA |
| C.7.8 g苯含σ键的数目为0.6NA |
| D.有铁粉参加的反应若生成3 molFe2+,则转移电子数一定为6NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列“解释或结论”与“实验操作及现象”不相符 的一组是
| 序号 | 实验操作及现象 | 解释或结论 |
| A | 将氯水滴入KI-淀粉溶液中,溶液变成蓝色 | Cl2的氧化性强于I2 |
| B | 将打磨后的镁条放入盛有稀盐酸的试管中,用手触摸试管外壁感觉变热 | 镁条与稀盐酸反应是放热反应 |
| C | 某钠盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该盐一定是Na2CO3 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 不能确定原溶液中含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验方案设计、现象及结论均正确的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 检验铁锈中是否含有Fe2+ | 将表面生锈的铁粉用过量稀硫酸溶解,在所得溶液中滴加KMnO4溶液,KMnO4溶液褪色 | 铁锈中含有Fe2+ |
| B | 验证卤素单质的氧化性强弱 | 向NaBr溶液中加入过量氯水,溶液呈黄色,再加KI-淀粉溶液,溶液变蓝色 | 说明氧化性: Cl2>Br2>I2 |
| C | 中和热的测定 | 在利用标准HCl滴定未知浓度NaOH时,用温度传感器测定锥形瓶内溶液的起始温度和最高温度,并计算得放出热量为Q kJ,消耗HCl的物质的量为n mol | 中和热为: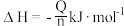 |
| D | 验证不同微粒与Cu2+的配位能力 | 向稀CuCl2溶液中加入适量的NaCl固体,溶液颜色由蓝色变为绿色 | [Cu(H2O)4]2+转化为CuCl ,说明Cl-与Cu2+的配位能力比H2O强 ,说明Cl-与Cu2+的配位能力比H2O强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 :
: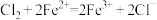


 溶液滴入
溶液滴入 溶液中:
溶液中: