肼(N2H4)是重要的化工原料,能与水、乙醇等混溶;它是一种二元弱碱,在水中的电离方式与氨相似,室温下电离常数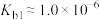 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。
(1)写出N元素在元素周期表中的位置___________ 。
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式___________ 。
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步: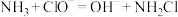
①写出第二步反应的离子方程式___________ 。
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)___________ 。
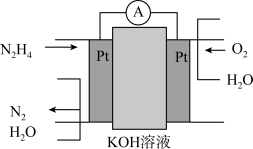
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________ 。
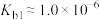 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。(1)写出N元素在元素周期表中的位置
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步:
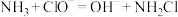
①写出第二步反应的离子方程式
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为

更新时间:2024-01-01 15:33:18
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】生活中化学无处不在,家庭厨卫用品中有许多中学化学常见的物质。请你回答下列问题。
(1)若不慎将食盐洒在天然气灶的火焰上,观察到的现象是____ 。
(2)碳酸氢钠可以作为治疗胃酸(主要成分为盐酸)过多的药物的主要成分,其反应原理的离子方程式为____ 。
(3)使用漂白粉[含Ca(ClO)2]时,按一定比例与水混合,并在空气中放置一段时间,使Ca(ClO)2与H2O及空气中的CO2充分反应,目的是得到具有漂白性的____ (填物质名称),请写出反应的化学方程式:____ 。
| 名称 | 食盐 | 碱面 | 发酵粉 | 洁厕灵 | 漂白粉 |
| 主要成分 | NaCl | Na2CO3 | NaHCO3 | HCl | Ca(ClO)2 |
(1)若不慎将食盐洒在天然气灶的火焰上,观察到的现象是
(2)碳酸氢钠可以作为治疗胃酸(主要成分为盐酸)过多的药物的主要成分,其反应原理的离子方程式为
(3)使用漂白粉[含Ca(ClO)2]时,按一定比例与水混合,并在空气中放置一段时间,使Ca(ClO)2与H2O及空气中的CO2充分反应,目的是得到具有漂白性的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知 与硫的氧化物、氮的氧化物反应可以生成
与硫的氧化物、氮的氧化物反应可以生成 、NOCl、
、NOCl、 等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于
等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于 等有机溶剂。
等有机溶剂。
(1)NOCl中N元素的化合价为_______ ,N、O、Cl三种元素原子半径由大到小的顺序为_______ 。
(2)实验室制取的NOCl中常含有 ,除去
,除去 的方法为
的方法为_______ 。
(3)NOCl遇水生成一种氮的氧化物(该氧化物遇空气变红棕色),且只有一种元素的化合价发生改变,写出该反应的化学方程式:_______ 。
(4)NOCl与 同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:
同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:_______ 。反应中消耗1mol NOCl则转移电子的物质的量为_______ 。
(5) 可作为晶体的除水剂(反应生成两种酸性气体),写出
可作为晶体的除水剂(反应生成两种酸性气体),写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
 与硫的氧化物、氮的氧化物反应可以生成
与硫的氧化物、氮的氧化物反应可以生成 、NOCl、
、NOCl、 等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于
等化合物。NOCl常温下是黄色气体,具有强氧化性,遇水分解,不溶于 等有机溶剂。
等有机溶剂。(1)NOCl中N元素的化合价为
(2)实验室制取的NOCl中常含有
 ,除去
,除去 的方法为
的方法为(3)NOCl遇水生成一种氮的氧化物(该氧化物遇空气变红棕色),且只有一种元素的化合价发生改变,写出该反应的化学方程式:
(4)NOCl与
 同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:
同时通入水中可生成一种无污染的气体,写出该反应的离子方程式:(5)
 可作为晶体的除水剂(反应生成两种酸性气体),写出
可作为晶体的除水剂(反应生成两种酸性气体),写出 与
与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】H1N1病毒是一种病毒。研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将H1N1病毒杀灭。氯气与氢氧化钙溶液充分反应,得到以次氯酸钙[Ca(ClO)2]为主要成分的漂粉精,其稳定性比漂白粉高。将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为______________________________ 。另取少许上层清液,先滴加适量的硝酸酸化,再滴加________ (填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为____________________________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】若溶液中同时含有SO 和Cl-,如何设计实验检验Cl-的存在
和Cl-,如何设计实验检验Cl-的存在 _____ ?
 和Cl-,如何设计实验检验Cl-的存在
和Cl-,如何设计实验检验Cl-的存在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。

明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是_______ 价。CrO 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于_______ (填“酸”“碱”“盐”或“氧化物”)。
(2)区分明胶的水溶液和K2SO4溶液的方法是_______ 。分离提纯明胶的水溶液和K2SO4溶液的混合物的方法是_______ 。
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10mL明胶的水溶液与5mLNaCl溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明Cl-能够透过半透膜:_______ 。

明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(2)区分明胶的水溶液和K2SO4溶液的方法是
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10mL明胶的水溶液与5mLNaCl溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明Cl-能够透过半透膜:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】锰锂电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
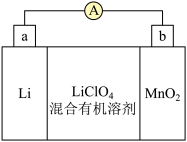
(1)外电路的电流方向是由____ 极流向___ 极(填字母)
(2)电池正极反应式___________ 。
(3)MnO2可与KOH和KClO3在高温下反应,生成反应的化学方程式为___________ 。

(1)外电路的电流方向是由
(2)电池正极反应式
(3)MnO2可与KOH和KClO3在高温下反应,生成反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:请回答下列问题:
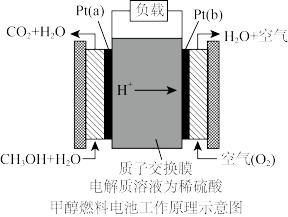
(1)Pt(a)电极是电池的_______ 极,电极反应式为:_______ ;
(2)Pt(b)电极发生_______ 反应(填“氧化”或“还原”),电极反应式为:_______ 。
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有_______ mol。在用石墨作电极时,用其电解饱和食盐水,则阳极生成的氯气在标况下的体积约为_______ L。

(1)Pt(a)电极是电池的
(2)Pt(b)电极发生
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】燃料电池在日常生活和科学研究中越来越得到广泛使用。回答下列问题:
(1)镁—空气燃料电池是一种新型的燃料电池,可应用于电动汽车。其工作原理如图所示。
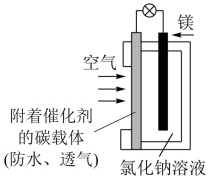
①通入空气的电极是_______ (填“正”或“负”)极。
②镁电极发生_______ (填“氧化”或“还原”)反应。
③电池总反应方程式为_______ 。
(2)航天技术中使用的氢氧燃料电池具有高能、轻便和无污染等优点。氢氧燃料电池有酸式和碱式两种。
①酸式氢氧燃料电池的电解质溶液是稀硫酸,负极为通_______ (填“ ”或“
”或“ ”)的多孔铂电极;其正极反应式为:
”)的多孔铂电极;其正极反应式为:_______ 。
②碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应式为_______ 。
(1)镁—空气燃料电池是一种新型的燃料电池,可应用于电动汽车。其工作原理如图所示。

①通入空气的电极是
②镁电极发生
③电池总反应方程式为
(2)航天技术中使用的氢氧燃料电池具有高能、轻便和无污染等优点。氢氧燃料电池有酸式和碱式两种。
①酸式氢氧燃料电池的电解质溶液是稀硫酸,负极为通
 ”或“
”或“ ”)的多孔铂电极;其正极反应式为:
”)的多孔铂电极;其正极反应式为:②碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题)
(1) ④⑤⑥的原子半径由大到小的顺序为______
(2) ②③⑦的最高价含氧酸的酸性由强到弱的顺序为______
(3) ⑦⑧⑨的第一电离能由小到大的顺序为______
(4)比较④和⑨的氢化物的稳定性大小______ ,沸点高低______
(5)写出元素⑩的+1价含氧酸的结构式______
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
(1) ④⑤⑥的原子半径由大到小的顺序为
(2) ②③⑦的最高价含氧酸的酸性由强到弱的顺序为
(3) ⑦⑧⑨的第一电离能由小到大的顺序为
(4)比较④和⑨的氢化物的稳定性大小
(5)写出元素⑩的+1价含氧酸的结构式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】元素周期表(律)在学习、 研究和生产实践中有很重要的作用。图表为元素周期表的一部分,回答下列问题
(1)⑦的元素名称为______________ 。
(2)元素①~⑧ 中金属性最强的是____________ ( 填元素符号)。
(3)比较②和⑤两种元素原子半径的大小:②______ ⑤(填“ >”或“< ”)。
(4)⑨ 的原子序数是_________ 。
(5)元素④~⑧中,最高价氧化物属于两性氧化物的是________ (填元素符号)。
族 周期 | ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ② | ③ | |||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | …… | ⑨ |
(1)⑦的元素名称为
(2)元素①~⑧ 中金属性最强的是
(3)比较②和⑤两种元素原子半径的大小:②
(4)⑨ 的原子序数是
(5)元素④~⑧中,最高价氧化物属于两性氧化物的是
您最近一年使用:0次



