现有下列八种物质:①盐酸;②小苏打;③FeSO4•7H2O;④二氧化碳;⑤蔗糖;⑥氢氧化铁胶体;⑦氨水;⑧NaHSO4固体。
(1)上述八种物质中,属于电解质的是_______ (填序号,下同);属于非电解质的是_______ 。
(2)向⑥中滴加①产生的现象为__________________________ 。
(3)将少量②的溶液与澄清石灰水混合,发生反应的离子方程式为____________________ 。
(1)上述八种物质中,属于电解质的是
(2)向⑥中滴加①产生的现象为
(3)将少量②的溶液与澄清石灰水混合,发生反应的离子方程式为
更新时间:2024-01-11 19:57:35
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.现有下列状态的物质:
①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖
其中属于电解质的是___________ ,属于强电解质的是___________ ,能导电的是___________ 。
Ⅱ.胶体是一种常见的分散系。
①向煮沸的蒸馏水中逐滴加入___________ 溶液,继续煮沸至___________ ,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体的化学方程式为___________ 。
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于___________ (填离子符号)的作用,使胶粒形成了沉淀,这个过程叫作___________ 。
③区分胶体和溶液常利用的性质叫作___________ 。
Ⅲ.①用FeCl3溶液刻蚀铜箔制造电路板,发生反应的离子方程式为_____________________ 。
②Cu是一种不活泼金属,但能与稀硝酸反应,发生的离子方程式为___________ 。
③NaHCO3不稳定,请写出其在受热条件下化学反应方程式__________________ 。
①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖
其中属于电解质的是
Ⅱ.胶体是一种常见的分散系。
①向煮沸的蒸馏水中逐滴加入
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于
③区分胶体和溶液常利用的性质叫作
Ⅲ.①用FeCl3溶液刻蚀铜箔制造电路板,发生反应的离子方程式为
②Cu是一种不活泼金属,但能与稀硝酸反应,发生的离子方程式为
③NaHCO3不稳定,请写出其在受热条件下化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“分类”的思想在化学学习及化学学科发展中起着重要作用。现有下列物质:
① 固体 ②熔融
固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤
③淀粉溶液 ④液态氯化氢 ⑤ 溶液 ⑥
溶液 ⑥ ⑦金属铜 ⑧
⑦金属铜 ⑧ ⑨酒精 ⑩
⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)②熔融 能导电,其电离方程式为
能导电,其电离方程式为___________ 。
(3)③淀粉溶液,⑤ 溶液二者如果混合,可采用
溶液二者如果混合,可采用___________ 方法分离。
(4)⑧ 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为___________ ,每当有 参与反应,转移电子数为
参与反应,转移电子数为___________ (设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
(5)已知⑨ (亚磷酸)与足量
(亚磷酸)与足量 溶液反应的化学方程式为
溶液反应的化学方程式为 ,
, 属于
属于___________ (填“正盐”或“酸式盐”)。
①
 固体 ②熔融
固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤
③淀粉溶液 ④液态氯化氢 ⑤ 溶液 ⑥
溶液 ⑥ ⑦金属铜 ⑧
⑦金属铜 ⑧ ⑨酒精 ⑩
⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是
(2)②熔融
 能导电,其电离方程式为
能导电,其电离方程式为(3)③淀粉溶液,⑤
 溶液二者如果混合,可采用
溶液二者如果混合,可采用(4)⑧
 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为 参与反应,转移电子数为
参与反应,转移电子数为 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。(5)已知⑨
 (亚磷酸)与足量
(亚磷酸)与足量 溶液反应的化学方程式为
溶液反应的化学方程式为 ,
, 属于
属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图为化学“五元环”图案,在图案上分别写了 、
、 、
、 、
、 、
、 五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:

(1)分类依据A、B、D中可总结为“两种物质都是盐”的是_______ (填代号)。
(2)写出 的电离方程式:
的电离方程式:_______ 。
(3)在烧杯中加入20mL蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和 溶液,继续加热至呈红褐色后停止加热。氢氧化铁胶体与氯化铁溶液的本质区别
溶液,继续加热至呈红褐色后停止加热。氢氧化铁胶体与氯化铁溶液的本质区别_______ 。
(4)高铁酸钠( )(铁为+6价)是一种新型净水剂,可用
)(铁为+6价)是一种新型净水剂,可用 通过下述途径制取:
通过下述途径制取: (未配平)
(未配平)
①配平方程式:_______ 。
_______ _______NaOH+_______NaClO→_______
_______NaOH+_______NaClO→_______ _______NaCl+_______
_______NaCl+_______
②该反应中氧化剂是_______ ,氧化产物为_______ 。
 、
、 、
、 、
、 、
、 五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
(1)分类依据A、B、D中可总结为“两种物质都是盐”的是
(2)写出
 的电离方程式:
的电离方程式:(3)在烧杯中加入20mL蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和
 溶液,继续加热至呈红褐色后停止加热。氢氧化铁胶体与氯化铁溶液的本质区别
溶液,继续加热至呈红褐色后停止加热。氢氧化铁胶体与氯化铁溶液的本质区别(4)高铁酸钠(
 )(铁为+6价)是一种新型净水剂,可用
)(铁为+6价)是一种新型净水剂,可用 通过下述途径制取:
通过下述途径制取: (未配平)
(未配平)①配平方程式:
_______
 _______NaOH+_______NaClO→_______
_______NaOH+_______NaClO→_______ _______NaCl+_______
_______NaCl+_______
②该反应中氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质,是认识电解质的性质的前提:以下有①~⑩种物质:①H2 ②石墨 ③ HCl ④CO2 ⑤NaHCO3 ⑥熔融Ba(OH)2 ⑦氯水 ⑧稀硫酸 ⑨熔融硫酸铁 ⑩碳酸钙,请回答下列问题:
(1)上述状态下可导电的电解质的是_______ ;(填序号下同),属于非电解质的是________ ;氯水中具有漂白性的物质是________ (写化学式)。
(2)小苏打的水溶液能导电的原因是________ (用化学用语回答)。
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是_______ 。常用澄清石灰水检验CO2气体,反应的离子方程式是_______ 。
(4)40.0g硫酸铁固体溶于水配成250mL溶液, 的物质的量浓度为
的物质的量浓度为________ 。
(5)若将标准情况下aLHCl气体熔于1L水中,所得溶液稀盐酸的密度为dg/mL,则此时所得盐酸的物质的量浓度为______ mol·L-1。
(1)上述状态下可导电的电解质的是
(2)小苏打的水溶液能导电的原因是
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是
(4)40.0g硫酸铁固体溶于水配成250mL溶液,
 的物质的量浓度为
的物质的量浓度为(5)若将标准情况下aLHCl气体熔于1L水中,所得溶液稀盐酸的密度为dg/mL,则此时所得盐酸的物质的量浓度为______ mol·L-1。
A.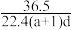 | B.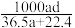 | C.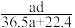 | D.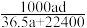 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有下列物质:①NaCl固体 ②盐酸 ③ 溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(
溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇( ) ⑧液态硫酸 ⑨熔融态
) ⑧液态硫酸 ⑨熔融态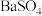 ⑩液态
⑩液态 。请回答下列问题(用序号):
。请回答下列问题(用序号):
(1)属于电解质的是_______ ;属于非电解质的是_______ 。
(2)上述状态下可导电的物质是_______ ;
(3) 是一种酸式盐,可用作清洁剂、防腐剂等。
是一种酸式盐,可用作清洁剂、防腐剂等。
① 溶于水时的电离方程式
溶于水时的电离方程式_______ 。
②少量 与
与 溶液混合,该反应的离子方程式为
溶液混合,该反应的离子方程式为_______ 。
③写出澄清石灰水与过量二氧化碳反应的离子方程式:_______ 。
 溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(
溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇( ) ⑧液态硫酸 ⑨熔融态
) ⑧液态硫酸 ⑨熔融态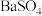 ⑩液态
⑩液态 。请回答下列问题(用序号):
。请回答下列问题(用序号):(1)属于电解质的是
(2)上述状态下可导电的物质是
(3)
 是一种酸式盐,可用作清洁剂、防腐剂等。
是一种酸式盐,可用作清洁剂、防腐剂等。①
 溶于水时的电离方程式
溶于水时的电离方程式②少量
 与
与 溶液混合,该反应的离子方程式为
溶液混合,该反应的离子方程式为③写出澄清石灰水与过量二氧化碳反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空:
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水,
a.其中能导电的是(填编号,下同):_______ ;属于电解质的是_______ ;属于非电解质的是:_______ 。
b.请写出③和⑨反应的离子方程式_______
c.过量的①和少量的④在水溶液中的离子方程式为_______
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下,把方程式补充完整并配平:______
_______ClO-+_______Fe3++_______=_______ _______Cl-+_______H2O
_______Cl-+_______H2O
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水,
a.其中能导电的是(填编号,下同):
b.请写出③和⑨反应的离子方程式
c.过量的①和少量的④在水溶液中的离子方程式为
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下,把方程式补充完整并配平:
_______ClO-+_______Fe3++_______=_______
 _______Cl-+_______H2O
_______Cl-+_______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.已知制备Cl2的方法可以为:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O。
(1)用双线桥法表示该反应电子转移的方向和数目___________ 。
(2)反应中氧化剂是___________ ,氧化产物是___________ ,被氧化与未被氧化的的HCl质量之比为___________ ;
(3)HCl在上述反应中显示出来的性质是___________;
(4)若有112L(标准状况)Cl2生成,反应中转移电子的数目为___________ 。
Ⅱ.制取新型净水剂高铁酸钠( )原理为:
)原理为:
___________ ___________
___________ ___________ —___________
___________ —___________ ___________
___________ ___________(缺项处填
___________(缺项处填 、
、 或
或 )
)
(5)请配平该化学方程式___________ 。
Ⅲ.NaHCO3是生活中常见的物质,请回答下列问题:
(6)写出NaHCO3在水溶液中的电离方程式:___________ 。
(7)NaHCO3属于“酸”、“碱”、“盐”中的___________ 。
(8)写出NaHCO3溶液与NaOH溶液反应的离子方程式___________ 。
(9)Na2CO3固体中含有少量的NaHCO3杂质,除去杂质发生反应的化学方程式为___________ 。
(1)用双线桥法表示该反应电子转移的方向和数目
(2)反应中氧化剂是
(3)HCl在上述反应中显示出来的性质是___________;
| A.氧化性 | B.还原性 | C.酸性 | D.挥发性 |
Ⅱ.制取新型净水剂高铁酸钠(
 )原理为:
)原理为:___________
 ___________
___________ ___________ —___________
___________ —___________ ___________
___________ ___________(缺项处填
___________(缺项处填 、
、 或
或 )
)(5)请配平该化学方程式
Ⅲ.NaHCO3是生活中常见的物质,请回答下列问题:
(6)写出NaHCO3在水溶液中的电离方程式:
(7)NaHCO3属于“酸”、“碱”、“盐”中的
(8)写出NaHCO3溶液与NaOH溶液反应的离子方程式
(9)Na2CO3固体中含有少量的NaHCO3杂质,除去杂质发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空:
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是________ .
(2)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是________ 。
(3)下列三个氧化还原反应中,氧化性最强的物质是______ 。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还应用上述反应中的________ 作氧化剂。
(4)取15 mL Ba(OH)2溶液注入锥形瓶中,然后逐滴加入NaHCO3溶液,当Ba2+恰好完全沉淀时,溶液中的溶质是________ ,发生反应的离子方程式为________________________ 。继续滴加NaHCO3溶液发生反应的离子方程式为___________ 。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还应用上述反应中的
(4)取15 mL Ba(OH)2溶液注入锥形瓶中,然后逐滴加入NaHCO3溶液,当Ba2+恰好完全沉淀时,溶液中的溶质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在一个用铝制的易拉罐内充满CO2气体,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口。经过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起来。
(1)罐壁内凹而瘪的原因是_________________________________________ ,
离子方程式可能为_______________________________________________ ;
(2)罐再鼓起的原因是________________________________________ ,
离子方程式可能为_______________________________________________ 。
(1)罐壁内凹而瘪的原因是
离子方程式可能为
(2)罐再鼓起的原因是
离子方程式可能为
您最近一年使用:0次



