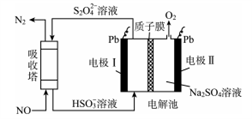
用一种具有“卯榫”结构的双极膜组装电解池(如图),可实现大电流催化电解 溶液制氨。工作时,
溶液制氨。工作时, 在双极膜界面处被催化解离成
在双极膜界面处被催化解离成 和
和 ,有利于电解反应顺利进行。下列说法不正确的是
,有利于电解反应顺利进行。下列说法不正确的是
 溶液制氨。工作时,
溶液制氨。工作时, 在双极膜界面处被催化解离成
在双极膜界面处被催化解离成 和
和 ,有利于电解反应顺利进行。下列说法不正确的是
,有利于电解反应顺利进行。下列说法不正确的是
A.“卯榫”结构的双极膜中的 移向电极a 移向电极a |
B.b电极的电极反应式为 |
| C.电解过程中,阳极室中KOH的物质的量浓度增大 |
D.每生成 ,双极膜处有16mol的 ,双极膜处有16mol的 解离 解离 |
2023·四川南充·一模 查看更多[3]
河南省信阳高级中学2023-2024学年高三上学期2月月考理综试题-高中化学(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届四川省南充高级中学高三上学期一模理综试题
更新时间:2024-01-10 08:53:05
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】高铁酸钠(Na2FeO4)是一种新型绿色水处理剂。 工业上可用电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是


| A.阳极电极反应式:Fe-6e- +8OH-=FeO42- +4H2O |
| B.甲溶液可循环利用 |
| C.离子交换膜a是阴离子交换膜 |
| D.当电路中通过2mol电子的电量时,会有1molH2生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】废旧锌锰电池处理后的废料[含MnO2、MnOOH、Zn(OH)2、 Fe等]制备Zn和MnO2的一种工艺流程如下:
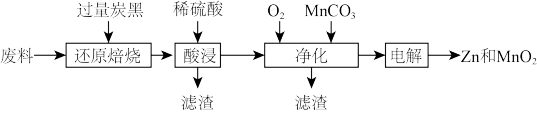
已知:Mn的金属活动性强于Fe,Mn2+在pH大于5.5时易被氧化。
下列说法不正确的是

已知:Mn的金属活动性强于Fe,Mn2+在pH大于5.5时易被氧化。
下列说法不正确的是
| A.“还原焙烧”时Mn元素被还原 |
| B.“酸浸” 过程中适当加热,主要目的是加快浸取速率 |
| C.“净化”时MnCO3的作用是调节溶液的pH,使Fe3+形成Fe(OH)3沉淀而除去 |
| D.“电解”时阳极反应式为Mn2+-2e-+4OH-=MnO2+2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列有关实验原理、装置、操作的描述中正确的是
| A | B | C | D |
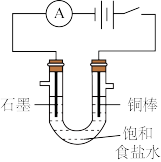 | 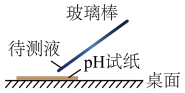 | 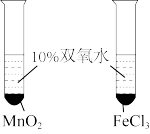 | 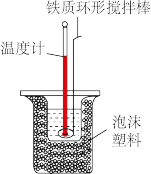 |
| 利用电解法制氢气和氯气 | pH试纸的测定 | 研究不同催化剂对反应速率的影响 | 反应热的测定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】第三代混合动力车目前一般使用镍氢电池(M表示储氢合金;汽车在刹车或下坡时,电池处于充电状态)。镍氢电池充放电原理的示意图如下:
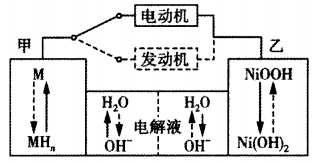
其总反应式为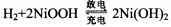 。根据所给信息判断,下列说法错误的是
。根据所给信息判断,下列说法错误的是

其总反应式为
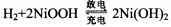 。根据所给信息判断,下列说法错误的是
。根据所给信息判断,下列说法错误的是| A.混合动力汽车上坡或加速时,乙电极的电极反应式为:NiOOH+H2O+eˉ==Ni(OH)2+OHˉ |
| B.混合动力汽车上坡或加速时,电解液中OHˉ向甲电极移动 |
| C.混合动力汽车下坡或刹车时,甲电极周围溶液的pH减小 |
| D.混合动力汽车下坡或刹车时,电流的方向为:甲电极→发动机→乙电极 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】SOEC装置是一种高温固体氧化物电解池,可以从大气中回收CO2,其工作温度为600~1000℃,利用固态CeO2中的 定向移动形成离子电流。SOEC由多个层状工作单元叠加而成,拆解后装置如图所示(CO2在电极b上反应,外接电源与部分气体管路、流向未显示)。下列说法正确的是
定向移动形成离子电流。SOEC由多个层状工作单元叠加而成,拆解后装置如图所示(CO2在电极b上反应,外接电源与部分气体管路、流向未显示)。下列说法正确的是
 定向移动形成离子电流。SOEC由多个层状工作单元叠加而成,拆解后装置如图所示(CO2在电极b上反应,外接电源与部分气体管路、流向未显示)。下列说法正确的是
定向移动形成离子电流。SOEC由多个层状工作单元叠加而成,拆解后装置如图所示(CO2在电极b上反应,外接电源与部分气体管路、流向未显示)。下列说法正确的是
A.电极b为阳极,电极反应为 |
B.在气孔Z附近检测到少量 ,说明发生了电极反应: ,说明发生了电极反应: |
C.装置工作过程中,CeO2(s)电解质中的 由电极a移向电极b 由电极a移向电极b |
| D.由于产生有毒气体CO,故必须将各层密封,防止气体泄露 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得的溶液中加入1 mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解)。则电解过程中转移电子的物质的量为
| A.4 mol | B.8 mol | C.6 mol | D.5mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】ClO2是一种安全稳定、高效低毒的消毒剂,常用于自来水的消毒。工业上通过惰性电极电解NH4Cl和HCl溶液来制备ClO2,其原理如图所示。下列说法正确的是
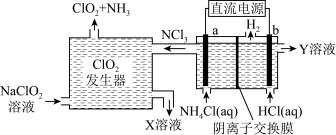

| A.b与电源的正极连接,在b极区流出的Y溶液为稀盐酸 |
| B.当有0.3mol阴离子通过离子交换膜时,ClO2发生器中产生1.12LNH3 |
C.a电极发生的电极反应为 -6e-+3Cl-=NCl3+4H+ -6e-+3Cl-=NCl3+4H+ |
| D.每生成1 mol ClO2,b极区溶液质量减少1 g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】工业上制取KIO3可采用如下两种方法:
方法1:直接歧化法:将精制I2溶于过量KOH溶液,发生的反应为3I2+6KOH=KIO3+5KI+3H2O。
方法2:电解法:将直接歧化法反应后的溶液,加入阳极区,使KI转化为KIO3(I-+6OH--6e-= +3H2O),在阴极区加入KOH溶液,电解槽用水冷却。
+3H2O),在阴极区加入KOH溶液,电解槽用水冷却。

下列说法正确的是
方法1:直接歧化法:将精制I2溶于过量KOH溶液,发生的反应为3I2+6KOH=KIO3+5KI+3H2O。
方法2:电解法:将直接歧化法反应后的溶液,加入阳极区,使KI转化为KIO3(I-+6OH--6e-=
 +3H2O),在阴极区加入KOH溶液,电解槽用水冷却。
+3H2O),在阴极区加入KOH溶液,电解槽用水冷却。
下列说法正确的是
| A.方法1中,氧化剂与还原剂物质的量之比为1:2 |
| B.当外电路转移1mole-,阴极区溶液质量减少18g |
| C.电解过程中处于阴极区的电极1上会有氧气生成 |
| D.若电流利用率为100%,理论上电解法制KIO3碘原子的利用率是直接歧化法的3倍 |
您最近一年使用:0次