按要求填空:
(1)某气体 ,它的摩尔质量为M
,它的摩尔质量为M ,阿伏伽德罗常数用
,阿伏伽德罗常数用 表示,则一个X原子的质量为
表示,则一个X原子的质量为___________  。
。
(2)18.6g 中含有
中含有 个
个 ,
, 的值为
的值为___________ 。
(3)某工厂用氨制硝酸和铵盐的流程如图所示。
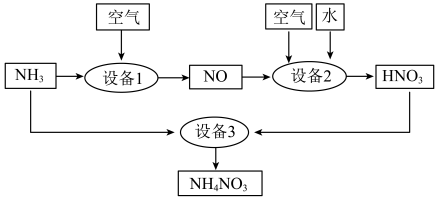
①设备1中发生反应的化学方程式是___________ 。
②在工业上,可用浓氨水检验输送氯气的管道是否漏气,若漏气则有白烟生成,写出反应的化学方程式:___________ 。同温同压下,理论上设备1与设备2中消耗空气的体积比为___________ 。
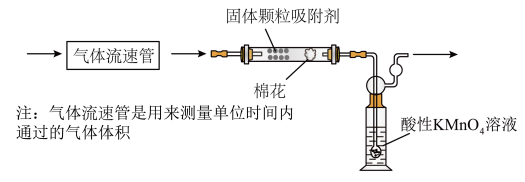
(4)某化学兴趣小组为测定空气中 含量,用如图所示装置进行定量分析:若实验中气体流速为
含量,用如图所示装置进行定量分析:若实验中气体流速为
 ,酸性
,酸性 溶液的体积为
溶液的体积为 L,其浓度为
L,其浓度为
 。从气体通入到紫色恰好褪去,用时
。从气体通入到紫色恰好褪去,用时 。此过程的离子方程式为
。此过程的离子方程式为___________ 。此次取样的空气中 含量为
含量为___________  。
。
(1)某气体
 ,它的摩尔质量为M
,它的摩尔质量为M ,阿伏伽德罗常数用
,阿伏伽德罗常数用 表示,则一个X原子的质量为
表示,则一个X原子的质量为 。
。(2)18.6g
 中含有
中含有 个
个 ,
, 的值为
的值为(3)某工厂用氨制硝酸和铵盐的流程如图所示。

①设备1中发生反应的化学方程式是
②在工业上,可用浓氨水检验输送氯气的管道是否漏气,若漏气则有白烟生成,写出反应的化学方程式:
(4)某化学兴趣小组为测定空气中
 含量,用如图所示装置进行定量分析:若实验中气体流速为
含量,用如图所示装置进行定量分析:若实验中气体流速为
 ,酸性
,酸性 溶液的体积为
溶液的体积为 L,其浓度为
L,其浓度为
 。从气体通入到紫色恰好褪去,用时
。从气体通入到紫色恰好褪去,用时 。此过程的离子方程式为
。此过程的离子方程式为 含量为
含量为 。
。
更新时间:2024-02-10 20:17:29
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)标准状况下,1.7gH2S的体积为___ L。
(2)Fe2(SO4)3溶液中SO 的浓度为0.3mol·L-1,c[Fe2(SO4)3]=
的浓度为0.3mol·L-1,c[Fe2(SO4)3]=___ mol·L-1。
(3)标准状况下,8.8g某气态氧化物RO2的体积为4.48L,则元素R的相对原子质量为___ 。
(4)用18mol/L浓硫酸配制100mL3.6mol/L的稀硫酸。需要浓硫酸___ mL。
(5)画出下列反应的双线桥,并完成填空:___ 。
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
该反应的还原剂是___ ,还原产物是___ 。
(1)标准状况下,1.7gH2S的体积为
(2)Fe2(SO4)3溶液中SO
 的浓度为0.3mol·L-1,c[Fe2(SO4)3]=
的浓度为0.3mol·L-1,c[Fe2(SO4)3]=(3)标准状况下,8.8g某气态氧化物RO2的体积为4.48L,则元素R的相对原子质量为
(4)用18mol/L浓硫酸配制100mL3.6mol/L的稀硫酸。需要浓硫酸
(5)画出下列反应的双线桥,并完成填空:
Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O该反应的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学的知识填空。
(1)已知铜在常温下能被稀HNO3溶解:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O
①用双线桥法表示上述电子转移的方向和数目(在化学方程式上标出)______ 。
②请将上述反应改写成离子方程式:_________________________________________ ;
③19.2g铜与稀硝酸完全反应,生成的气体在标准状况下的体积为_________________ L;若4 mol HNO3参加反应,则该过程转移电子的数目为__________________________ 。
(2)标准状况下,44.8 L由O2和CO2组成的混合气体的质量为82g,则O2的质量为_________ g,该混合气体的平均摩尔质量为_______________________ 。
(3)3.4g NH3中所含氢原子数目与标准状况下__________ L CH4所含氢原子数相同。
(1)已知铜在常温下能被稀HNO3溶解:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O
①用双线桥法表示上述电子转移的方向和数目(在化学方程式上标出)
②请将上述反应改写成离子方程式:
③19.2g铜与稀硝酸完全反应,生成的气体在标准状况下的体积为
(2)标准状况下,44.8 L由O2和CO2组成的混合气体的质量为82g,则O2的质量为
(3)3.4g NH3中所含氢原子数目与标准状况下
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知CO2与碱溶液发生反应时,依次发生如下离子反应:CO2+2OH-→CO32-+H2O、CO2+CO32-+H2O→2HCO3-。
(1)向含0.01mol氢氧化钙的石灰水中通入CO2,得到0.4g白色沉淀,则通入CO2的物质的量为_____ mol或_____ mol。
(2)现有NaOH和Ba(OH)2混合溶液100mL,已知该溶液中c(OH-)=1mol/L,向溶液中缓缓通入CO2气体(溶液体积变化忽略不计),当至少通入CO2气体体积为0.56L(标准状态)时生成的沉淀最多,则原溶液中氢氧化钠和氢氧化钡的物质的量浓度各为多少?(写出计算过程)____ 。
(1)向含0.01mol氢氧化钙的石灰水中通入CO2,得到0.4g白色沉淀,则通入CO2的物质的量为
(2)现有NaOH和Ba(OH)2混合溶液100mL,已知该溶液中c(OH-)=1mol/L,向溶液中缓缓通入CO2气体(溶液体积变化忽略不计),当至少通入CO2气体体积为0.56L(标准状态)时生成的沉淀最多,则原溶液中氢氧化钠和氢氧化钡的物质的量浓度各为多少?(写出计算过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在浓硝酸中放入铜片,则:
(1)开始反应的化学方程式为___________ ,实验现象为___________ 。
(2)若铜有剩余,则反应将要结束时的化学方程式为________ 。
(3)待反应停止后若有铜剩余,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是___________ 。
(4)若将12.8 g铜与一定量的浓硝酸反应,铜消耗完时,共产生气体5.6 L(标准状况),则所消耗的硝酸的物质的量是________ 。
(1)开始反应的化学方程式为
(2)若铜有剩余,则反应将要结束时的化学方程式为
(3)待反应停止后若有铜剩余,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是
(4)若将12.8 g铜与一定量的浓硝酸反应,铜消耗完时,共产生气体5.6 L(标准状况),则所消耗的硝酸的物质的量是
您最近一年使用:0次
【推荐2】按下面各个小题的要求填空
(1)有下列各组物质,将符合下方描述的组合对应的字母填在横线上
A. O2和O3 B.12C和13C C.甲烷和庚烷D. CH3CH2CH2CH3和 E.
E. 和
和
a.____________ 组两物质互为同位素。
b.____________ 组两物质互为同素异形体。
c.____________ 组两物质属于同系物。
d.____________ 组两物质互为同分异构体。
(2)(1)①P4(s,白磷)+5O2(g)=P4O10(s) △H1=−2983.2kJ/mol
②P(s,红磷)+5/4O2(g)=1/4P4O10(s),△H=−738.5kJ/mol
根据上述信息,写出白磷转化为红磷的热化学方程式________ .
(3)已知C2H4(g)和C2H5OH(l)的燃烧热分别是1141kJ/mol和1366.8kJ/mol,写出C2H4(g)和H2O(l)反应生成C2H5OH(l)的热化学方程式:_______ 。
(4)某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜。某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下气体6.72L(其中NO2和NO的体积比为2:1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比___________ 。
②反应后得到的溶液中H+的浓度为1.0mol/L,求原硝酸的物质的量浓度。(假设反应前后溶液的体积不变)_____________
(1)有下列各组物质,将符合下方描述的组合对应的字母填在横线上
A. O2和O3 B.12C和13C C.甲烷和庚烷D. CH3CH2CH2CH3和
 E.
E. 和
和
a.
b.
c.
d.
(2)(1)①P4(s,白磷)+5O2(g)=P4O10(s) △H1=−2983.2kJ/mol
②P(s,红磷)+5/4O2(g)=1/4P4O10(s),△H=−738.5kJ/mol
根据上述信息,写出白磷转化为红磷的热化学方程式
(3)已知C2H4(g)和C2H5OH(l)的燃烧热分别是1141kJ/mol和1366.8kJ/mol,写出C2H4(g)和H2O(l)反应生成C2H5OH(l)的热化学方程式:
(4)某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜。某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下气体6.72L(其中NO2和NO的体积比为2:1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比
②反应后得到的溶液中H+的浓度为1.0mol/L,求原硝酸的物质的量浓度。(假设反应前后溶液的体积不变)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu 反应,若在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为:___________________ 。
(2)在一定体积的10mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积__________ (填“大于”、“ 等于”或“小于”)180mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________ 。
(3)镁铁混合物4.9g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2 .24LNO气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是____________ 。
(1)稀盐酸不与Cu 反应,若在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为:
(2)在一定体积的10mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积
(3)镁铁混合物4.9g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2 .24LNO气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫代硫酸钠晶体( ,
,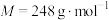 )可用作定影剂、还原剂。市售硫代硫酸钠中常含有硫酸根离子。回答下列问题:
)可用作定影剂、还原剂。市售硫代硫酸钠中常含有硫酸根离子。回答下列问题:
I.市售硫代硫酸钠中硫酸根离子的检验
供选用的试剂:稀盐酸、稀 、
、 溶液、
溶液、 溶液、
溶液、 溶液
溶液
(1)溶解。选用去氧蒸馏水溶解样品的原因是___________ 。
(2)滴加___________ ,观察到现象是有淡黄色沉淀和气泡产生,原因是___________ (用离子方程式回答)。
(3)静置后取上层清液少许,再滴加 溶液,出现
溶液,出现___________ ,说明含有 。
。
Ⅱ.硫酸根离子的去除
(4)可用 溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度
溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度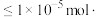
 认为完全除尽)溶液中
认为完全除尽)溶液中 的浓度至少为
的浓度至少为___________ (保留两位小数,已知:该温度下,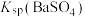
 ,
,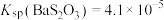 )。
)。
Ⅲ.利用 标准溶液定量测定硫代硫酸钠的纯度,步骤如下:
标准溶液定量测定硫代硫酸钠的纯度,步骤如下:
(5)溶液配制:称取mg某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至100mL的___________ (填仪器名称)中,加蒸馏水至刻度线。
(6)滴定:取a 的
的 标准溶液bmL,用硫酸酸化后加入过量KI溶液,发生反应:
标准溶液bmL,用硫酸酸化后加入过量KI溶液,发生反应: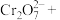
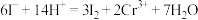 ,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: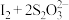
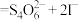 。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为cmL,则样品纯度为
。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为cmL,则样品纯度为___________ %。
 ,
,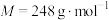 )可用作定影剂、还原剂。市售硫代硫酸钠中常含有硫酸根离子。回答下列问题:
)可用作定影剂、还原剂。市售硫代硫酸钠中常含有硫酸根离子。回答下列问题:I.市售硫代硫酸钠中硫酸根离子的检验
供选用的试剂:稀盐酸、稀
 、
、 溶液、
溶液、 溶液、
溶液、 溶液
溶液(1)溶解。选用去氧蒸馏水溶解样品的原因是
(2)滴加
(3)静置后取上层清液少许,再滴加
 溶液,出现
溶液,出现 。
。Ⅱ.硫酸根离子的去除
(4)可用
 溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度
溶液除去市售硫代硫酸钠溶液中硫酸根离子,当刚好除尽时(金属离子浓度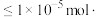
 认为完全除尽)溶液中
认为完全除尽)溶液中 的浓度至少为
的浓度至少为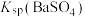
 ,
,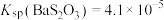 )。
)。Ⅲ.利用
 标准溶液定量测定硫代硫酸钠的纯度,步骤如下:
标准溶液定量测定硫代硫酸钠的纯度,步骤如下:(5)溶液配制:称取mg某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至100mL的
(6)滴定:取a
 的
的 标准溶液bmL,用硫酸酸化后加入过量KI溶液,发生反应:
标准溶液bmL,用硫酸酸化后加入过量KI溶液,发生反应: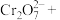
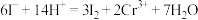 ,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: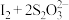
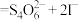 。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为cmL,则样品纯度为
。加入淀粉溶液作为指示剂,继续滴定至终点。平行滴定3次,样品溶液的平均用量为cmL,则样品纯度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】 (三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用 作感光剂,以
作感光剂,以 溶液为显色剂。其光解反应的化学方程式为:
溶液为显色剂。其光解反应的化学方程式为: ;显色反应的化学方程式为
;显色反应的化学方程式为_______ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是_______ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有_______ 、_______ 。
③为防止倒吸,停止实验时应进行的操作是_______ 。
④样品完全分解后,装置A中的残留物含有FeO和 ,检验
,检验 存在的方法是:
存在的方法是:_______ 。
(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀 酸化,用c mol/L
酸化,用c mol/L  溶液滴定至终点。滴定终点的现象是
溶液滴定至终点。滴定终点的现象是_______ 。
②向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀 酸化,用c mol/L
酸化,用c mol/L  溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液V mL。该晶体中铁的质量分数的表达式为
溶液V mL。该晶体中铁的质量分数的表达式为_______ 。若滴定前滴定管尖嘴内无气泡,终点读数时滴定管尖嘴内留有气泡,会使测定结果_______ 。(填偏大,偏小或无影响)
 (三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:(1)晒制蓝图时,用
 作感光剂,以
作感光剂,以 溶液为显色剂。其光解反应的化学方程式为:
溶液为显色剂。其光解反应的化学方程式为: ;显色反应的化学方程式为
;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和
 ,检验
,检验 存在的方法是:
存在的方法是:(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀
 酸化,用c mol/L
酸化,用c mol/L  溶液滴定至终点。滴定终点的现象是
溶液滴定至终点。滴定终点的现象是②向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀
 酸化,用c mol/L
酸化,用c mol/L  溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液V mL。该晶体中铁的质量分数的表达式为
溶液V mL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】二氧化氯消毒剂是国际公认的高效消毒灭菌剂。
(1)制备 的一种反应为:
的一种反应为: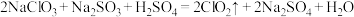 ,用双线桥法标出其电子转移的方向和数目
,用双线桥法标出其电子转移的方向和数目_______ 。
(2)实验室可用亚氯酸钠 溶液与氯气反应制
溶液与氯气反应制 ,此反应的化学方程式为
,此反应的化学方程式为_______ 。
(3) 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是_______ 。
(4) 可经过题图所示的转化制取
可经过题图所示的转化制取 。已知“反应II”为复分解反应。
。已知“反应II”为复分解反应。

①“反应I”的离子方程式为_______ 。
②过滤之后是洗涤,判断 沉淀是否洗涤干净的方法是
沉淀是否洗涤干净的方法是_______ 。
(5)一种“二氧化氯泡腾片”有效成分为 、
、 、
、 ,该泡腾片能快速溶于水,产生大量气泡,得到
,该泡腾片能快速溶于水,产生大量气泡,得到 溶液。取某品牌泡腾片1片溶于水配成
溶液。取某品牌泡腾片1片溶于水配成 溶液,为测定溶液中
溶液,为测定溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:
①取该溶液 ,加入锥形瓶中,用稀硫酸调节溶液
,加入锥形瓶中,用稀硫酸调节溶液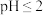 ,再加入足量
,再加入足量 晶体,发生反应:
晶体,发生反应: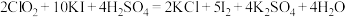
②用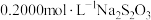 溶液和生成的碘单质反应,化学方程式如下:
溶液和生成的碘单质反应,化学方程式如下: ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液
溶液 。
。
则配成的 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为_______ 。(写出计算过程)
(1)制备
 的一种反应为:
的一种反应为: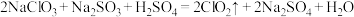 ,用双线桥法标出其电子转移的方向和数目
,用双线桥法标出其电子转移的方向和数目(2)实验室可用亚氯酸钠
 溶液与氯气反应制
溶液与氯气反应制 ,此反应的化学方程式为
,此反应的化学方程式为(3)
 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是(4)
 可经过题图所示的转化制取
可经过题图所示的转化制取 。已知“反应II”为复分解反应。
。已知“反应II”为复分解反应。
①“反应I”的离子方程式为
②过滤之后是洗涤,判断
 沉淀是否洗涤干净的方法是
沉淀是否洗涤干净的方法是(5)一种“二氧化氯泡腾片”有效成分为
 、
、 、
、 ,该泡腾片能快速溶于水,产生大量气泡,得到
,该泡腾片能快速溶于水,产生大量气泡,得到 溶液。取某品牌泡腾片1片溶于水配成
溶液。取某品牌泡腾片1片溶于水配成 溶液,为测定溶液中
溶液,为测定溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:①取该溶液
 ,加入锥形瓶中,用稀硫酸调节溶液
,加入锥形瓶中,用稀硫酸调节溶液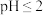 ,再加入足量
,再加入足量 晶体,发生反应:
晶体,发生反应: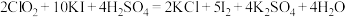
②用
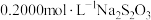 溶液和生成的碘单质反应,化学方程式如下:
溶液和生成的碘单质反应,化学方程式如下: ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液
溶液 。
。则配成的
 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次



