碱性锌锰干电池是一种使用广泛的便携式电源,电池总反应为Zn+2MnO2+H2O=ZnO+2MnOOH。下列说法错误的是
| A.MnOOH中Mn的化合价为+3 |
| B.参与正极反应的物质为MnO2和H2O |
| C.负极的电极反应为Zn-2e-=Zn2+ |
| D.电池工作时,电子由负极通过外电路流向正极 |
更新时间:2024-01-14 20:26:12
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列因果关系说法合理的是
| A.Mg的金属活动性强于Al,所以Mg、Al作电极的原电池中,Mg为负极,Al为正极 |
| B.浓硫酸能氧化Cu单质而稀硫酸不能,说明稀硫酸没有氧化性 |
| C.HCl的酸性强于H2S的,原因是Cl的非金属性强于S的 |
| D.过氧乙酸(CH3COOOH)与H2O2都包含“-O-O-”结构,所以两者均具有较强的氧化性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某原电池装置如图所示,电池总反应为 2Ag + Cl2 = 2AgCl。已知阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒。下列说法正确的是
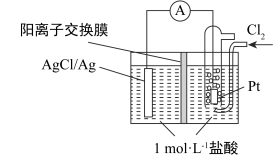

| A.正极反应式为 AgCl + e—= Ag + Cl— |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用 NaCl 溶液代替盐酸,则电池总反应随之改变 |
| D.当外电路中转移 0.1mol e—时,阳离子交换膜左侧溶液中约减少0.2mol 离子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】微生物燃料电池能在较低的有机负荷下将化学能转化为电能,可用于有机污染的生物修复,其反应原理如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是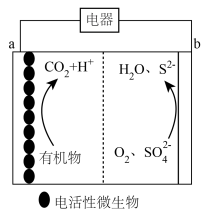
| A.a极是电池负极 |
B.电子从 极经电解质溶液流向 极经电解质溶液流向 极 极 |
C. 向 向 极移动 极移动 |
D.若“有机物”是甲烷,则a极每产生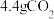 ,转移电子数为 ,转移电子数为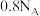 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
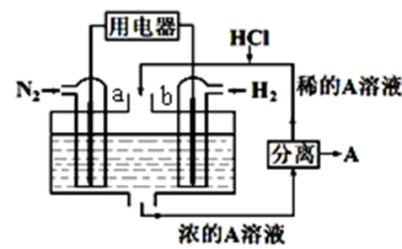
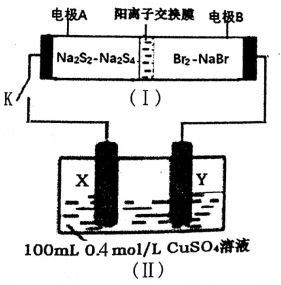
【推荐2】化学电源在生活中有广泛的应用,各种电池的示意图如图,下列有关说法正确的是
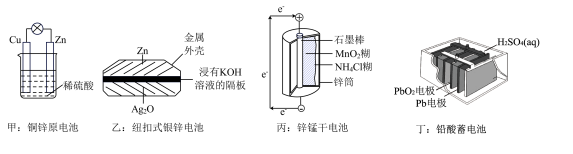
| A.甲:电流由锌片经导线流向铜片 |
| B.乙:负极的电极反应式为Zn-2e-=Zn2+ |
| C.丙:锌筒作负极,发生还原反应,使用一段时间锌筒会变薄 |
| D.丁:使用一段时间后电解质溶液的酸性减弱,导电能力减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下图原电池装置中,用盐桥连接两烧杯中的电解质溶液。盐桥中阳、阴离子的电迁移率应尽可能地相近。(电迁移率用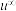 表示,单位:
表示,单位: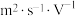 )。下列有关说法
)。下列有关说法不正确 的是
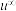 表示,单位:
表示,单位: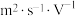 )。下列有关说法
)。下列有关说法| 阳离子 |  | 阴离子 |  | 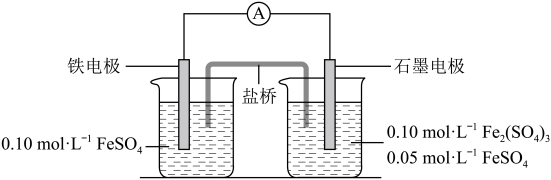 已知:左、右烧杯中溶液体积相同 |
 | 4.07 |  | 4.61 | |
 | 5.19 |  | 7.40 | |
 | 6.59 |  | 7.91 | |
 | 7.62 |  | 8.27 |
A.盐桥中的电解质可以为 |
| B.盐桥中的阳离子进入右侧烧杯溶液中 |
| C.电流计读数不变时,向右侧烧杯中加入硫酸铁固体,指针会继续偏转 |
D.电池反应一段时间后,测得左侧溶液中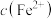 增加了 增加了 ,则右侧溶液中 ,则右侧溶液中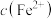 为 为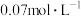 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.原电池中,负极上发生的反应是还原反应 |
| B.原电池中,电流的方向是负极−导线−正极 |
| C.双液原电池中的盐桥是为了连通电路,所以也可以用金属导线代替 |
| D.在原电池中,阳离子移向正极,阴离子移向负极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】研究人员最近发明了一种“水”电池,在海水中电池反应可表示为: ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.填充MnO2的电极为正极 |
B.该电池的负极反应式是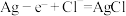 |
| C.在电池中,Na+不断移动到“水”电池的正极 |
| D.外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是1mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】科学家开发出的固体电解质 可以提升锂-硫电池的放电性能(如图)。下列说法正确的是
可以提升锂-硫电池的放电性能(如图)。下列说法正确的是
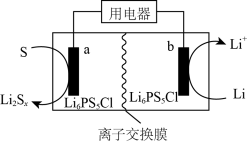
 可以提升锂-硫电池的放电性能(如图)。下列说法正确的是
可以提升锂-硫电池的放电性能(如图)。下列说法正确的是
| A.a极为负极 |
| B.该离子交换膜仅允许阴离子通过 |
C.a极的电极反应式为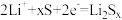 |
| D.当b极上消耗14gLi时,转移1mol电子 |
您最近一年使用:0次

 -4e-=2H2O+2CO2,则下列推断中正确的是
-4e-=2H2O+2CO2,则下列推断中正确的是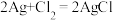 。下列说法错误的是
。下列说法错误的是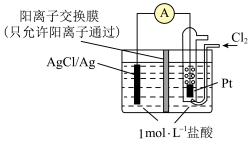
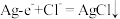
 溶液代替盐酸,则电池总反应不变
溶液代替盐酸,则电池总反应不变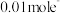 时,交换膜左侧溶液中减少
时,交换膜左侧溶液中减少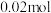 离子
离子