随着原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如下图所示:
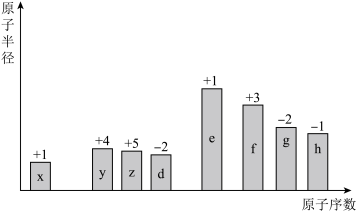
(1)h在元素周期表中的位置是___________ 。
(2)d、g的简单氢化物中热稳定性较强的是___________ (填化学式)。
(3)由10个x原子与4个y原子构成化合物的结构式有___________ 种。
(4)e、g形成的离子化合物的电子式为___________ 。e元素形成的最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(5)e与f相比,金属性较强的是___________ (用元素符号表示),下列事实能证明这一结论的是___________ 。(填字母序号)。
a.e单质的熔点比f单质的低,单质的硬度也比f单质小
b.e单质可与冷水剧烈反应,而f单质与冷水几乎不反应
c.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
(6)h的单质能将z从其简单氢化物中置换出来,化学方程式为___________ 。

(1)h在元素周期表中的位置是
(2)d、g的简单氢化物中热稳定性较强的是
(3)由10个x原子与4个y原子构成化合物的结构式有
(4)e、g形成的离子化合物的电子式为
(5)e与f相比,金属性较强的是
a.e单质的熔点比f单质的低,单质的硬度也比f单质小
b.e单质可与冷水剧烈反应,而f单质与冷水几乎不反应
c.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
(6)h的单质能将z从其简单氢化物中置换出来,化学方程式为
更新时间:2024-01-24 17:22:36
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
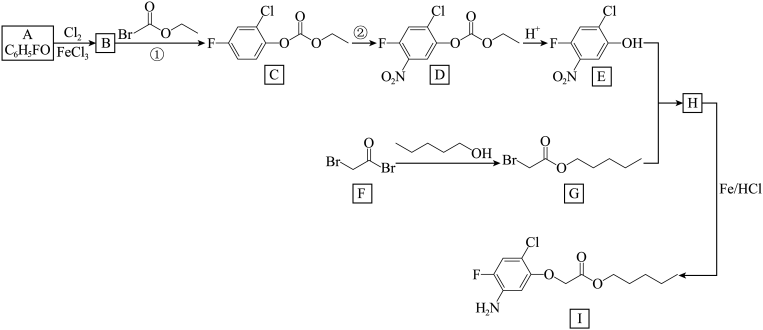
【推荐1】化合物I是合成药物的中间体,其一种合成路线如下图:___________ ;I分子中碳原子的杂化方式有___________ ;Z是I与足量氢气在镍催化下完全反应的生成物,则Z分子中含有___________ 个手性碳原子。
(2)反应①在该合成路线中的作用是___________ 。
(3)“H→I”的反应类型为___________ 。
(4)反应②的化学方程式为___________ 。
(5)“E+G→H”的化学方程式为___________ 。
(6)W在分子组成上比G少一个CH2,同时满足下列条件的W有___________ 种。(不考虑立体异构)
①水解得到的醇羟基能被氧化成羧基
②能与碳酸氢钠溶液反应放出二氧化碳
(7)参照上述合成路线,设计由苯酚合成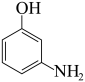 的路线图(其他试剂任选)
的路线图(其他试剂任选)___________ 。
(2)反应①在该合成路线中的作用是
(3)“H→I”的反应类型为
(4)反应②的化学方程式为
(5)“E+G→H”的化学方程式为
(6)W在分子组成上比G少一个CH2,同时满足下列条件的W有
①水解得到的醇羟基能被氧化成羧基
②能与碳酸氢钠溶液反应放出二氧化碳
(7)参照上述合成路线,设计由苯酚合成
 的路线图(其他试剂任选)
的路线图(其他试剂任选)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如图:
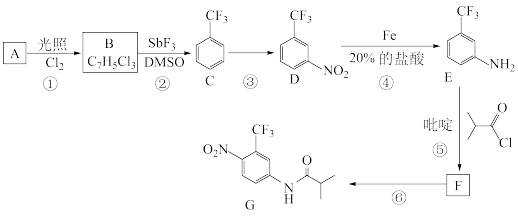
请回答下列问题:
(1)A的化学名称为______ ;C中官能团的名称是_______ 。
(2)③的反应试剂和反应条件分别是_______ ,该反应类型是________ 。
(3)已知吡啶是一种有机碱,在反应⑤中的作用是________
(4)反应④的化学方程式为__________
(5)G的相对分子质量为__________ 。
(6)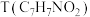 是E在碱性条件下的水解产物,同时符合下列条件的T的同分异构体有
是E在碱性条件下的水解产物,同时符合下列条件的T的同分异构体有___ 种。其中核磁共振氢谱上有4组峰且峰面积比为1∶2∶2∶2的物质的结构简式为_____ 。
①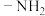 直接连在苯环上;②能与新制氢氧化铜悬浊液共热产生红色固体。
直接连在苯环上;②能与新制氢氧化铜悬浊液共热产生红色固体。
(7)参照上述合成路线,以CH3CH2COCl和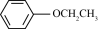 为原料,经三步合成某化工产品
为原料,经三步合成某化工产品 的路线为(其他无机试剂任选)
的路线为(其他无机试剂任选)_____ 。

请回答下列问题:
(1)A的化学名称为
(2)③的反应试剂和反应条件分别是
(3)已知吡啶是一种有机碱,在反应⑤中的作用是
(4)反应④的化学方程式为
(5)G的相对分子质量为
(6)
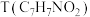 是E在碱性条件下的水解产物,同时符合下列条件的T的同分异构体有
是E在碱性条件下的水解产物,同时符合下列条件的T的同分异构体有①
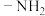 直接连在苯环上;②能与新制氢氧化铜悬浊液共热产生红色固体。
直接连在苯环上;②能与新制氢氧化铜悬浊液共热产生红色固体。(7)参照上述合成路线,以CH3CH2COCl和
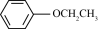 为原料,经三步合成某化工产品
为原料,经三步合成某化工产品 的路线为(其他无机试剂任选)
的路线为(其他无机试剂任选)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】布洛芬是生活中常用的退烧药,它除了具有降温作用、缓解疼痛外,还有抑制肺部炎症的作用。一种制备布洛芬的合成路线如图:
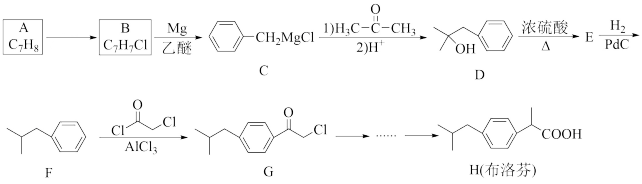
请回答下列问题:
(1)A的化学名称为_______ ;A转化为B所需要的反应条件为_______ 。
(2)有机物X与CH3COCH3分子式相同且能发生银镜反应,写出X发生银镜反应的化学方程式_______ 。
(3)E分子中含有2个甲基,则E的结构简式为_______ 。
(4)F转化为G的化学方程式为_______ 。
(5)依据RCH=CH2+CO+H2O RCH(CH3)COOH某研究小组以有机物Z为原料能一步合成布洛芬,则Z的结构简式为
RCH(CH3)COOH某研究小组以有机物Z为原料能一步合成布洛芬,则Z的结构简式为_______ 。
(6)有机物Y是布洛芬的同分异构体,满足下列条件的Y有_______ 种。
①苯环上有三个取代基,其中之一为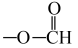 ;
;
②苯环上有两种不同化学环境的氢原子。
(7)写出以乙苯、CH3CH2COCl、CH3CH2MgCl为原料制备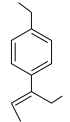 的合成路线:
的合成路线:_______ (无机试剂任选,合成路线示例见本题题干)。

请回答下列问题:
(1)A的化学名称为
(2)有机物X与CH3COCH3分子式相同且能发生银镜反应,写出X发生银镜反应的化学方程式
(3)E分子中含有2个甲基,则E的结构简式为
(4)F转化为G的化学方程式为
(5)依据RCH=CH2+CO+H2O
 RCH(CH3)COOH某研究小组以有机物Z为原料能一步合成布洛芬,则Z的结构简式为
RCH(CH3)COOH某研究小组以有机物Z为原料能一步合成布洛芬,则Z的结构简式为(6)有机物Y是布洛芬的同分异构体,满足下列条件的Y有
①苯环上有三个取代基,其中之一为
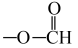 ;
;②苯环上有两种不同化学环境的氢原子。
(7)写出以乙苯、CH3CH2COCl、CH3CH2MgCl为原料制备
 的合成路线:
的合成路线:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】用图表来处理数据是发现科学规律的一种重要方法。
(1)下图是原子序数为1~18的元素原子的最外层电子数随原子序数变化的直方图。图中元素a是_______ (填元素名称)。

(2)下图表示元素的一种性质随原子序数变化的情况,分析该图纵坐标表示的是_______ 。2020年新型冠状病毒席卷世界各地,“84”消毒液(有效成分为NaClO)发挥了重要作用,用原子序数为17的元素单质和氢氧化钠溶液制备NaClO的离子方程式为_______ 。

(3)下表给出了部分元素的原子半径:
①请根据表中数据分析,同主族元素原子半径的递变规律是_______ 。比较Na+和F-的半径大小:r(Na+)_______ r(F-)(填“>”、“=”或“<”)。
②Cs在元素周期表中的位置是_______ 。
③下列可作为比较Na和K金属性强弱的方法是_______ (填字母)。
a.比较等量的两种金属与盐酸反应放出气体的多少
b.比较最高价氧化物对应水化物的碱性强弱
c.比较单质燃烧时的焰色
d.比较大小、形状相同的等量金属与水反应的剧烈程度
(1)下图是原子序数为1~18的元素原子的最外层电子数随原子序数变化的直方图。图中元素a是

(2)下图表示元素的一种性质随原子序数变化的情况,分析该图纵坐标表示的是

(3)下表给出了部分元素的原子半径:
| 元素符号 | Li | Be | B | C | N | O | F | Na | K | Rb | Cs |
| 原子半径/nm | 0.152 | 0.089 | 0.082 | 0.077 | 0.075 | 0.074 | 0.071 | 0.186 | 0.227 | 0.248 | 0.265 |
②Cs在元素周期表中的位置是
③下列可作为比较Na和K金属性强弱的方法是
a.比较等量的两种金属与盐酸反应放出气体的多少
b.比较最高价氧化物对应水化物的碱性强弱
c.比较单质燃烧时的焰色
d.比较大小、形状相同的等量金属与水反应的剧烈程度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】表为周期表的一部分,其中的编号代表对应的元素,请用元素符号 回答下列问题
(1)上述元素中,属于ds区的是_______ (填元素符号)。
(2)不能 说明⑨的金属性比⑩强的是_______ 。
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是_______ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ 分子的空间构型为_______ 。
(4)元素⑫与 可形成
可形成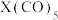 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ⑪ | ⑫ | ⑬ | ⑭ |
(2)
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是
(4)元素⑫与
 可形成
可形成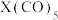 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:______ 与盐酸反应最剧烈,____ 与盐酸反应的速度最慢;____ 与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为______________________________ ;
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_________ ,________________ ;
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律
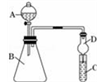
(4)干燥管D的作用为_______________ ;
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液________________________ 的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有______________ 溶液的洗气瓶.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律

(4)干燥管D的作用为
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是部分短周期元素的常见化合价与原子序数的关系图:
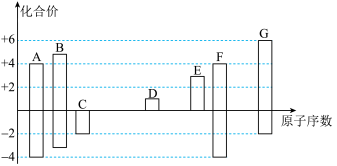
请回答下列问题:
(1)AB-离子与__________ 互为等电子体,lmolAB-离子含有___________ molπ键。
(2)用电子式表示D2G的形成过程________________________ 。
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器______________________________ ;
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时__________________________
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。
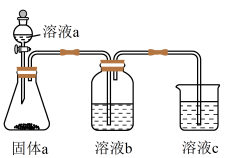
①溶液a和b分别为________________ ,________________ 。
②溶液c中的离子方程式为________________________________________________ 。
③请从原子结构的角度解释非金属性B>A的原因______________________________ 。

请回答下列问题:
(1)AB-离子与
(2)用电子式表示D2G的形成过程
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。

①溶液a和b分别为
②溶液c中的离子方程式为
③请从原子结构的角度解释非金属性B>A的原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如表是元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:

(1)⑥在元素周期表中的位置是____ ;②、③、④三种元素的原子半径最小的是____ (填元素符号)。③和④的气态氢化物中稳定性更强的是____ (填化学式)。
(2)写出①和②形成的一种化合物的电子式____ 。
(3)⑤和⑦分别形成的最高价氧化物对应的水化物发生反应的离子方程式是____ 。
(4)④和⑨分别形成的简单阴离子还原性较弱的是____ (填离子符号)。
(5)⑤和⑥分别形成的简单离子的半径为 > (填离子符号)____ 。
(6)砷(As)与②同主族,下列推断正确的是____ (填序号)。
a.砷元素的最低负化合价为-3
b.热稳定性:AsH3>NH3
c.最高价氧化物对应的水化物的酸性:HClO4>H3AsO4
(7)设计实验方案证明⑧和⑨的非金属性强弱:____ 。

(1)⑥在元素周期表中的位置是
(2)写出①和②形成的一种化合物的电子式
(3)⑤和⑦分别形成的最高价氧化物对应的水化物发生反应的离子方程式是
(4)④和⑨分别形成的简单阴离子还原性较弱的是
(5)⑤和⑥分别形成的简单离子的半径为 > (填离子符号)
(6)砷(As)与②同主族,下列推断正确的是
a.砷元素的最低负化合价为-3
b.热稳定性:AsH3>NH3
c.最高价氧化物对应的水化物的酸性:HClO4>H3AsO4
(7)设计实验方案证明⑧和⑨的非金属性强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如表是元素周期表的一部分,请据表标注的元素回答(用相应的化学符号作答):

(1)形成单质不含化学键的是_____ (填化学式)。
(2)元素a分别与元素e、k、m所形成的简单气态化合物中稳定性最强的是_____ (填化学式)。
(3)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为_____ (用物质化学式表示)。
(4)元素g、h、m、n所形成的简单离子的半径由大到小的顺序为_____ (用离子符号表示)。
(5)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有_____ 。
(6)写出由元素a、e、g组成的化合物的电子式:_____ 。
(7)写出由元素b、e组成的化合物be2的结构式:_____ 。
(8)下列不能说明氯元素的非金属性比硫元素强的是_____ (填字母)。

(1)形成单质不含化学键的是
(2)元素a分别与元素e、k、m所形成的简单气态化合物中稳定性最强的是
(3)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为
(4)元素g、h、m、n所形成的简单离子的半径由大到小的顺序为
(5)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有
(6)写出由元素a、e、g组成的化合物的电子式:
(7)写出由元素b、e组成的化合物be2的结构式:
(8)下列不能说明氯元素的非金属性比硫元素强的是
| A.氯、硫的最低负价分别为-1、-2 |
| B.硫化氢在300℃时开始分解,HCl在1500℃时开始缓慢分解 |
| C.HClO4的酸性比H2SO3的强 |
| D.向Na2S水溶液中通入Cl2有淡黄色沉淀生成 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】短周期四种元素A、B、C、D,它们的原子序数依次增大。A、D同主族且最外层电子数为奇数,A为元素周期表中原子半径最小的元素,B原子的最外层电子数是次外层电子数的2倍,C为地壳中含量最多的元素。请回答下列问题:
(1)C元素的离子结构示意图________ ,C元素形成的常见液态化合物的结构式________ 。
(2)D元素在元素周期表中的位置__________ ,写出D在C单质中燃烧形成的化合物的电子式__________ 。
(3)B与C分别形成的简单气态氢化物中较稳定的是______ ,其中B形成的简单气态氢化物的空间结构 _______ ,画出B与C反应生成的XY2型化合物的电子式______________ 。
(4)过量B的最高价氧化物与D的最高价氧化物对应的水化物的溶液反应的离子方程式__________________________________________________________________ 。
(5)分子式为B6A14的物质含有多种同分异构体,其中一种同分异构体的一氯代物只有两种,写出该种物质的结构简式______________ 。
(1)C元素的离子结构示意图
(2)D元素在元素周期表中的位置
(3)B与C分别形成的简单气态氢化物中较稳定的是
(4)过量B的最高价氧化物与D的最高价氧化物对应的水化物的溶液反应的离子方程式
(5)分子式为B6A14的物质含有多种同分异构体,其中一种同分异构体的一氯代物只有两种,写出该种物质的结构简式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】四种短周期元素在周期表中的相对位置如下表所示,其中Z原子最外层电子数是其电子层数的2 倍。元素M与Z同周期,且原子半径是同周期中最大的。元素R是第四周期的过渡元素;R有甲、乙两种常见氢氧化物,其中甲在常温下置于空气中,会由白色变为灰绿色,最后变为红褐色的乙。
请按要求回答下列问题:
(1)X的单质的电子式:_________ ;W最高价氧化物的水化物的化学式:________________ 。
(2)M、Z、W分别形成的简单离子的半径由大到小顺序为(填离子符号)__________ ;写一个能说明元素W比元素Z的非金属性强的化学方程式:____________________ 。
(3)甲变为乙的化学方程式为_______________________ 。
(4)常温下,当用200mL 1mol·L-1的MOH溶液吸收4.48L(已折算为标准状况)ZY2时,所得溶液的主要溶质(填化学式)为___________ ;此时溶液pH<7,则其中含Z元素的几种粒子(忽略ZY2)的浓度由大到小的顺序为___________________________ 。
(5) 工业上用电化学法治理酸性废液中的XY3-的原理如图示,其阴极的反应式为_______________ 。
X | Y | |
Z | W |
请按要求回答下列问题:
(1)X的单质的电子式:
(2)M、Z、W分别形成的简单离子的半径由大到小顺序为(填离子符号)
(3)甲变为乙的化学方程式为
(4)常温下,当用200mL 1mol·L-1的MOH溶液吸收4.48L(已折算为标准状况)ZY2时,所得溶液的主要溶质(填化学式)为
(5) 工业上用电化学法治理酸性废液中的XY3-的原理如图示,其阴极的反应式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,Y的单质在W2中燃烧的产物可使品红溶液褪色.Z和W元素形成的化合物Z3W4具有磁性.U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)X在周期表中的位置为______ ;UW2的电子式为______ ;X在UW2中剧烈燃烧生成的黑、白两种固体中化学键类型依次是______ 、______ 。
(2)U、V、W形成的10电子氢化物中,最稳定的是______ (写化学式、下同);沸点最高的是______ ;结合H+能力最强的是(写化学式)______ 。
(3)Z3W4与稀盐酸反应的离子方程式为______ 。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为______ ,由此可知VW和YW2还原性较强的是(写化学式)______ 。
(5)已知YW2和Cl2均可使品红溶液褪色,现将一定量的YW2和Cl2通入品红溶液中:
①若品红不褪色,则品红溶液中所发生的化学方程式为______ 。
②若品红褪色,为证明YW2和Cl2谁过量,最简单的操作、现象、结论是______ 。
请回答下列问题:
(1)X在周期表中的位置为
(2)U、V、W形成的10电子氢化物中,最稳定的是
(3)Z3W4与稀盐酸反应的离子方程式为
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
(5)已知YW2和Cl2均可使品红溶液褪色,现将一定量的YW2和Cl2通入品红溶液中:
①若品红不褪色,则品红溶液中所发生的化学方程式为
②若品红褪色,为证明YW2和Cl2谁过量,最简单的操作、现象、结论是
您最近一年使用:0次



