将NaCl溶于水配成0.5mol/L的溶液,溶解过程如图所示。下列说法正确的是
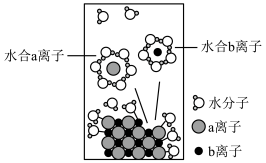
| A.a离子为Cl-,b离子为Na+ | B.溶液中含有0.5NA个水合Na+ |
C.溶液中存在NaCl Na++Cl- Na++Cl- | D.溶解NaCl的过程需在容量瓶中进行 |
更新时间:2024-01-22 21:13:48
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,2.24L  被足量水吸收后形成的氯水中, 被足量水吸收后形成的氯水中, 的分子数为0.1 的分子数为0.1 |
B.常温常压下,7.1g  与足量NaOH溶液反应,转移的电子数为0.2 与足量NaOH溶液反应,转移的电子数为0.2 |
C.0.5 的 的 溶液中含有的 溶液中含有的 数目为0.5 数目为0.5 |
D.7.8g  固体中含有的阴离子数为0.1 固体中含有的阴离子数为0.1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】 为阿伏加 德罗常数的值,下列叙述正确的是( )
为阿伏加 德罗常数的值,下列叙述正确的是( )
 为阿伏加 德罗常数的值,下列叙述正确的是( )
为阿伏加 德罗常数的值,下列叙述正确的是( )A.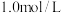 的 的 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
B.12g金刚石中含有碳碳键的个数为 |
C. 时 时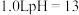 的NaOH溶液中含有 的NaOH溶液中含有 的数目为 的数目为 |
D.1mol的甲基与1mol的铵银离子所含电子数均为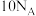 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1molP4和1molCH4中,共价键数均为4NA |
| B.足量的锌与一定量的浓硫酸充分反应,放出标况下2.24 L气体时,转移电子数为0.2NA |
| C.电解精炼铜时,若阴极得电子数为2NA,则阳极质量减少64g |
| D.一定条件下,1molSO2和0.5molO2充分反应,可生成1molSO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】反应NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3↓可用于联合制碱。下列说法正确的是
A.氯离子的结构示意图: |
B.中子数为10的氧原子: |
C.反应体系中核外电子总数相等的微粒只有NH3和 |
D.NaHCO3的电离方程式:NaHCO3=Na++H++ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列化学用语表示正确的是
| A.硫酸铁的化学式: FeSO4 |
| B.K2FeO4 中Fe元素的化合价:+3 |
C.氮原子的结构示意图: |
D.Cu(NO3)2的电离方程式:Cu(NO3)2 = Cu2+ + NO |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】X、Y、Z、M、Q、R皆为前20号元素且原子序数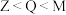 ,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
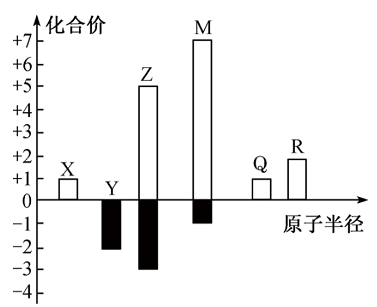
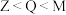 ,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
,其原子半径与最高或最低化合价的关系如图所示。下列说法错误的是
| A.X、Y、Z三种元素组成的化合物可能是酸或碱 |
| B.R位于第四周期第ⅡA族 |
C.简单离子半径: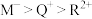 |
| D.Z与M的最高价氧化物对应的水化物均为强酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
真题
【推荐2】科研人员最新研制成一种新型的氮化镓(GaN)晶体管,有望取代传统晶体管。氮化镓中镓元素( )
| A.为+3价 | B.位于第IA族 |
| C.位于第三周期 | D.离子半径大于其原子半径 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】几种第二、三周期元素的原子半径及主要化合价如表所示,下列叙述错误的是
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 75 | 74 |
| 主要化合价 | +2 | +3 | +5、-3 | -2 |
| A.X、Y的最高价氧化物对应水化物的碱性:X>Y |
| B.X与Z形成的化合物为共价化合物 |
| C.气态氢化物稳定性:Z<W |
| D.简单离子的半径:Z>W |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学用浓盐酸配制480mL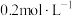 的稀盐酸。下列说法错误的是
的稀盐酸。下列说法错误的是
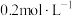 的稀盐酸。下列说法错误的是
的稀盐酸。下列说法错误的是| A.选用500mL容量瓶 |
| B.配制溶液所用的容量瓶不需要干燥 |
| C.实验需用到的玻璃仪器只有烧杯、容量瓶、胶头滴管三种 |
| D.若定容时仰视刻度线,所配溶液浓度偏小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列实验能成功的是
| A | B | C | D |
| 实验室制备Fe(OH)2 | 实验室制取少量氯气 | 制氧化钠 | 配制0.10mol/L NaOH溶液 |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 的水解:
的水解: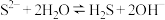
 在水溶液中的电离:
在水溶液中的电离: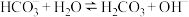
 的水解:
的水解:



