月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ ,Na在氧气中完全燃烧所得产物的电子式为_______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________ (填“高”或“低”)
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为______ ;SiO2的晶体类型为________ 。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为______ (写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH2和700kgN2,若以所得H2和N2为原料经一系列反应最多可制得碳酸氢铵___ kg。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为
(4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH2和700kgN2,若以所得H2和N2为原料经一系列反应最多可制得碳酸氢铵
更新时间:2016-12-09 06:07:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】甲、乙、丙、丁是原子序数依次增大的短周期元素,甲与丙、乙与丁分别同主族,甲、丙均可与乙形成原子个数之比为1:1和2:1的化合物。由甲、乙、丁中的一种或几种元素可组成下列转化关系中的所有物质。
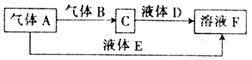
请回答下列问题:
(1)丙元素的离子结构示意图为
(2)E的电子式为
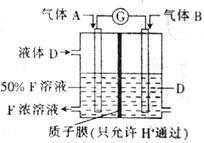
(3)科学家提出设想,以右上图所示装置利用电化学原理生产溶液F,写出通入气体A的一极的电极反应式:


请回答下列问题:
(1)丙元素的离子结构示意图为
(2)E的电子式为
(3)科学家提出设想,以右上图所示装置利用电化学原理生产溶液F,写出通入气体A的一极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】A元素原子M电子层有6个电子,B元素与A元素原子具有相同电子层数,B元素的原子最外层上只有1个电子。
(1)画出B元素的原子结构示意图:_______ 。
(2)A、B两元素形成的化合物的名称是_______ ,该化合物在无色火焰上灼烧时,火焰呈_______ 色。
(1)画出B元素的原子结构示意图:
(2)A、B两元素形成的化合物的名称是
您最近一年使用:0次
【推荐3】元素周期表是学习和研究化学的重要工具,下面是元素周期表的部分内容,请根据下表回答问题:
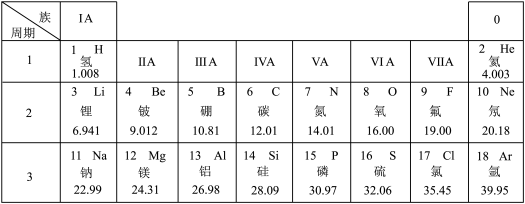
(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为___________ 。
(3)已知某微粒的结构示意图为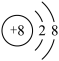 ,请写出该微粒的符号
,请写出该微粒的符号___________ 。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为___________ 。

(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
| A.门捷列夫 | B.拉瓦锡 | C.道尔顿 | D.阿伏加德罗 |
(3)已知某微粒的结构示意图为
 ,请写出该微粒的符号
,请写出该微粒的符号(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】芯片主要由单晶体硅成。下图是硅及其化合物的类价二维图,根据要求完成下列化学方程式或离子方程式。
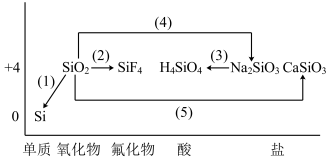
(1)利用焦炭在电炉中还原二氧化硅的化学方程式为_______________ 。
(2)利用氢氟酸刻蚀玻璃的化学方程式为_______________ 。
(3)硅酸钠转化为原硅酸的离子方程式_______________ 。
(4)二氧化硅与烧碱溶液反应的化学方程式_______________ 。
(5)石英与纯碱在玻璃熔炉里加强热发生反应的化学方程式为_______________ 。

(1)利用焦炭在电炉中还原二氧化硅的化学方程式为
(2)利用氢氟酸刻蚀玻璃的化学方程式为
(3)硅酸钠转化为原硅酸的离子方程式
(4)二氧化硅与烧碱溶液反应的化学方程式
(5)石英与纯碱在玻璃熔炉里加强热发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)①写出NH3的电子式___________ ;
②写出光导纤维主要成分的化学式___________ 。
(2)浓硝酸需要避光保存在棕色试剂瓶的原因是(请用化学方程式表达)___________ 。
(3)氢氧化钠溶液不能用玻璃塞的原因是(请用离子方程式表达)___________ 。
②写出光导纤维主要成分的化学式
(2)浓硝酸需要避光保存在棕色试剂瓶的原因是(请用化学方程式表达)
(3)氢氧化钠溶液不能用玻璃塞的原因是(请用离子方程式表达)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ ;乘务员使用的无线通话机的芯片材料是___________ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与二氧化硅反应的化学方程式___________ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式___________ 。
(5)Na2SiO3溶液俗称___________ 。工业上常用2C+SiO2 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是___________ (填化学式),氧化剂是___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与二氧化硅反应的化学方程式
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式
(5)Na2SiO3溶液俗称
 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)在下列物质中,可以导电的是_______ (填序号,下同),是电解质的有_______ 。
① 晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨
晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨
(2)某气体在标准状况下的密度为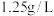 ,则14g该气体所含有的物质的量为
,则14g该气体所含有的物质的量为_______ 。
(3)从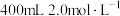 的
的 溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中
溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中 的物质的量浓度为
的物质的量浓度为_______  。
。
(4)已知 与
与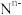 具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为_______ 。
(1)在下列物质中,可以导电的是
①
 晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨
晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨(2)某气体在标准状况下的密度为
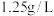 ,则14g该气体所含有的物质的量为
,则14g该气体所含有的物质的量为(3)从
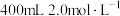 的
的 溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中
溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中 的物质的量浓度为
的物质的量浓度为 。
。(4)已知
 与
与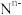 具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】
(1).实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):______________________________ ;玻璃试剂瓶不能盛放氢氟酸的原因是(用化学方程式表示):_____________________________________ 。
(2).实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,则形成沉淀的离子方程式是___________________________ 。取瓶中的上层清液加入稀盐酸,观察到既有气泡产生又有沉淀生成,其离子方程式分别为_____________________________________ 。用Na2SiO3溶液浸泡过的棉花不易燃烧,体现Na2SiO3的用途可做___________________ 的原料。
(3).某溶液中有NH4+、Mg2+、Fe2+、Fe3+、Al3+五种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是__________ ,有所增加的阳离子是___________ 。
A. NH4+ B. Mg2+ C. Fe2+ D. Al3+ E. Fe3+
(4).质量相同的H216O和D216O所含质子数之比为_______________ , 中子数之比为____________ 。
(5).A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为__________________ 。
(1).实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):
(2).实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,则形成沉淀的离子方程式是
(3).某溶液中有NH4+、Mg2+、Fe2+、Fe3+、Al3+五种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A. NH4+ B. Mg2+ C. Fe2+ D. Al3+ E. Fe3+
(4).质量相同的H216O和D216O所含质子数之比为
(5).A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】四种晶体的熔点数据如表:
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,原因是___________ 。
| 物质 | CF4 | SiF4 | BF3 | AlF3 |
| 相对分子质量 | -183 | -90 | -127 | >1000 |
您最近一年使用:0次
【推荐2】完成下列填空:
(一)下列 8 组物质或粒子:
①14N 和 14C ②16O 和 18O ③氰酸铵(NH4CNO)与尿素[CO(NH2)2] ④足球烯(C60)和金刚石 ⑤CH3CH2CH2CH3 和 CH(CH3)3 ⑥CH3CH2CH3 和 CH3(CH2)2CH3 ⑦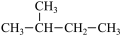 和
和 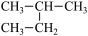 ⑧
⑧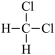 和
和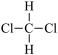
(1)互为同素异形体的是__________ (填编号,下同);
(2)互为同位素的是________________ ;
(3)互为同系物的是___________ ;
(4)互为同分异构体的是________________ 。
(二)有下列几种晶体:
A、水晶 B、冰醋酸 C、白磷 D、金刚石 E、晶体氩 F、干冰 G、氟化钠 H、过氧化钠
(1)属于原子晶体的化合物是__________________ (填序号,下同);
(2)含有共价键的离子晶体是________________________ ;
(3)受热融化时需要克服共价键的晶体是_________________________ ;
(4)写出下列物质的电子式:过氧化钠_____________ ,二氧化碳________________ 。
(三)某烷烃的结构简式为: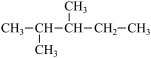
(1)用系统命名法命名该烃:__________________________ ;
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构可能有________ 种(不包括立体异构,下同);
(3)若该烷烃是由炔烃加氢得到的,则原快烃的结构有_________________ 种;
(4)该烷烃在光照条件下与氯气反应,生成的一氧代烷最多有____________ 种。
(四)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。 当把 0.4mol 液态肼和0.8mol H2O2 混合反应,生成氮气和水蒸气,放出 256.7KJ 的热量(相当于 25℃、101 kPa 下测得的热量)。
①反应的热化学方程式为________________________________ ;
②已知 H2O(1)=H2O(g) ΔH=+44kJ/mol。
则 16g 液态肼与液态双氧水反应生成液态水时放出的热量是_________________ kJ;
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是____________ 。
(一)下列 8 组物质或粒子:
①14N 和 14C ②16O 和 18O ③氰酸铵(NH4CNO)与尿素[CO(NH2)2] ④足球烯(C60)和金刚石 ⑤CH3CH2CH2CH3 和 CH(CH3)3 ⑥CH3CH2CH3 和 CH3(CH2)2CH3 ⑦
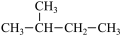 和
和 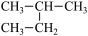 ⑧
⑧ 和
和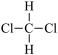
(1)互为同素异形体的是
(2)互为同位素的是
(3)互为同系物的是
(4)互为同分异构体的是
(二)有下列几种晶体:
A、水晶 B、冰醋酸 C、白磷 D、金刚石 E、晶体氩 F、干冰 G、氟化钠 H、过氧化钠
(1)属于原子晶体的化合物是
(2)含有共价键的离子晶体是
(3)受热融化时需要克服共价键的晶体是
(4)写出下列物质的电子式:过氧化钠
(三)某烷烃的结构简式为:
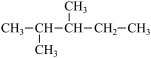
(1)用系统命名法命名该烃:
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构可能有
(3)若该烷烃是由炔烃加氢得到的,则原快烃的结构有
(4)该烷烃在光照条件下与氯气反应,生成的一氧代烷最多有
(四)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。 当把 0.4mol 液态肼和0.8mol H2O2 混合反应,生成氮气和水蒸气,放出 256.7KJ 的热量(相当于 25℃、101 kPa 下测得的热量)。
①反应的热化学方程式为
②已知 H2O(1)=H2O(g) ΔH=+44kJ/mol。
则 16g 液态肼与液态双氧水反应生成液态水时放出的热量是
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次

 H、
H、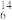 C、
C、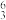 Li、
Li、 Mg、
Mg、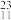 Na、
Na、 N、
N、 Li。其中表示核素的符号共
Li。其中表示核素的符号共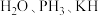 按熔点由高到低的顺序排列为
按熔点由高到低的顺序排列为

