(1).实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):
(2).实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,则形成沉淀的离子方程式是
(3).某溶液中有NH4+、Mg2+、Fe2+、Fe3+、Al3+五种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A. NH4+ B. Mg2+ C. Fe2+ D. Al3+ E. Fe3+
(4).质量相同的H216O和D216O所含质子数之比为
(5).A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为
更新时间:2018-04-07 08:12:02
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某无色溶液中,已知含有H+、Mg2+、 、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示
、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示_______ (用尺子作图,标出数量关系)。
 、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示
、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有 、
、 、
、 、
、 、
、 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
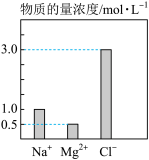
步骤一:仔细观察,该溶液呈无色、透明、均一状态:
步骤二:加入足量 溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除图中的离子外,肯定还含有的离子是_______ ,肯定不含有的离子是_______ 。
(2)步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、干燥。检验沉淀已洗干净的方法是_______ 。
(3)原溶液中 物质的量浓度为
物质的量浓度为_______ mol/L。
(4)向原溶液中加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ 。
(5)若向100mL原溶液中加入1mol/L的 溶液,当生成的沉淀质量刚好最大时,加入的
溶液,当生成的沉淀质量刚好最大时,加入的 溶液体积为
溶液体积为_______ L。
 、
、 、
、 、
、 、
、 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
步骤一:仔细观察,该溶液呈无色、透明、均一状态:
步骤二:加入足量
 溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。(1)原溶液中除图中的离子外,肯定还含有的离子是
(2)步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、干燥。检验沉淀已洗干净的方法是
(3)原溶液中
 物质的量浓度为
物质的量浓度为(4)向原溶液中加入
 溶液,反应的离子方程式为
溶液,反应的离子方程式为(5)若向100mL原溶液中加入1mol/L的
 溶液,当生成的沉淀质量刚好最大时,加入的
溶液,当生成的沉淀质量刚好最大时,加入的 溶液体积为
溶液体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答问题
(1)现有以下物质:①NaCl固体;②CO2;③液态醋酸;④石墨棒;⑤盐酸;⑥酒精(C2H5OH)⑦熔融K2SO4;请回答下列问题(用序号填写);
其中能导电的是___________ ;属于电解质的是 ___________ ;属于非电解质的是 ___________ 。
(2)某河道两旁有甲、乙两厂。它们排放的工业废水中,共含 K+、Ag+、Cu2+、OH-、Cl-和 六种离子。
六种离子。
①甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子是___________ ;
②乙厂的废水中含有另外三种离子。如果加一定量___________ (选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属___________  填写金属元素符号
填写金属元素符号 。
。
③另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的___________  填写离子符号
填写离子符号 转化为沉淀。经过滤后的废水主要含
转化为沉淀。经过滤后的废水主要含___________ ,可用来浇灌农田。
(1)现有以下物质:①NaCl固体;②CO2;③液态醋酸;④石墨棒;⑤盐酸;⑥酒精(C2H5OH)⑦熔融K2SO4;请回答下列问题(用序号填写);
其中能导电的是
(2)某河道两旁有甲、乙两厂。它们排放的工业废水中,共含 K+、Ag+、Cu2+、OH-、Cl-和
 六种离子。
六种离子。①甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子是
②乙厂的废水中含有另外三种离子。如果加一定量
 填写金属元素符号
填写金属元素符号 。
。③另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的
 填写离子符号
填写离子符号 转化为沉淀。经过滤后的废水主要含
转化为沉淀。经过滤后的废水主要含
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
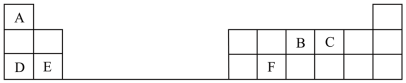
请填写下列空白:
(1)A与B形成 的电子式为
的电子式为________ ;C的原子结构示意图为________ 。
(2)B的最高价氧化物对应的水化物的化学式为_______ ;D、E的最高价氧化物对应的水化物中碱性较弱的是_______  用化学式表示
用化学式表示 ;
;
(3)F的氧化物与氢氧化钠溶液反应的离子方程式为______________ 。

请填写下列空白:
(1)A与B形成
 的电子式为
的电子式为(2)B的最高价氧化物对应的水化物的化学式为
 用化学式表示
用化学式表示 ;
; (3)F的氧化物与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答下列问题:
(1) 个
个 分子的质量为
分子的质量为_______ g。
(2)常温下可用铁槽车运输浓硫酸,原因是_______ 。
(3)氯气可用于制备“战略金属”钛,有关反应为: ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目_______ 。
(4)氯气发生泄漏时,人员应_______ (填字母);同时喷 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为_______ 。
a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用_______ (填“玻璃”或“橡胶”)塞。
(1)
 个
个 分子的质量为
分子的质量为(2)常温下可用铁槽车运输浓硫酸,原因是
(3)氯气可用于制备“战略金属”钛,有关反应为:
 ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目(4)氯气发生泄漏时,人员应
 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放
 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是___________ (填化学式)。
(2)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,用化学方程式说明原因___________ 。
(3)工业上可利用水玻璃( )和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式
)和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式___________ 。
(4)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现。已知主族元素“类硅”的最高化合价为+4价,其最高价氧化物对应的水化物为两性氢氧化物。写出“类硅”在元素周期表中的位置___________ 。
(5)在元素周期表中,硒(Se)位于第4周期,与O同主族。下列关于Se的推断中,正确的是___________ (填序号)。
①原子的最外层电子数为6
②元素的非金属性:Se>O
③原子半径:Se>S
④最高价氧化物对应的水化物酸性: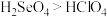
(1)可用于制作计算机芯片和太阳能电池的是
(2)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,用化学方程式说明原因
(3)工业上可利用水玻璃(
 )和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式
)和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式(4)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现。已知主族元素“类硅”的最高化合价为+4价,其最高价氧化物对应的水化物为两性氢氧化物。写出“类硅”在元素周期表中的位置
(5)在元素周期表中,硒(Se)位于第4周期,与O同主族。下列关于Se的推断中,正确的是
①原子的最外层电子数为6
②元素的非金属性:Se>O
③原子半径:Se>S
④最高价氧化物对应的水化物酸性:
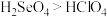
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质属于硅酸盐材料的是 。
(2) 是玻璃的主要成分之一,
是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程为
与氢氧化钠溶液反应的化学方程为_____________ 。工艺师常用___________ (填物质名称)来雕刻玻璃。
(3)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。 可由
可由 与纯碱混合高温熔融反应制得,方程式为
与纯碱混合高温熔融反应制得,方程式为____________ ,高温熔融纯碱时下列坩埚可选___________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)工业制备硅单质方程式____________________ ,该反应中氧化剂是______________ 。
(5)根据如图所示装置回答以下问题。 ,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀
,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀 ②稀盐酸 ③碳酸钙 ④
②稀盐酸 ③碳酸钙 ④ 溶液 ⑤
溶液 ⑤ 。试剂A与C分别为
。试剂A与C分别为_____ (填序号);试管中发生反应的离子方程式为__________________ 。有同学认为此实验不能说明酸性强弱,你认为原因是_______________________ 。
(1)下列物质属于硅酸盐材料的是 。
| A.陶瓷 | B.玻璃 | C.水泥 | D.生石灰 |
(2)
 是玻璃的主要成分之一,
是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程为
与氢氧化钠溶液反应的化学方程为(3)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作 可由
可由 与纯碱混合高温熔融反应制得,方程式为
与纯碱混合高温熔融反应制得,方程式为A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)工业制备硅单质方程式
(5)根据如图所示装置回答以下问题。

 ,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀
,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀 ②稀盐酸 ③碳酸钙 ④
②稀盐酸 ③碳酸钙 ④ 溶液 ⑤
溶液 ⑤ 。试剂A与C分别为
。试剂A与C分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)在 CO、CO2、SO2、NO、NO2、SiO2中,属于酸性氧化物的是__________ ,能导致酸雨的是___________ 。
(2)硅酸钠是为数不多的溶于水的硅酸盐,向硅酸钠溶液中通入足量CO2有白色沉淀产生,写出该反应的离子反应方程式:____________________ 。
(3)有如下反应(未配平):BrF3+H2O→Br2+O2+HBrO3+HF,已知生成物中Br2与O2的物质的量之比为1∶1。则:
①配平后H2O与HF物质的量之比为___________ ;
②还原剂为______________ ;
③如有5mol H2O参加反应,则参加氧化还原反应的H2O物质的量为_______________ mol。
(1)在 CO、CO2、SO2、NO、NO2、SiO2中,属于酸性氧化物的是
(2)硅酸钠是为数不多的溶于水的硅酸盐,向硅酸钠溶液中通入足量CO2有白色沉淀产生,写出该反应的离子反应方程式:
(3)有如下反应(未配平):BrF3+H2O→Br2+O2+HBrO3+HF,已知生成物中Br2与O2的物质的量之比为1∶1。则:
①配平后H2O与HF物质的量之比为
②还原剂为
③如有5mol H2O参加反应,则参加氧化还原反应的H2O物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题.
(1)久置的硅酸钠溶液会出现浑浊现象其原因为________ (用化学方程式表示)
(2)红热的木炭与浓硫酸反应的化学方程式________
(3)SO2催化氧化成SO3的化学方程式:________
(4)写出铜与稀硝酸反应的离子方程式________
(5)实验室制取氨气的化学方程式为________ ,常用________ 来干燥氨气.
(6)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是________ ,还原产物是_______ .
②氧化剂与氧化产物的物质的量比是________ 。
(1)久置的硅酸钠溶液会出现浑浊现象其原因为
(2)红热的木炭与浓硫酸反应的化学方程式
(3)SO2催化氧化成SO3的化学方程式:
(4)写出铜与稀硝酸反应的离子方程式
(5)实验室制取氨气的化学方程式为
(6)根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是
②氧化剂与氧化产物的物质的量比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g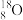 中含有的中子数为NA
中含有的中子数为NA
D.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g
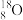 中含有的中子数为NA
中含有的中子数为NAD.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)自然界中存在的碘的稳定性核素是碘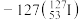 。某次核电站事故释放出的放射性物质中含有人工放射性核素碘
。某次核电站事故释放出的放射性物质中含有人工放射性核素碘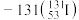 。碘
。碘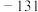 一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是
一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是______ (填序号)。
A. 和
和 原子核外的价电子排布不同
原子核外的价电子排布不同
B. 和
和 互为同位素
互为同位素
C. 原子的核外电子排布式中只有1个能级上未充满电子
原子的核外电子排布式中只有1个能级上未充满电子
D. 的中子数与质子数之差为74
的中子数与质子数之差为74
(2)有四种短周期元素,它们的结构、性质等信息如下表所示:
① 元素原子的核外电子排布式为
元素原子的核外电子排布式为______ 。
②离子半径:
______ (填“ ”或“
”或“ ”)
”) 。
。
③ 元素原子的核外电子排布图为
元素原子的核外电子排布图为______ ,其原子核外有______ 个未成对电子,能量最高的电子为______ 轨道上的电子,该轨道呈______ 形。
④写出 、
、 两元素的最高价氧化物对应的水化物反应的离子方程式:
两元素的最高价氧化物对应的水化物反应的离子方程式:______ 。
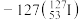 。某次核电站事故释放出的放射性物质中含有人工放射性核素碘
。某次核电站事故释放出的放射性物质中含有人工放射性核素碘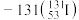 。碘
。碘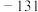 一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是
一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是A.
 和
和 原子核外的价电子排布不同
原子核外的价电子排布不同B.
 和
和 互为同位素
互为同位素C.
 原子的核外电子排布式中只有1个能级上未充满电子
原子的核外电子排布式中只有1个能级上未充满电子D.
 的中子数与质子数之差为74
的中子数与质子数之差为74(2)有四种短周期元素,它们的结构、性质等信息如下表所示:
| 元素 | 结构、性质等信息 |
| A | 是短周期元素中(除稀有气体外)第一电离能最小的元素,该元素单质的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时可用作制冷剂 |
| D | 原子核外电子共有17种不同的运动状态 |
①
 元素原子的核外电子排布式为
元素原子的核外电子排布式为②离子半径:

 ”或“
”或“ ”)
”) 。
。③
 元素原子的核外电子排布图为
元素原子的核外电子排布图为④写出
 、
、 两元素的最高价氧化物对应的水化物反应的离子方程式:
两元素的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】碘(I)在元素周期表中位于ⅦA族,是人体必需的微量元素之一。
(1) 可用于治疗甲亢。
可用于治疗甲亢。 的原子核内中子数为
的原子核内中子数为___________ 。
(2)①碘元素的非金属性比氯元素的弱,其原因是由于同主族元素从上到下原子核外电子层数依次增多,___________ 逐渐增大,___________ 能力逐渐减弱。
②下列事实能够用“碘的非金属性比氯的弱”来解释的是___________ (填序号)。
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c. 与
与 的化合比
的化合比 与
与 的化合更容易
的化合更容易
(3)氢碘酸是HI的水溶液,是一种酸性比盐酸强的酸。
资料:ⅰ.盐酸和氢碘酸均可使氢氧化铁溶解,后者得到的产物中含有 。
。
ⅱ.KI溶液不能溶解氢氧化铁,KI溶液与 溶液反应的产物中含有
溶液反应的产物中含有 。
。
①盐酸与氢氧化铁发生反应的离子方程式是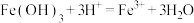 ;氢碘酸与氢氧化铁发生反应的离子方程式是
;氢碘酸与氢氧化铁发生反应的离子方程式是___________ 。
②结合上述资料,由物质性质解释①中两反应的异同:___________ 。
(1)
 可用于治疗甲亢。
可用于治疗甲亢。 的原子核内中子数为
的原子核内中子数为(2)①碘元素的非金属性比氯元素的弱,其原因是由于同主族元素从上到下原子核外电子层数依次增多,
②下列事实能够用“碘的非金属性比氯的弱”来解释的是
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c.
 与
与 的化合比
的化合比 与
与 的化合更容易
的化合更容易(3)氢碘酸是HI的水溶液,是一种酸性比盐酸强的酸。
资料:ⅰ.盐酸和氢碘酸均可使氢氧化铁溶解,后者得到的产物中含有
 。
。ⅱ.KI溶液不能溶解氢氧化铁,KI溶液与
 溶液反应的产物中含有
溶液反应的产物中含有 。
。①盐酸与氢氧化铁发生反应的离子方程式是
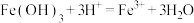 ;氢碘酸与氢氧化铁发生反应的离子方程式是
;氢碘酸与氢氧化铁发生反应的离子方程式是②结合上述资料,由物质性质解释①中两反应的异同:
您最近一年使用:0次



