按要求回答下列问题:
(1) 个
个 分子的质量为
分子的质量为_______ g。
(2)常温下可用铁槽车运输浓硫酸,原因是_______ 。
(3)氯气可用于制备“战略金属”钛,有关反应为: ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目_______ 。
(4)氯气发生泄漏时,人员应_______ (填字母);同时喷 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为_______ 。
a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用_______ (填“玻璃”或“橡胶”)塞。
(1)
 个
个 分子的质量为
分子的质量为(2)常温下可用铁槽车运输浓硫酸,原因是
(3)氯气可用于制备“战略金属”钛,有关反应为:
 ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目(4)氯气发生泄漏时,人员应
 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放
 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用
更新时间:2022-02-21 08:13:22
|
相似题推荐
【推荐1】已知反应:
①
②
③
④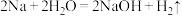
⑤









回答下列问题:
(1)上述反应中,属于置换反应的是___________ (填序号,下同);同一元素之间发生氧化还原反应的是___________ 。
(2)反应②中氧化剂是___________ (填化学式,下同);反应③中氧化产物是___________ 。
(3)在反应④中,每生成1个 分子时,转移的电子数为
分子时,转移的电子数为___________
(4)配平反应⑤,并用双线桥法标出反应中电子转移的方向和数目___________ 。
(5)反应⑤中 表现的性质有
表现的性质有___________ 。
(6)已知有下列两个反应:① ;②
;②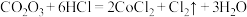 ,
, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
①

②

③

④
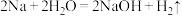
⑤










回答下列问题:
(1)上述反应中,属于置换反应的是
(2)反应②中氧化剂是
(3)在反应④中,每生成1个
 分子时,转移的电子数为
分子时,转移的电子数为(4)配平反应⑤,并用双线桥法标出反应中电子转移的方向和数目
(5)反应⑤中
 表现的性质有
表现的性质有(6)已知有下列两个反应:①
 ;②
;②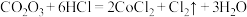 ,
, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是____________ 。
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为____________ 。
(3)根据上述反应可推知___________ 。
a.氧化性:H3AsO4>KBrO3
b.氧化性:KBrO3>H3AsO4
c.还原性:X>AsH3
d.还原性:AsH3>X
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目___________
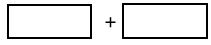
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
(3)根据上述反应可推知
a.氧化性:H3AsO4>KBrO3
b.氧化性:KBrO3>H3AsO4
c.还原性:X>AsH3
d.还原性:AsH3>X
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生如下反应: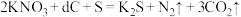 。其中作氧化剂的是
。其中作氧化剂的是___________ (填化学式)。
(2)中国古代著作中有“银针验毒”的记录,其原理为: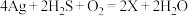 ,则
,则 的化学式是
的化学式是_______ ,其中 在该反应中
在该反应中_______ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

(1)Ⅰ中铁丝上观察到的现是___________ 。
(2)写出Ⅱ中发生反应的离子方程是___________ 。
(3)结合Ⅰ、Ⅱ实验现象可知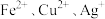 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(4)已知 可发生反应:
可发生反应: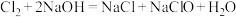 。
。
①该反应中氧化剂是___________ (填化学式,下同),还原剂是_______ 。
②用双线桥法标出电子转移的数目和方向:___________ 。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生如下反应:
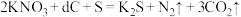 。其中作氧化剂的是
。其中作氧化剂的是(2)中国古代著作中有“银针验毒”的记录,其原理为:
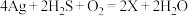 ,则
,则 的化学式是
的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

(1)Ⅰ中铁丝上观察到的现是
(2)写出Ⅱ中发生反应的离子方程是
(3)结合Ⅰ、Ⅱ实验现象可知
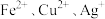 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(4)已知
 可发生反应:
可发生反应: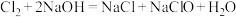 。
。①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)实验室里可以用KMnO4与浓盐酸反应制取氯气,其反应的离子方程式为: ________
(2)某温度下,将Cl2通入NaOH 溶液中,反应得到含有C1O-与C1O3-物质的量之比为1: 1的混合液,
反应的化学方程式是________________________ 。
(3)“流感”成为2017 年冬季最可怕的流行病,历城二中要求每班每天必须用“84”消毒液进行消
毒,已知某品牌“84”消毒液的有效成分为NaClO,写出向该溶液中通入过量的CO2所发生的有关离子方程式________________________
(4)氰(CN) 2的化学性质和卤素(X2) 很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:_______
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当
于多少克Cl2的氧化能力。NaClO2的有效氯含量为_________ 。(计算结果保留两位小数)
(2)某温度下,将Cl2通入NaOH 溶液中,反应得到含有C1O-与C1O3-物质的量之比为1: 1的混合液,
反应的化学方程式是
(3)“流感”成为2017 年冬季最可怕的流行病,历城二中要求每班每天必须用“84”消毒液进行消
毒,已知某品牌“84”消毒液的有效成分为NaClO,写出向该溶液中通入过量的CO2所发生的有关离子方程式
(4)氰(CN) 2的化学性质和卤素(X2) 很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式:
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当
于多少克Cl2的氧化能力。NaClO2的有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有A、B、C三种气体,A是密度最小的气体,B在通常情况下呈黄绿色,纯净的A可以在B中安静地燃烧生成C。把气体B通入到适量石灰乳中可以得到白色浑浊物D。请据此回答下列问题:
(1)写出下列各反应的化学方程式
①实验室制备气体B:______
②将气体B通入到适量石灰乳中:__________
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是________ (用字母表示)。
(3)将白色浑浊物D溶于水得到澄清溶液,
①向澄清溶液中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为___________
②白色浑浊物D因具有漂白性又称为________ ,该物质在空气中容易变质的原因为(用化学方程式表示)_____________
(1)写出下列各反应的化学方程式
①实验室制备气体B:
②将气体B通入到适量石灰乳中:
(2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是
(3)将白色浑浊物D溶于水得到澄清溶液,
①向澄清溶液中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为
②白色浑浊物D因具有漂白性又称为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用 和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
(1) Ca(ClO)2中Cl元素的化合价是___________ ;工业上将氯气制成漂白粉的主要目的是___________ 。工业上制成漂白粉的化学方程式:___________ 。
(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是___________(填字母)。
(3)浸泡衣物时加入漂粉精(有效成分Ca(ClO)2)在空气中放置一段时间漂白效果更好,请用化学方程式解释原因:___________ 。
(4)若将漂白液(有效成分NaClO)与洁厕灵(主要成分是盐酸)混合使用,则会产生有毒气体,其反应的离子方程式是___________ 。
(5)有效氯是漂白粉中有效成分Ca(ClO)2含量大小的标志。
已知:①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
②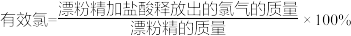 。
。
若某漂粉精的有效氯为60%,该漂粉精中Ca(ClO)2的质量分数为___________ (计算结果保留一位小数)。
 和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
和碱制漂白粉、漂粉精及漂白液。请回答下列问题:(1) Ca(ClO)2中Cl元素的化合价是
(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是___________(填字母)。
| A.生石灰 | B.漂白粉 |
| C.NaOH | D. |
(4)若将漂白液(有效成分NaClO)与洁厕灵(主要成分是盐酸)混合使用,则会产生有毒气体,其反应的离子方程式是
(5)有效氯是漂白粉中有效成分Ca(ClO)2含量大小的标志。
已知:①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
②
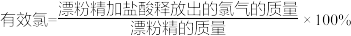 。
。若某漂粉精的有效氯为60%,该漂粉精中Ca(ClO)2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某化学学习小组设计通过以下步骤用铜丝和硫酸制取胆矾晶体:

(1)固体A为___ 色;胆矾的化学式为___ 。
(2)为加快反应②,可采取的实验方法是___ (写出一种即可)。
(3)操作①、操作②的具体实验操作名称是___ 。
(4)有同学提出可以将反应①和反应②合并,也就是将铜丝与浓硫酸直接混合加热即可得到蓝色溶液。该同学所提方案不足之处是__ (写出一种即可)。

(1)固体A为
(2)为加快反应②,可采取的实验方法是
(3)操作①、操作②的具体实验操作名称是
(4)有同学提出可以将反应①和反应②合并,也就是将铜丝与浓硫酸直接混合加热即可得到蓝色溶液。该同学所提方案不足之处是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列各过程主要表现了浓硫酸的哪些性质?请将答案的序号分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体___________ 。
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸___________ 。
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体___________ 。
(4)常温下可以用铁或铝的容器贮存浓硫酸___________ 。
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末___________ 。
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体___________ 。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体
(4)常温下可以用铁或铝的容器贮存浓硫酸
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)①写出NH3的电子式___________ ;
②写出光导纤维主要成分的化学式___________ 。
(2)浓硝酸需要避光保存在棕色试剂瓶的原因是(请用化学方程式表达)___________ 。
(3)氢氧化钠溶液不能用玻璃塞的原因是(请用离子方程式表达)___________ 。
②写出光导纤维主要成分的化学式
(2)浓硝酸需要避光保存在棕色试剂瓶的原因是(请用化学方程式表达)
(3)氢氧化钠溶液不能用玻璃塞的原因是(请用离子方程式表达)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)下列物质不含有硅酸盐的是____ 。
A.陶瓷 B.金刚砂 C.水泥 D.碳纳米管 E.玻璃 F.富勒烯
(2)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因____ ,工艺师常用____ (填物质名称)来雕刻玻璃。
(3)绿柱石(绿宝石矿藏的主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO•Al2O3•6SiO2,其n值为____ 。
(4)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作____ 。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是____ (填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(1)下列物质不含有硅酸盐的是
A.陶瓷 B.金刚砂 C.水泥 D.碳纳米管 E.玻璃 F.富勒烯
(2)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因
(3)绿柱石(绿宝石矿藏的主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO•Al2O3•6SiO2,其n值为
(4)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】分金属在现代社会中发挥着巨大的作用,铝的化合物在工农业生产及人们的日常生活中也具有广泛地作用。
(1)若将铝溶解,下列试剂中最好选用________ (填选项字母)。
A.浓硫酸B.稀硫酸C.稀硝酸
(2)以铝土矿(主要成分是Al2O3,杂质有SiO2、Fe2O3等)为原料,采用拜耳法生产Al2O3的流程如下图所示:
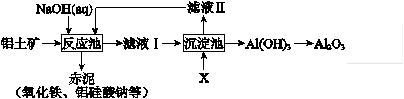
①Al2O3可用于电解制Al,电解时需加入冰晶石(Na3AlF6)作为助熔剂,用NaF和Al2(SO4)3反应制备冰晶石的化学方程式为________________ ;电解时用石墨作阳极,温度维持在950~970℃,阳极需定期更换,其原因为________________________ 。
②赤泥中铝硅酸钠的化学式可表示为:3Na2O·3Al2O3·5SiO2·5H2O,则滤液I的主要成分是________________ ;铝土矿的品位常用铝硅比(A/S,即矿石中Al2O3与SiO2的质量比)来衡量。某种铝土矿的A/S=10.2,则加入足量NaOH溶液后铝的理论溶出率为________________ 。
③该生产过程中,需向沉淀池中加入过量的X,该反应的离子方程式为________________ 。
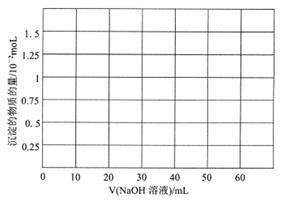
(3)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式____ ,Be(OH)2溶于NaOH溶液的化学方程式为:Be(OH)2+2NaOH=Na2BeO2+2H2O,往10.0mL1.00mol·L-1的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加入量的变化图_______ :
(1)若将铝溶解,下列试剂中最好选用
A.浓硫酸B.稀硫酸C.稀硝酸
(2)以铝土矿(主要成分是Al2O3,杂质有SiO2、Fe2O3等)为原料,采用拜耳法生产Al2O3的流程如下图所示:

①Al2O3可用于电解制Al,电解时需加入冰晶石(Na3AlF6)作为助熔剂,用NaF和Al2(SO4)3反应制备冰晶石的化学方程式为
②赤泥中铝硅酸钠的化学式可表示为:3Na2O·3Al2O3·5SiO2·5H2O,则滤液I的主要成分是
③该生产过程中,需向沉淀池中加入过量的X,该反应的离子方程式为
(3)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式

您最近一年使用:0次



