如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时 掉入水中。回答下列问题:
掉入水中。回答下列问题:
(1)钠与水反应的现象有很多,不同的现象证明不同的性质。

①能证明钠的密度比水小的现象是__________ 。
②能证明钠的熔点低的现象是__________ 。
③能证明有氢氧化钠生成的现象是____________________ 。
④能证明有气体产生的现象是A端液面__________ (填“上升”“下降”或“不变”,下同),B端液面____________________ 。
(2)除杂
① 气体混有
气体混有 杂质,除杂试剂是
杂质,除杂试剂是____________________ 。
② 溶液混有
溶液混有 杂质,除杂试剂是
杂质,除杂试剂是____________________ ,离子方程式____________________ 。
 掉入水中。回答下列问题:
掉入水中。回答下列问题:(1)钠与水反应的现象有很多,不同的现象证明不同的性质。

①能证明钠的密度比水小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
④能证明有气体产生的现象是A端液面
(2)除杂
①
 气体混有
气体混有 杂质,除杂试剂是
杂质,除杂试剂是②
 溶液混有
溶液混有 杂质,除杂试剂是
杂质,除杂试剂是
更新时间:2024-01-27 22:29:37
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】以不同类别物质间转化为线索,认识钠及其化合物。请回答下列问题:
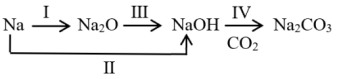
(1)转化Ⅰ的产物 属于
属于_______ (填“酸”或“碱”)性氧化物。
(2)若改变转化Ⅰ的反应条件,可得到钠的另一种氧化物 ,写出其与
,写出其与 反应的化学方程式
反应的化学方程式_______ 。
(3)某同学为探究转化Ⅱ,将钠投入足量水中,记录了如下实验现象和实验结论:①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低。

补齐下表(从①~⑧中选择,填序号):
写出转化Ⅱ中反应的化学方程式_______ 。
(4)某同学设计了如下两个对照实验,对比碳酸钠与碳酸氢钠热稳定性的差异。
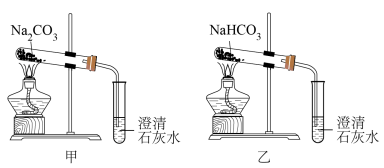
通过实验,该同学得出结论,热稳定性: 。该同学依据的现象是
。该同学依据的现象是_______ 。

(1)转化Ⅰ的产物
 属于
属于(2)若改变转化Ⅰ的反应条件,可得到钠的另一种氧化物
 ,写出其与
,写出其与 反应的化学方程式
反应的化学方程式(3)某同学为探究转化Ⅱ,将钠投入足量水中,记录了如下实验现象和实验结论:①有碱生成 ②溶液变红 ③钠四处游动 ④钠浮在水面上 ⑤有气体产生 ⑥钠的密度比水小 ⑦钠熔成光亮的小球 ⑧反应放热,钠熔点低。

补齐下表(从①~⑧中选择,填序号):
| 实验现象 | ④ | ③ | ② | |
| 实验结论 | ⑧ | ⑤ |
(4)某同学设计了如下两个对照实验,对比碳酸钠与碳酸氢钠热稳定性的差异。

通过实验,该同学得出结论,热稳定性:
 。该同学依据的现象是
。该同学依据的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)某课外活动小组研究金属钾的性质。他们根据物质___ 决定物质性质的思想观念,先分析Na、K原子结构示意图,发现它们在原子结构上共同的特点是___ ,知道了Na、K属于同一类物质,并且K比Na活泼。在进行K跟硫酸铜溶液反应的实验时,必须要用到的仪器有___ 、小刀、玻璃片、滤纸、___ 。发生的化学反应依次主要有___ ,___ 。
(2)用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到的实验现象是___ ,说明Na2O2和H2O反应的结论是:a.有氧气生成;b.___ 。
研究性学习小组的同学拟用如图装置进行实验,以证明上述结论。
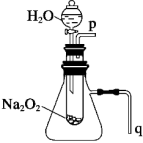
①用以验证结论a的实验操作方法及现象是___ 。
②用以验证结论b的实验__ 。
(3)某实验小组对氯水成分和性质进行研究,实验如图:
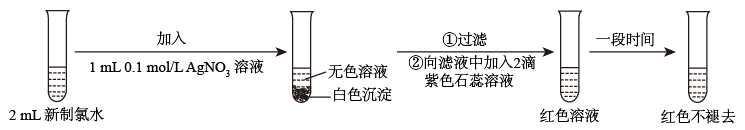
甲同学认为,“红色不褪去”不是因为氯水被稀释所致。乙同学持反对意见。为了证明甲同学错误,乙同学继续以下实验,请在横线上补充所加入的试剂和观察到的现象。
①加入:___ ,现象:___ 。

(1)某课外活动小组研究金属钾的性质。他们根据物质
(2)用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到的实验现象是
研究性学习小组的同学拟用如图装置进行实验,以证明上述结论。

①用以验证结论a的实验操作方法及现象是
②用以验证结论b的实验
(3)某实验小组对氯水成分和性质进行研究,实验如图:

甲同学认为,“红色不褪去”不是因为氯水被稀释所致。乙同学持反对意见。为了证明甲同学错误,乙同学继续以下实验,请在横线上补充所加入的试剂和观察到的现象。
①加入:

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)
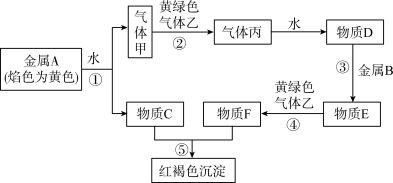
请回答下列问题:
(1)丙的化学式为_______ 。
(2)A的一种氧化物为淡黄色固体,该物质的化学式为_______ 。
(3)写出气体乙与C溶液反应可以制漂白液,该反应的离子方程式为:_______ 。
(4)气体甲与气体乙反应时,则可以观察到的现象是:_______ 。
(5)若将F饱和溶液分别滴入下列物质中加热,能形成胶体的是_______。
(6) 胶体区别于
胶体区别于 溶液最本质的特征是_______。
溶液最本质的特征是_______。

请回答下列问题:
(1)丙的化学式为
(2)A的一种氧化物为淡黄色固体,该物质的化学式为
(3)写出气体乙与C溶液反应可以制漂白液,该反应的离子方程式为:
(4)气体甲与气体乙反应时,则可以观察到的现象是:
(5)若将F饱和溶液分别滴入下列物质中加热,能形成胶体的是_______。
| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
(6)
 胶体区别于
胶体区别于 溶液最本质的特征是_______。
溶液最本质的特征是_______。A. 胶体粒子的直径在1~100nm之间 胶体粒子的直径在1~100nm之间 |
B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 |
D. 胶体的分散质粒子能透过滤纸 胶体的分散质粒子能透过滤纸 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】I.为比较Na2CO3和NaHCO3的热稳定性,某同学设计了如下实验装置。实验时,先检查装置的气密性,再取少量Na2CO3粉末加在大试管的底部,另取少量NaHCO3粉末加在小试管底部。预热后在大试管底部加热。
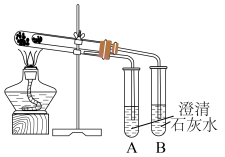
回答下列问题:
(1)小试管中放置___________ 药品(填化学名称)。
(2)开始加热一段时间后,试管___________ (填“A”或“B”)中会出现浑浊现象。实验现象证明,加热条件下,Na2CO3比NaHCO3更___________ (填“稳定”或“不稳定”)。
II.为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下,请回答:
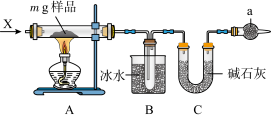
(3)仪器a的名称是___________ 。
(4)装置B中冰水的作用是___________ 。
(5)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的质量分数偏高的是___________。

回答下列问题:
(1)小试管中放置
(2)开始加热一段时间后,试管
II.为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如下,请回答:

(3)仪器a的名称是
(4)装置B中冰水的作用是
(5)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的质量分数偏高的是___________。
| A.样品分解不完全 |
| B.装置B、C之间缺少CO2的干燥装置 |
| C.产生CO2气体的速率太快,没有被碱石灰完全吸收 |
| D.反应完全后停止加热,通入过量的空气 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】根据如图所示装置(部分仪器已略去)回答下列有关问题:

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是___________ (填“I”或“II”),请写出实验甲中较不稳定物质的分解方程式___________ 。
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花着火。写出Na2O2与CO2反应的化学方程式:___________ 。
(3)下列对Na2O2的叙述中,正确的是___________。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花着火。写出Na2O2与CO2反应的化学方程式:
(3)下列对Na2O2的叙述中,正确的是___________。
| A.Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物 |
| B.Na2O2能与水反应,所以Na2O2可以作气体的干燥剂 |
| C.Na2O2与CO2反应时,Na2O2只作氧化剂 |
| D.Na2O2与CO2反应产生氧气,可用于呼吸面具中氧气的来源 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】 是高中化学常见的元素。回答下列问题:
是高中化学常见的元素。回答下列问题:
(1) 、
、 、
、 、
、 久置空气中最终都会变成
久置空气中最终都会变成_______ (填化学式)。
(2)某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
①图1实验在加热过程中能观察到Ⅱ烧杯有白色沉淀产生,则物质_______ (填“A”或“B”)为 ,该物质受热分解的化学方程式为
,该物质受热分解的化学方程式为_______ 。
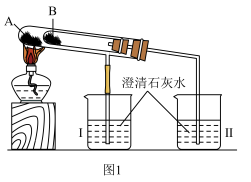
②如图2所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。

ⅰ.两试管中均产生气体,_______ (填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈。
ⅱ.反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是_______ (填字母)。
a.装置Ⅰ的气球体积较大 b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(3)某同学为探究 和
和 与
与 溶液的反应,将两种固体分别配制成
溶液的反应,将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:
实验后,发现操作2的现象与预测有差异,实验过程中产生白色沉淀和气体。则该条件下, 溶液与
溶液与 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为_______ 。
 是高中化学常见的元素。回答下列问题:
是高中化学常见的元素。回答下列问题:(1)
 、
、 、
、 、
、 久置空气中最终都会变成
久置空气中最终都会变成(2)某实验小组欲探究
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。①图1实验在加热过程中能观察到Ⅱ烧杯有白色沉淀产生,则物质
 ,该物质受热分解的化学方程式为
,该物质受热分解的化学方程式为
②如图2所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。

ⅰ.两试管中均产生气体,
ⅱ.反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是
a.装置Ⅰ的气球体积较大 b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(3)某同学为探究
 和
和 与
与 溶液的反应,将两种固体分别配制成
溶液的反应,将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:| 实验方案 | 预测现象 | 预测依据 |
操作1:向  溶液中滴加 溶液中滴加   溶液 溶液 | 有白色沉淀生成 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
操作2:向  溶液中滴加 溶液中滴加   溶液 溶液 | 无明显现象 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应 反应 |
 溶液与
溶液与 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为
您最近一年使用:0次



