锰元素能形成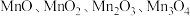 等多种氧化物,其中大颗粒
等多种氧化物,其中大颗粒 是重要的电池材料。工业上以碳酸锰矿(主要成分为
是重要的电池材料。工业上以碳酸锰矿(主要成分为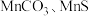 ),和软锰矿(主要成分为
),和软锰矿(主要成分为 )为原料制取
)为原料制取 。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。
。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。
已知: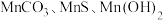 常温下皆为难溶于水的固体,硫化氢
常温下皆为难溶于水的固体,硫化氢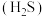 是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
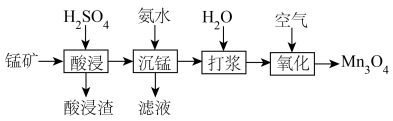
(1)“酸浸”: 溶于硫酸的离子方程式:
溶于硫酸的离子方程式:___________ 。
(2)“打浆”:将所得 制成悬浊液,可加快“氧化”反应速率的原因是
制成悬浊液,可加快“氧化”反应速率的原因是___________ 。
(3)“氧化”所得固体产物中锰元素质量分数随通空气时间的变化如图所示。
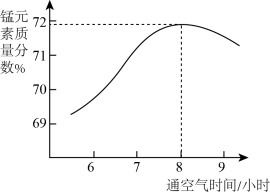
通空气超过8小时,产物中锰元素质量分数减小的原因是___________ 。
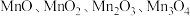 等多种氧化物,其中大颗粒
等多种氧化物,其中大颗粒 是重要的电池材料。工业上以碳酸锰矿(主要成分为
是重要的电池材料。工业上以碳酸锰矿(主要成分为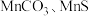 ),和软锰矿(主要成分为
),和软锰矿(主要成分为 )为原料制取
)为原料制取 。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。
。其工艺主要包括“酸浸”“沉锰”“打浆”“氧化”。已知:
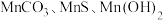 常温下皆为难溶于水的固体,硫化氢
常温下皆为难溶于水的固体,硫化氢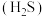 是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
是一种易燃、具有臭鸡蛋气味的有毒气体,有较强的还原性,溶于水得到氢硫酸溶液,是一种比碳酸还弱的酸。
(1)“酸浸”:
 溶于硫酸的离子方程式:
溶于硫酸的离子方程式:(2)“打浆”:将所得
 制成悬浊液,可加快“氧化”反应速率的原因是
制成悬浊液,可加快“氧化”反应速率的原因是(3)“氧化”所得固体产物中锰元素质量分数随通空气时间的变化如图所示。

通空气超过8小时,产物中锰元素质量分数减小的原因是
更新时间:2024-02-02 08:21:27
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铋(Bi)与氮同族,氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、生产金属铋等。一种以用火法炼铜过程产生的铜转炉烟尘(除含铋的化合物之外,还有CuSO4、ZnSO4、CuS、Fe2O3、PbSO4及As2O3)制备高纯氯氧化铋的工艺流程如下:

请回答:
(1)BiOCl中Bi元素的化合价为__________ 。
(2)向“酸浸”所得“浸液1”中加入Zn粉,主要目的是__________________________ 。
(3)“浸铜”时,有单质硫生成,其反应的离子方程式为____________________________ 。
(4)“浸铋”时,温度升高,铋的浸出率降低,其原因为____________________________ 。
(5)“沉铋”时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为__________ 。
(6)“除铅、砷”时,可以采用以下两种方法:
①加入改性羟基磷灰石固体(HAP):浸液2与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表:
实验中应采用的L/S=__________ 。
②铁盐氧化法:向浸液2中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。当溶液中c(AsO43-)=1×10-9 mol/L,且不产生Fe(OH)3沉淀,此时溶液的pH为__________ 。(已知:1g2=0.3;FeAsO4、Fe(OH)3的Ksp分别为5×10-21、4×10-38。)

请回答:
(1)BiOCl中Bi元素的化合价为
(2)向“酸浸”所得“浸液1”中加入Zn粉,主要目的是
(3)“浸铜”时,有单质硫生成,其反应的离子方程式为
(4)“浸铋”时,温度升高,铋的浸出率降低,其原因为
(5)“沉铋”时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为
(6)“除铅、砷”时,可以采用以下两种方法:
①加入改性羟基磷灰石固体(HAP):浸液2与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表:
| L/S | 125∶1 | 50∶1 | 25∶1 | 15∶1 |
| Pb2+去除率/% | 84.86 | 94.15 | 95.40 | 96.83 |
| As3+去除率/% | 98.79 | 98.92 | 98.34 | 99.05 |
| m(沉铋)/g | 2.34 | 2.33 | 2.05 | 1.98 |
实验中应采用的L/S=
②铁盐氧化法:向浸液2中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。当溶液中c(AsO43-)=1×10-9 mol/L,且不产生Fe(OH)3沉淀,此时溶液的pH为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】硫酰氯(SO2Cl2)熔点-54.1℃、沸点69.2℃,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
(1)SO2Cl2中S的化合价为_______ ,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为________________ 。
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(夹持装置未画出)。
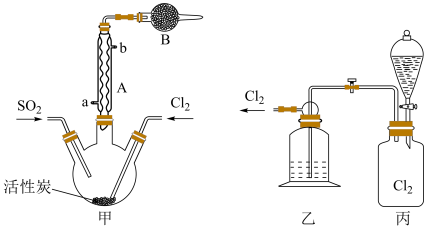
①仪器A的名称为___________ ,装置乙中装入的试剂_____________ ,装置B的作用是_______________________ 。
②装置丙分液漏斗中盛装的最佳试剂是________ (选填字母)。
A.蒸馏水 B.10.0 mol/L浓盐酸
C.浓氢氧化钠溶液 D.饱和食盐水
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。
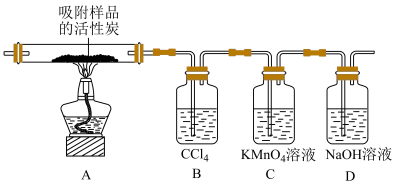
①加热时A中试管出现黄绿色,装置B的作用是____________ 。
②装置C中的现象是___________ ,反应的离子方程式为___________________ 。
(1)SO2Cl2中S的化合价为
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(夹持装置未画出)。

①仪器A的名称为
②装置丙分液漏斗中盛装的最佳试剂是
A.蒸馏水 B.10.0 mol/L浓盐酸
C.浓氢氧化钠溶液 D.饱和食盐水
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。

①加热时A中试管出现黄绿色,装置B的作用是
②装置C中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。室温下,两支试管分别编号①和②,实验数据如下:
试管①中 溶液褪色的速率开始十分缓慢,一段时间后突然加快。请回答:
溶液褪色的速率开始十分缓慢,一段时间后突然加快。请回答:
(1)该反应的离子方程式为_______ 。
(2)为了配制 的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙和
的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙和_______ 、_______ 、_______ 。
(3)该实验结论是_______ 。
(4)实验②选用 固体而不是
固体而不是 固体的原因是
固体的原因是_______ 。
(5)该同学为使实验更加严密,在试管③中做了如下实验,请把实验方案补充完整,并预测褪色时间。
| 实验序号 | ① | ② |
| 加入试剂 |  酸性 酸性 溶液 溶液 溶液 溶液 |  酸性 酸性 溶液 溶液 溶液一粒黄豆粒大的 溶液一粒黄豆粒大的 固体 固体 |
| 褪色时间/s | 116 | 6 |
 溶液褪色的速率开始十分缓慢,一段时间后突然加快。请回答:
溶液褪色的速率开始十分缓慢,一段时间后突然加快。请回答:(1)该反应的离子方程式为
(2)为了配制
 的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙和
的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙和(3)该实验结论是
(4)实验②选用
 固体而不是
固体而不是 固体的原因是
固体的原因是(5)该同学为使实验更加严密,在试管③中做了如下实验,请把实验方案补充完整,并预测褪色时间。
| 实验序号 | ③ |
| 加入试剂 |  酸性 酸性 溶液 溶液 溶液一粒黄豆粒大的 溶液一粒黄豆粒大的 |
| 褪色时间/s |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.某小组学生通过观察反应 中沉淀产生的快慢来定性探究影响化学反应速率的因素,实验数据如下表所示:
中沉淀产生的快慢来定性探究影响化学反应速率的因素,实验数据如下表所示:
(1)a=___________ ℃。
(2)对比实验Ⅰ、Ⅱ,探究___________ (外界因素)对该反应速率的影响。
(3)V=___________ mL,加入VmL水的目的是___________ 。
Ⅱ.某研究小组探究甲烷和氯气的反应情况,实验装置如图所示:
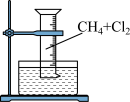
(4)水槽中盛放的液体应为___________ ,其作用为___________ 。
(5)反应片刻后发现量筒内壁上有油状液滴出现,该油状液滴可能是___________ 。
Ⅲ.以太阳能为热源,铁氧化合物循环分解水制H2的过程如图所示:
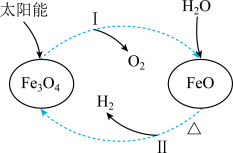
(6)过程Ⅱ的化学方程式为:___________ 。
(7)过程Ⅰ中每消耗1mol 转移
转移___________ mol电子。
 中沉淀产生的快慢来定性探究影响化学反应速率的因素,实验数据如下表所示:
中沉淀产生的快慢来定性探究影响化学反应速率的因素,实验数据如下表所示:| 实验编号 | Na2S2O3 | H2SO4溶液 | 蒸馏水 | |||
| c/(mol/L) | V/mL | c(mol/L) | V/mL | V/mL | T/℃ | |
| Ⅰ | 0.1 | 1 | 0.5 | 1 | V | 30 |
| Ⅱ | 0.1 | 2 | 0.5 | l | 7 | a |
| Ⅲ | 0.1 | 2 | 0.5 | 1 | 7 | 40 |
(2)对比实验Ⅰ、Ⅱ,探究
(3)V=
Ⅱ.某研究小组探究甲烷和氯气的反应情况,实验装置如图所示:

(4)水槽中盛放的液体应为
(5)反应片刻后发现量筒内壁上有油状液滴出现,该油状液滴可能是
Ⅲ.以太阳能为热源,铁氧化合物循环分解水制H2的过程如图所示:

(6)过程Ⅱ的化学方程式为:
(7)过程Ⅰ中每消耗1mol
 转移
转移
您最近一年使用:0次
【推荐2】某电镀铜厂有两种废水需要处理,一种废水中含有CN﹣离子,另一种废水中含有Cr2O72﹣离子。该厂拟定如图所示的废水处理流程。

回答以下问题:
(1)电镀铜时的阳极材料是_______ 。
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因__________ 。
(3)②中反应后无气体放出,该反应的离子方程式为_________ 。
(4)③中反应时,每0.4mol Cr2O72﹣转移2.4mol e﹣,该反应的离子方程式为______ 。
(5)铜是与人类关系非常密切的有色金属,已知常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生:2Cu+=Cu+Cu2+。大多数+1价铜的化合物是难溶物,如:Cu2O、CuI、CuCl、CuH等。
①写出CuH在过量稀盐酸中有气体生成的离子方程式______________ 。
②将CuH溶解在适量的稀硝酸中,完成下列反应的化学方程式:___ CuH +___ HNO3= __ Cu(NO3)2 +____ H2↑ +___ NO +___ H2O。

回答以下问题:
(1)电镀铜时的阳极材料是
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因
(3)②中反应后无气体放出,该反应的离子方程式为
(4)③中反应时,每0.4mol Cr2O72﹣转移2.4mol e﹣,该反应的离子方程式为
(5)铜是与人类关系非常密切的有色金属,已知常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生:2Cu+=Cu+Cu2+。大多数+1价铜的化合物是难溶物,如:Cu2O、CuI、CuCl、CuH等。
①写出CuH在过量稀盐酸中有气体生成的离子方程式
②将CuH溶解在适量的稀硝酸中,完成下列反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了CrFeAlMg的深度利用和Na+内循环。工艺流程如下:

回答下列问题:
(1)高温连续氧化工序中被氧化的元素是_______ (填元素符号)。
(2)工序①的名称为_______ 。
(3)滤渣Ⅰ的主要成分是_______ (填化学式)。
(4)工序③中发生反应的离子方程式为_______ 。
(5)物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为_______ ,可代替NaOH的化学试剂还有_______ (填化学式)。
(6)热解工序产生的混合气体最适宜返回工序_______ (填“①”“②”“③”或“④”)参与内循环。

回答下列问题:
(1)高温连续氧化工序中被氧化的元素是
(2)工序①的名称为
(3)滤渣Ⅰ的主要成分是
(4)工序③中发生反应的离子方程式为
(5)物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为
(6)热解工序产生的混合气体最适宜返回工序
您最近一年使用:0次



