按要求完成下列填空:
(1)O2-的结构示意图是_______ ;NH3的电子式是_______ 。
(2)CH4分子的空间结构为_______ ;黄铁矿的化学式是_______ 。
(3)下列给定的物质中:①NaCl晶体;②CH3COOH;③镁条;④氨气;⑤液态的HCl。属于非电解质的是_______ (填编号)。
(4)胆矾晶体遇浓硫酸变白,体现了浓硫酸的_______ 性。
(5)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是_______ L(设NA为阿伏加德罗常数的值)。
(1)O2-的结构示意图是
(2)CH4分子的空间结构为
(3)下列给定的物质中:①NaCl晶体;②CH3COOH;③镁条;④氨气;⑤液态的HCl。属于非电解质的是
(4)胆矾晶体遇浓硫酸变白,体现了浓硫酸的
(5)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
更新时间:2024-03-04 18:49:02
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1)①写出芒硝的化学式___________ ;
②写出环氧乙烷的结构简式___________ 。
(2)已知 与水反应生成乙炔,写出
与水反应生成乙炔,写出 的电子式
的电子式___________ 。
(3)写出向次氯酸钠溶液中通入少量 气体的离子方程式
气体的离子方程式___________ 。
(1)①写出芒硝的化学式
②写出环氧乙烷的结构简式
(2)已知
 与水反应生成乙炔,写出
与水反应生成乙炔,写出 的电子式
的电子式(3)写出向次氯酸钠溶液中通入少量
 气体的离子方程式
气体的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:___________ 。
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为___________ 。
(3)已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。若有64gCu被氧化,则被还原的HNO3的物质的量是___________ 。
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为___________ 。
(5)含有10个电子,9个质子的微粒___________ 。(至少2个)
(6)用电子式表示MgCl2的形成过程___________ 。
(7)配平___________
Mn2++PbO2+H+→MnO +Pb2++H2O
+Pb2++H2O
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为
(3)已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。若有64gCu被氧化,则被还原的HNO3的物质的量是
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
(5)含有10个电子,9个质子的微粒
(6)用电子式表示MgCl2的形成过程
(7)配平
Mn2++PbO2+H+→MnO
 +Pb2++H2O
+Pb2++H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.氢气是一种绿色能源,我国目前是全球最大的产氢国。
(1)氢元素有1H、2H和3H三种核素,它们含有相同的________。(双选)
| A.中子数 | B.质量数 | C.质子数 | D.核外电子数 |
A.氢分子中含有共价键
B. 氢分子的空间填充模型可表示为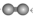
C. 氢气液化时,氢分子间平均距离变小
Ⅱ.“人靠田养,苗靠肥长”,粮食增产离不开氮肥。NH3是制备氮肥的原料之一。
(3)写出NH3的电子式
(4)下列关于 NH3的说法错误的是________。
| A.极易溶于水 | B.可用作制冷剂 | C.属于电解质 | D.属于共价化合物 |
Ⅲ.尿素[CO(NH2)2]是使用量最多的氮肥之一。
(5)尿素属于________。
| A.铵态氮肥 | B.硝态氮肥 | C.有机氮肥 | D.复合肥 |
Ⅳ.氮化硅(Si3N4)陶瓷材料可应用于原子反应堆。氮化硅可由下列反应制得:3SiO2+6C+2N2
 Si3N4+ 6CO,Si3N4中氮元素的化合价为-3。
Si3N4+ 6CO,Si3N4中氮元素的化合价为-3。(7)用单线桥标出上述反应中电子转移的方向和数目
(8)该反应的氧化剂是
(9)若生成0.25mol Si3N4,则反应过程中转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将24g氢氧化钠固体溶于水配成100mL溶液,其密度为1.219g·mL-1。
(1)该溶液中氢氧化钠的物质的量浓度为多少__ ?
(2)该溶液中氢氧化钠的质量分数为多少__ ?
(1)该溶液中氢氧化钠的物质的量浓度为多少
(2)该溶液中氢氧化钠的质量分数为多少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列填空:
(1)某金属氯化物 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为___________ g/mol
(2)一定量的液态化合物 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为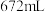 ,则反应前
,则反应前 的体积是
的体积是___________ mL,反应结束后,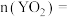
___________ mol
(3) 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
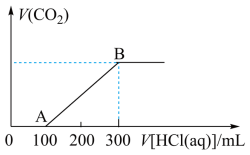
①OA段、AB段发生反应的化学方程式___________ 、___________ 。
②B点时,反应所得溶液中溶质的物质的量浓度是___________ mol/L
(1)某金属氯化物
 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为(2)一定量的液态化合物
 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为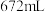 ,则反应前
,则反应前 的体积是
的体积是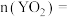
(3)
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
①OA段、AB段发生反应的化学方程式
②B点时,反应所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有如下物质:①铁丝 ②NaOH溶液 ③NaHSO4 固体 ④CO2 ⑤酒精 ⑥蒸馏水 ⑦CCl4 ⑧熔融的KNO3 ⑨红褐色的氢氧化铁胶体
(1)以上物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是_______ 。
(3)分离⑤与⑥的混合液所用的方法是_______ ;分离⑥与⑦的混合液所用的方法是_______ 。
(4)物质③溶于水的电离方程式为_______
(5)向⑨的溶液中逐渐滴加③的溶液,看到的现象是_______
(6)常选择有机溶剂CCl4萃取水溶液中的I2,选择CCl4做萃取剂的原因有:CCl4与水不反应也_______ ;I2在CCl4中溶解_______ (填“大于”或“小于”)I2在水中溶解。
(1)以上物质中,属于电解质的是
(2)已知蒸馏水有非常微弱的导电性,上述物质除⑥外,能导电的是
(3)分离⑤与⑥的混合液所用的方法是
(4)物质③溶于水的电离方程式为
(5)向⑨的溶液中逐渐滴加③的溶液,看到的现象是
(6)常选择有机溶剂CCl4萃取水溶液中的I2,选择CCl4做萃取剂的原因有:CCl4与水不反应也
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】了解物质分类,电解质和非电解质的组成与性质等是研究反应本质的前提。
有以下几种物质:
①铝箔 ②稀硝酸 ③氯化氢 ④氨气 ⑤熟石灰 ⑥二氧化碳 ⑦碳酸钡 ⑧硫酸铝。
请按要求回答下列问题。
(1)以上物质中能导电的是___________ (填序号,下同)。
(2)以上物质中属于电解质,但熔融状态下不能导电的是___________ 。
(3)将气体⑥通入⑤的水溶液中直至过量,可观察到___________ 现象。
(4)水溶液中⑧的电离方程式为:___________ 。
(5)溶液②和⑦反应的离子方程式:___________ 。
有以下几种物质:
①铝箔 ②稀硝酸 ③氯化氢 ④氨气 ⑤熟石灰 ⑥二氧化碳 ⑦碳酸钡 ⑧硫酸铝。
请按要求回答下列问题。
(1)以上物质中能导电的是
(2)以上物质中属于电解质,但熔融状态下不能导电的是
(3)将气体⑥通入⑤的水溶液中直至过量,可观察到
(4)水溶液中⑧的电离方程式为:
(5)溶液②和⑦反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空。
根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空。
A.吸水性 B.脱水性 C.强氧化性 D.强氧化性和酸性
(1)浓硫酸常用作干燥剂,说明浓硫酸具有_________ ;
(2)用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有_________ ;
(3)浓硫酸和浓硝酸都可以与铜反应,反应中浓硫酸和浓硝酸显示出_________ ;
 根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空。
根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空。A.吸水性 B.脱水性 C.强氧化性 D.强氧化性和酸性
(1)浓硫酸常用作干燥剂,说明浓硫酸具有
(2)用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有
(3)浓硫酸和浓硝酸都可以与铜反应,反应中浓硫酸和浓硝酸显示出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列各过程主要表现了浓硫酸的哪些性质?请将答案的序号分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体___________ 。
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸___________ 。
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体___________ 。
(4)常温下可以用铁或铝的容器贮存浓硫酸___________ 。
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末___________ 。
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体___________ 。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体
(4)常温下可以用铁或铝的容器贮存浓硫酸
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.以下实验中分别利用了硫酸的哪些性质?请将答案的序号分别填在横线上。
①脱水性②强氧化性③吸水性④强酸性
(1)浓硫酸干燥氯气;_______ ;
(2)适量浓硫酸与蔗糖混合后,体积膨胀颜色变黑;_______ ;
(3)浓硫酸与铜反应,溶液变蓝,且生成刺激性气体;_______ 。
Ⅱ.按要求写方程式
(4)写出实验室用亚硫酸钠和硫酸制取二氧化硫的化学方程式_______ ;
(5)写出铜和浓硫酸在加热条件下反应的化学方程式_______ 。
①脱水性②强氧化性③吸水性④强酸性
(1)浓硫酸干燥氯气;
(2)适量浓硫酸与蔗糖混合后,体积膨胀颜色变黑;
(3)浓硫酸与铜反应,溶液变蓝,且生成刺激性气体;
Ⅱ.按要求写方程式
(4)写出实验室用亚硫酸钠和硫酸制取二氧化硫的化学方程式
(5)写出铜和浓硫酸在加热条件下反应的化学方程式
您最近一年使用:0次



