按要求完成下列填空:
(1)某金属氯化物 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为___________ g/mol
(2)一定量的液态化合物 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为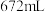 ,则反应前
,则反应前 的体积是
的体积是___________ mL,反应结束后,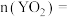
___________ mol
(3) 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
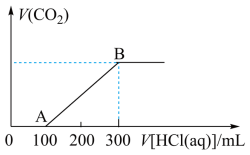
①OA段、AB段发生反应的化学方程式___________ 、___________ 。
②B点时,反应所得溶液中溶质的物质的量浓度是___________ mol/L
(1)某金属氯化物
 的摩尔质量为
的摩尔质量为 ,取该金属氯化物
,取该金属氯化物 配成水溶液,与足量
配成水溶液,与足量 溶液完全反应,生成
溶液完全反应,生成 白色沉淀。则金属M的摩尔质量为
白色沉淀。则金属M的摩尔质量为(2)一定量的液态化合物
 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: (注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为
(注:l表示液态,g表示气态),冷却后在标准状况下,测得生成物的体积为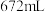 ,则反应前
,则反应前 的体积是
的体积是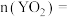
(3)
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 充分反应,再向上述所得溶液中逐滴滴加
充分反应,再向上述所得溶液中逐滴滴加 的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,(忽略液体混合带来的体积变化)所得气体的体积与所加盐酸的体积关系如图所示:
①OA段、AB段发生反应的化学方程式
②B点时,反应所得溶液中溶质的物质的量浓度是
更新时间:2023-11-24 14:04:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。回答下列问题:
。回答下列问题:
(1)该混合气体的平均摩尔质量:_______ 。
(2)混合气体中碳原子的个数:_______ 。(用 表示阿伏加德罗常数)
表示阿伏加德罗常数)
(3)将混合气体依次通过如图装置,最后收集在气球中。
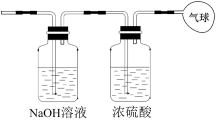
①气球中收集到的气体摩尔质量:_______ ;
②气球中收集到的气体的电子总数为_______ 。(用 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)
 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。回答下列问题:
。回答下列问题:(1)该混合气体的平均摩尔质量:
(2)混合气体中碳原子的个数:
 表示阿伏加德罗常数)
表示阿伏加德罗常数)(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体摩尔质量:
②气球中收集到的气体的电子总数为
 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1.某核素 的氯化物
的氯化物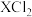 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数A______________ 。
(2)若X的核内中子数为20,求37g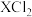 中所含质子的物质的量是
中所含质子的物质的量是______________
2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是______________ ,属于非电解质的是______________
(2)书写硫酸铁电离方程式:_______________________ 书写氯酸钾电离方程式:_______________________
 的氯化物
的氯化物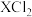 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:(1)X的质量数A
(2)若X的核内中子数为20,求37g
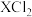 中所含质子的物质的量是
中所含质子的物质的量是2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是
(2)书写硫酸铁电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)质量相同的SO2和SO3的物质的量之比是_______ ,摩尔质量之比是_______ ,含氧原子个数比是_______ ,硫原子个数比是_______ 。
(2)1.204×1024个NH3分子所含的氢原子数_______ 。
(3)amol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为_______ 。
(4)32 g SO2标况下的体积为_______ L,含有_______ 个氧原子。
(5)1.204×1024个CO2分子的摩尔质量是_______ 。
(1)质量相同的SO2和SO3的物质的量之比是
(2)1.204×1024个NH3分子所含的氢原子数
(3)amol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为
(4)32 g SO2标况下的体积为
(5)1.204×1024个CO2分子的摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)3.4gNH3在标准状况下的体积为___ L。
(2)相同质量的O2和SO2,所含氧原子的物质的量之比为___ 。
(3)在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,混合气体的平均摩尔质量是___ 。
(2)相同质量的O2和SO2,所含氧原子的物质的量之比为
(3)在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,混合气体的平均摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是_______ 。
A.(2023·广东卷) 和
和 的混合物中含
的混合物中含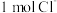 ,则混合物中质子数为
,则混合物中质子数为
B.(2022·浙江卷) 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
D.(2021·湖南卷) 与
与 在密闭容器中充分反应后的分子数为
在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH4和C2H4混合气体2.24L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA
 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是A.(2023·广东卷)
 和
和 的混合物中含
的混合物中含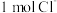 ,则混合物中质子数为
,则混合物中质子数为
B.(2022·浙江卷)
 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
D.(2021·湖南卷)
 与
与 在密闭容器中充分反应后的分子数为
在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH4和C2H4混合气体2.24L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)现有标准状况下以下五种物质:①44.8L甲烷(CH4)②6.02×1024个水分子③196g H2SO4④0.5mol CO2,它们中含分子数最多的是(填写序号,下同)____ ,原子数最少的是____ ,体积最大的是_____ 。
(2)①CO2 ②Na2CO3溶液 ③NaOH 固体 ④CaCO3 ⑤CH3COOH ⑥NH3·H2O ⑦乙醇 ⑧液态氯化氢
属于电解质的有___________________ ;非电解质的有___________________ 。(填序号)
(3)用双线桥法表示出下列反应的电子转移方向和数目_____________ 。3S+6KOH K2SO3+2K2S+3H2O
K2SO3+2K2S+3H2O
(2)①CO2 ②Na2CO3溶液 ③NaOH 固体 ④CaCO3 ⑤CH3COOH ⑥NH3·H2O ⑦乙醇 ⑧液态氯化氢
属于电解质的有
(3)用双线桥法表示出下列反应的电子转移方向和数目
 K2SO3+2K2S+3H2O
K2SO3+2K2S+3H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)有以下10种物质:①金 ②稀硫酸 ③液态HCl ④氨气 ⑤AgI胶体 ⑥二氧化碳 ⑦金属汞(俗称水银) ⑧Na2O2 ⑨熔融NaHSO4 ⑩氯气
按照表中提示的信息,把符合左栏条件的物质序号填入右栏相应的位置。
(2)在标准状况下,H2和C2H4的混合气体共11.2 L,质量为3.6 g,则两种气体的物质的量之和为_______ mol,其中H2为_______ mol,混合气体的摩尔质量为_______ g/mol。C2H4 的体积为_______ L
(3)物质分解方程式:2A=B↑+2C↑+2D↑,测得生成的混合气体在相同条件下的密度是H2密度的12倍,则A的摩尔质量为_______ g/mol。
(1)有以下10种物质:①金 ②稀硫酸 ③液态HCl ④氨气 ⑤AgI胶体 ⑥二氧化碳 ⑦金属汞(俗称水银) ⑧Na2O2 ⑨熔融NaHSO4 ⑩氯气
按照表中提示的信息,把符合左栏条件的物质序号填入右栏相应的位置。
| 序号 | 符合条件 | 物质序号 |
| Ⅰ | 混合物 | |
| Ⅱ | 电解质 | |
| Ⅲ | 能导电的物质 |
(3)物质分解方程式:2A=B↑+2C↑+2D↑,测得生成的混合气体在相同条件下的密度是H2密度的12倍,则A的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】向500mLNaOH溶液中投入10.8gAl,二者恰好完全反应后,则参加反应的NaOH的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2022年6月,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭,在酒泉卫星发射中心成功发射。火箭用偏二甲肼(C2H8N2)作燃料,四氧化二氮(N2O4)作推进剂,点燃后两者反应生成CO2、N2和H2O。已知:常温下,C2H8N2为无色液体,易溶于水;N2O4有剧毒,熔点为-11.2℃,沸点为21.2℃。
(1)C2H8N2的摩尔质量为_____ 。
(2)15gC2H8N2中含有的N原子数为_____ ,与_____ gN2O4中含有的氮原子数相同。
(3)常温下,将30gC2H8N2溶于水配成100mL溶液,该溶液的物质的量浓度为_____ mol/L;若要用其配制100mL1mol/L的C2H8N2水溶液,则需要量取原溶液的体积为_____ mL;若量取原溶液时俯视量筒读数,则配制的溶液浓度将_____ (填“偏高”或“偏低”)。
(1)C2H8N2的摩尔质量为
(2)15gC2H8N2中含有的N原子数为
(3)常温下,将30gC2H8N2溶于水配成100mL溶液,该溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有如下物质:①铜;② 溶液;③
溶液;③ 固体;④
固体;④ ;⑤酒精;⑥
;⑤酒精;⑥ ;⑦
;⑦ 溶液;⑧
溶液;⑧ 晶体。
晶体。
(1)以上物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)将②与⑦进行混合,该过程中发生的离子反应方程式是_______ 。
(3)向氢氧化钡溶液中加入物质③的溶液至 恰好沉淀完全,其离子方程式为
恰好沉淀完全,其离子方程式为_______ 。
(4)向②溶液中通入一定量的④,然后向该混合溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。

回答下列问题:
①AB段发生反应的离子方程式为_______ 。
②当加入35mL。盐酸时,产生 的体积(标准状况)为
的体积(标准状况)为_______ mL。
③原混合溶液中溶质及物质的量之比为_______ 。
 溶液;③
溶液;③ 固体;④
固体;④ ;⑤酒精;⑥
;⑤酒精;⑥ ;⑦
;⑦ 溶液;⑧
溶液;⑧ 晶体。
晶体。(1)以上物质中,属于电解质的是
(2)将②与⑦进行混合,该过程中发生的离子反应方程式是
(3)向氢氧化钡溶液中加入物质③的溶液至
 恰好沉淀完全,其离子方程式为
恰好沉淀完全,其离子方程式为(4)向②溶液中通入一定量的④,然后向该混合溶液中逐滴加入
 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示。
的体积(标准状况)关系如图所示。
回答下列问题:
①AB段发生反应的离子方程式为
②当加入35mL。盐酸时,产生
 的体积(标准状况)为
的体积(标准状况)为③原混合溶液中溶质及物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)胶体分散质粒子直径范围:___________ 。
(2)写出硫酸与氢氧化钡溶液反应的离子反应方程式:___________ 。
(3)写出盐酸与纯碱溶液反应的离子反应方程式:___________ ;
(4)写出碳酸钙与盐酸溶液反应的离子方程式:___________ ;
(5)写出Al2(SO4)3的电离方程式___________
(2)写出硫酸与氢氧化钡溶液反应的离子反应方程式:
(3)写出盐酸与纯碱溶液反应的离子反应方程式:
(4)写出碳酸钙与盐酸溶液反应的离子方程式:
(5)写出Al2(SO4)3的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,名不符实的一种物质是__________________________ 。
(2) “三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时):
__________________________________ ; _______________________________ 。
(3)“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是_____ (填序号)
A.Al B.Cu C.Fe D. Ag
(4)烧碱、纯碱溶液均可吸收CO2,当含0.4molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况,分别是:①_______ ②Na2CO3 ③___________ ④NaHCO3。将得到的固体重新溶解于水,在溶液中加过量的盐酸,使其充分反应后,得到溶液所含溶质的质量为__________ g。
(1)从物质的分类角度看,名不符实的一种物质是
(2) “三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时):
(3)“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是
A.Al B.Cu C.Fe D. Ag
(4)烧碱、纯碱溶液均可吸收CO2,当含0.4molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况,分别是:①
您最近一年使用:0次



