用 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是_______ 。
A.(2023·广东卷) 和
和 的混合物中含
的混合物中含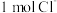 ,则混合物中质子数为
,则混合物中质子数为
B.(2022·浙江卷) 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
D.(2021·湖南卷) 与
与 在密闭容器中充分反应后的分子数为
在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH4和C2H4混合气体2.24L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA
 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是A.(2023·广东卷)
 和
和 的混合物中含
的混合物中含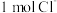 ,则混合物中质子数为
,则混合物中质子数为
B.(2022·浙江卷)
 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
D.(2021·湖南卷)
 与
与 在密闭容器中充分反应后的分子数为
在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH4和C2H4混合气体2.24L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA
2024高三·全国·专题练习 查看更多[1]
(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
更新时间:2024-01-06 08:11:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学是研究物质变化的科学。在120℃时分别进行如下四个反应(除S外其它物质均为气体):
①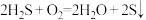
②
③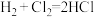
④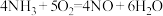
请回答下列问题
(1)请画出碳原子的结构示意图___________ ,O2-的电子式___________ 。
(2)以上所涉及的元素中,某元素的原子得到一个电子即可达到稳定结构,它的名称是___________ ,其原子中能量最高的电子在___________ 层上。(填电子层符号)
(3)以上所涉及物质中,按照物质分类的方法H2O,SO2,NO属于___________ 。
(4)已知元素有35Cl和37Cl两种同位素,相对原子质量为35.5,标准状况下5.6 L HCl气体中,H35Cl的质量为___________ g。
(5)120℃相同压强下,若将2 L H2S和5 L O2在密闭容器中按照反应②充分反应,恢复到原状态,则容器内气体的密度是相同条件下氢气的___________ 倍。
(6)若H2和Cl2的混合气体22.4 L(STP)发生反应③,产生的混合气体与氢氧化钠反应,则最多可消耗氢氧化钠的物质的量为___________ mol。
①
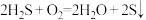
②

③
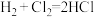
④
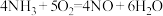
请回答下列问题
(1)请画出碳原子的结构示意图
(2)以上所涉及的元素中,某元素的原子得到一个电子即可达到稳定结构,它的名称是
(3)以上所涉及物质中,按照物质分类的方法H2O,SO2,NO属于
(4)已知元素有35Cl和37Cl两种同位素,相对原子质量为35.5,标准状况下5.6 L HCl气体中,H35Cl的质量为
(5)120℃相同压强下,若将2 L H2S和5 L O2在密闭容器中按照反应②充分反应,恢复到原状态,则容器内气体的密度是相同条件下氢气的
(6)若H2和Cl2的混合气体22.4 L(STP)发生反应③,产生的混合气体与氢氧化钠反应,则最多可消耗氢氧化钠的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
I.在紫外线作用下,氧气可转化为臭氧:3O2=2O3,低空臭氧的浓度过高时对人体有害,因此要尽量避免在阳光强烈照射的中午前后进行户外活动。
(1)O2转化为O3属于_______ (填“化学”或“物理”)变化;
(2)臭氧的摩尔质量为_______ ,已知:38℃、101kPa时,0.2molO3的体积为VL,则该条件下的气体摩尔体积为_______ ;
(3)1.6gO2和O3的混合气体中含有氧原子的数目为_______ (用NA表示阿伏加德罗常数的值)。
II.图中的几种物质是常见的盐,请回答下列问题。
(4)利用Na2CO3溶液和___________ 溶液反应,可制取NaOH。
(5)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的离子方程式为__________ ;
I.在紫外线作用下,氧气可转化为臭氧:3O2=2O3,低空臭氧的浓度过高时对人体有害,因此要尽量避免在阳光强烈照射的中午前后进行户外活动。
(1)O2转化为O3属于
(2)臭氧的摩尔质量为
(3)1.6gO2和O3的混合气体中含有氧原子的数目为
II.图中的几种物质是常见的盐,请回答下列问题。
(4)利用Na2CO3溶液和
(5)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44L,回答下列问题:
(1)该混合气体的平均摩尔质量为_________ 。
(2)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。
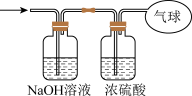
①气球中收集到的气体的相对分子质量为_______ 。
②气球中收集到的气体中,电子总数为________ (用NA表示阿伏加德罗常数的值)。
③气球的体积为________ L。
Ⅱ.物质的量是高中化学常用的物理量,请完成以下有关计算:
(3)0.5molNaOH中含有的电子数为_______ ,在_______ molNa2CO3中所含Na+数与上述0.5molNaOH所含Na+数目相等。
(4)现有14.4gCO,CO2和C2H4的混合气体,在标准状况下体积为8.96L。则混合气体中CO2的体积分数为________ 。
(5)物质A在一定温度下有分解反应A(s)=B(s)+C(g)+4D(g),若测得生成的气体的质量是同温同压下,相同体积氢气的10倍,且当所生成的气体在标况下的体积为22.4L时,所得B的质量为30.4g,A的摩尔质量为_______ 。
(1)该混合气体的平均摩尔质量为
(2)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。

①气球中收集到的气体的相对分子质量为
②气球中收集到的气体中,电子总数为
③气球的体积为
Ⅱ.物质的量是高中化学常用的物理量,请完成以下有关计算:
(3)0.5molNaOH中含有的电子数为
(4)现有14.4gCO,CO2和C2H4的混合气体,在标准状况下体积为8.96L。则混合气体中CO2的体积分数为
(5)物质A在一定温度下有分解反应A(s)=B(s)+C(g)+4D(g),若测得生成的气体的质量是同温同压下,相同体积氢气的10倍,且当所生成的气体在标况下的体积为22.4L时,所得B的质量为30.4g,A的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知1.28 g某气体氧化物(化学式为RO2)在标准状况下的体积为448 mL。
(1)该氧化物的摩尔质量为_________ 。
(2)R的相对原子质量为_________ 。
(1)该氧化物的摩尔质量为
(2)R的相对原子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据计算结果填空。
(1)1.8g水与_______ mol硫酸所含的分子数相等,它们所含氧原子数之比是_______ 。
(2)在标准状况下,448mL某气体的质量为0.64g,这种气体的摩尔质量为_______ 。
(3)含0.4mol Al2(SO4)3的溶液中,含_______ mol SO ,Al3+的物质的量
,Al3+的物质的量_______ (填“>”、“<”或“=”)0.8mol。
(1)1.8g水与
(2)在标准状况下,448mL某气体的质量为0.64g,这种气体的摩尔质量为
(3)含0.4mol Al2(SO4)3的溶液中,含
 ,Al3+的物质的量
,Al3+的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】含有1.204×1022个分子的HCl气体物质的量为_______ mol,在标准状态下所占的体积约为_______ L。
您最近一年使用:0次



