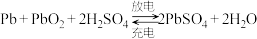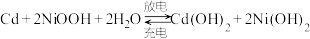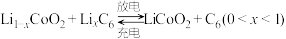高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是___________ 。
(2)放电时,正极发生___________ (填“氧化”或“还原”)反应。
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为___________ 。
(4)放电时,___________ (填“正”或“负”)极附近溶液的碱性增强。
 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:(1)高铁电池的负极材料是
(2)放电时,正极发生
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为
(4)放电时,
更新时间:2024-03-11 15:31:21
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】利用反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池。回答下列问题:
(1)该电池的负极材料是_______ ,发生_______ 反应(填“氧化”或“还原”);
(2)电解质溶液是_______ ;
(3)正极上出现的现象是_______ ;
(4)在外电路中,电子从_______ 极流向_______ 极。
(5)负极反应式:_______ ;正极反应式:_______ 。
(1)该电池的负极材料是
(2)电解质溶液是
(3)正极上出现的现象是
(4)在外电路中,电子从
(5)负极反应式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
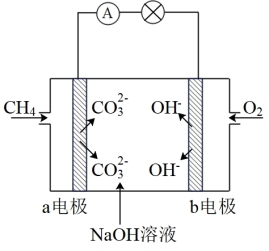
①电池的负极是____ (填“a”或“b”)电极,该极的电极反应式为___ 。
②电池工作一段时间后电解质溶液的pH____ (填“增大”“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应式为2CO+2CO -4e-=4CO2。
-4e-=4CO2。
①正极反应式是____ 。
②总电池反应式是___ 。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应式为2CO+2CO
 -4e-=4CO2。
-4e-=4CO2。①正极反应式是
②总电池反应式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I能源是现代社会发展的三大支柱之一,化学在提高能源的利用率和开发新能源中起到了重要的作用。电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是___________ (填字母)。
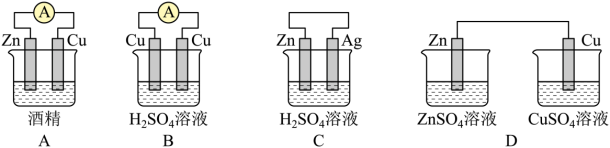
(2)该装置正极发生了___________ 反应(氧化或还原)。
(3)写出电极反应式:正极反应___________ ;负极反应___________ 。
II.铜与稀硝酸反应,生成标准状况下2.24升NO。请计算(写出计算过程):
(4)参加反应的铜的质量是___________ 。
(5)被还原的硝酸的物质的量是___________ 。
(1)下列装置中能够实现化学能转化为电能的是

(2)该装置正极发生了
(3)写出电极反应式:正极反应
II.铜与稀硝酸反应,生成标准状况下2.24升NO。请计算(写出计算过程):
(4)参加反应的铜的质量是
(5)被还原的硝酸的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电池的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Ag++Cl-=AgCl↓,B.Fe+Cu2+=Fe2++Cu,其中能设计成原电池的是______________ 。(填“A”或“B”)
(2)利用上述能构成原电池的反应,写出电极反应式。负极反应式______________ ,正极反应式______________ 。
(1)现有如下两个反应:A.Ag++Cl-=AgCl↓,B.Fe+Cu2+=Fe2++Cu,其中能设计成原电池的是
(2)利用上述能构成原电池的反应,写出电极反应式。负极反应式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图。请回答下列问题:

(1)电极X的材料名称是___ ;电解质溶液Y溶质的化学式是___ ;
(2)银电极为电池的___ 极,发生的电极反应为___ ;
(3)外电路中的电子是从___ 电极流向___ 电极。(填电极材料名称)。
(4)当有1.6g铜溶解时,银棒增重___ g。

(1)电极X的材料名称是
(2)银电极为电池的
(3)外电路中的电子是从
(4)当有1.6g铜溶解时,银棒增重
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
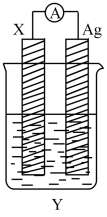
(1)电极X的材料是____ ;电解质溶液Y是____ 。
(2)X电极发生的电极反应式为____ ;Ag电极上发生的反应类型为____ 。
(3)外电路中的电子是从____ 电极流向____ 电极。Cu2+向___ (填“正极”或“负极”)移动。
(4)当Ag电极增重21.6g时,则X电极的质量减少____ 。
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O;B极:O2+4e-=2O2-。则A极是电池的____ 极;当B极参加反应的气体为112mL(标准状况),电路中转移电子的个数约为____ ,该电池的总反应为____ 。

(1)电极X的材料是
(2)X电极发生的电极反应式为
(3)外电路中的电子是从
(4)当Ag电极增重21.6g时,则X电极的质量减少
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O;B极:O2+4e-=2O2-。则A极是电池的
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】LiFePO4用于锂离子二次电池的电极材料,可由LiI和FePO4制备。
(1)FePO4难溶于水,制备方法如下:
Ⅰ.用稍过量的稀H2SO4溶解废铁屑,加热,搅拌,过滤;
Ⅱ.向滤液中加入一定量的H2O2;
Ⅲ.向含Fe3+的溶液加入Na2HPO4溶液,过滤后经进一步处理得FePO4。
①Ⅰ中反应进行完全的现象是__________________________________ 。
②用离子方程式说明H2O2的作用是_______________________________ 。
③Na2HPO4溶液显碱性的原因是_________________________ 。
(2)制备LiFePO4:将FePO4与LiI混合,在惰性气氛中加热,制得LiFePO4。化合物LiI中碘离子的作用是___________ 。
(3)锂离子二次电池的负极材料为金属锂和石墨的复合材料(石墨作为金属锂的载体),电池反应为:FePO4(s)+Li(s) LiFePO4(s),装置如下:
LiFePO4(s),装置如下:
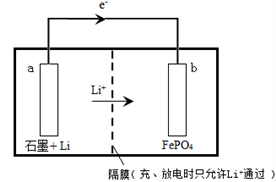
①该电池不能用电解质水溶液,原因是___________ 。
②放电时,b极的电极反应式是____________ 。
(1)FePO4难溶于水,制备方法如下:
Ⅰ.用稍过量的稀H2SO4溶解废铁屑,加热,搅拌,过滤;
Ⅱ.向滤液中加入一定量的H2O2;
Ⅲ.向含Fe3+的溶液加入Na2HPO4溶液,过滤后经进一步处理得FePO4。
①Ⅰ中反应进行完全的现象是
②用离子方程式说明H2O2的作用是
③Na2HPO4溶液显碱性的原因是
(2)制备LiFePO4:将FePO4与LiI混合,在惰性气氛中加热,制得LiFePO4。化合物LiI中碘离子的作用是
(3)锂离子二次电池的负极材料为金属锂和石墨的复合材料(石墨作为金属锂的载体),电池反应为:FePO4(s)+Li(s)
 LiFePO4(s),装置如下:
LiFePO4(s),装置如下:
①该电池不能用电解质水溶液,原因是
②放电时,b极的电极反应式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学电池在通讯、交通及日常生活中有着广泛的应用。
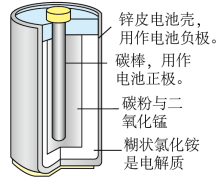
(1)右图是锌锰干电池的基本构造图,关于该电池的使用和性能,说法正确的是_____
A.该电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:2Ni(OH)2+Cd(OH)2 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2和Cd(OH)2均难于溶于但酸,以下说法正确的是________
A.以上反应是可逆反应 B.反应环境为碱性
C.电池放电时Cd做负极 D.是一种二次电池
(3)美国阿波罗的氢氧燃料电池是一种新型电源,其构造如图所示,a、b两个电极均由多孔的碳块组成,通入氢气和氧气由孔隙中逸出,并在电极表面发生电极反应而放电。
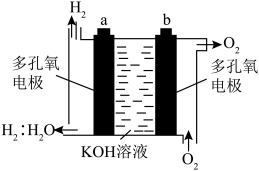
①其电极为a是_______ 极(填正或负)
②若为飞行员提供了360kg的水,则电路中通过了_______ mol电子。

(1)右图是锌锰干电池的基本构造图,关于该电池的使用和性能,说法正确的是
A.该电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:2Ni(OH)2+Cd(OH)2
 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O已知Ni(OH)2和Cd(OH)2均难于溶于但酸,以下说法正确的是
A.以上反应是可逆反应 B.反应环境为碱性
C.电池放电时Cd做负极 D.是一种二次电池
(3)美国阿波罗的氢氧燃料电池是一种新型电源,其构造如图所示,a、b两个电极均由多孔的碳块组成,通入氢气和氧气由孔隙中逸出,并在电极表面发生电极反应而放电。

①其电极为a是
②若为飞行员提供了360kg的水,则电路中通过了
您最近半年使用:0次