原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
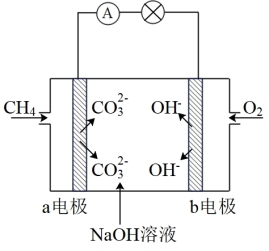
①电池的负极是____ (填“a”或“b”)电极,该极的电极反应式为___ 。
②电池工作一段时间后电解质溶液的pH____ (填“增大”“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应式为2CO+2CO -4e-=4CO2。
-4e-=4CO2。
①正极反应式是____ 。
②总电池反应式是___ 。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用碳酸锂和碳酸钠的熔融盐混合物作电解质,一氧化碳为负极燃气,空气与二氧化碳的混合气为正极助燃气,制得在650℃下工作的燃料电池,其负极反应式为2CO+2CO
 -4e-=4CO2。
-4e-=4CO2。①正极反应式是
②总电池反应式是
更新时间:2021-10-15 15:04:23
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】目前,第三代混合动力车已经投入市场,成为能源改革的典范。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:_____ 。
(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:_____ 。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH
 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.如图所示,某同学设计了一个燃料电池并进行电解实验,请回答下列问题:

(1)甲池中通____ (填“氧气”或“甲烷”)的是负极,其电极反应式为____ 。
(2)标准状况下,若有2.24L氧气参加反应,则乙装置中铁电极上生成气体的物质的量为____ mol。
(3)丙池中铜片上可观察到的现象为____ 。
II.据报道,我国已研制出“可充室温钠-二氧化碳电池”,如图所示,该电池的工作原理为4Na+3CO2 Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。

(4)放电时,钠箔为该电池的____ 极(填“正”或“负”):电解质溶液中ClO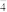 流向
流向____ (填“钠箔”或“多壁碳纳米管”)电极。
(5)充电时,多糖碳纳米管连接直流电源的____ (填“正”或“负”)极,其电极反应式为____ 。

(1)甲池中通
(2)标准状况下,若有2.24L氧气参加反应,则乙装置中铁电极上生成气体的物质的量为
(3)丙池中铜片上可观察到的现象为
II.据报道,我国已研制出“可充室温钠-二氧化碳电池”,如图所示,该电池的工作原理为4Na+3CO2
 Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
(4)放电时,钠箔为该电池的
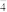 流向
流向(5)充电时,多糖碳纳米管连接直流电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于___ (“离子化合物”或“共价化合物”)。
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为___________ 。
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从___________ (填“a”或“b”)通入,该电池的正极是___________ (填“M”或“N”)电极,其中在N极发生的电极反应式是___________ 。
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为___________ L。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
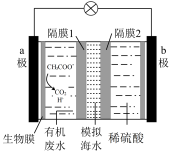
【推荐1】微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以 溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含
溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含 )。
)。
2.负极的电极反应式为:___________ 。
3.隔膜1为___________ 离子交换膜。
A.正 B.负
4.正、负极产生气体的物质的量之比为___________。
 溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含
溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含 )。
)。
| A.正 | B.负 | C.阳 | D.阴 |
3.隔膜1为
A.正 B.负
4.正、负极产生气体的物质的量之比为___________。
A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)CO还原脱硝技术可有效降低烟气中的NOx的排放量。回答下列问题:
CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g) △H1=—226kJ•mol—1
N2(g)+2O2(g)⇌2NO2(g) △H2=+68kJ•mol—1
N2(g)+O2(g)⇌2NO(g) △H3=+183kJ•mol—1
脱硝反应△H=______ ,该反应向正反应方向自发进行的倾向很大,其原因是_______ ,有利于提高NO平衡转化率的条件是(写出两条)________ 、___________ 。
(2)直接供氨式燃料电池是以NaOH溶液为电解质的.电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为_________ 。
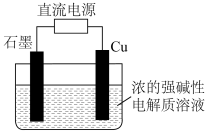
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出阳极的电极反应式_______ 。
CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g) △H1=—226kJ•mol—1
N2(g)+2O2(g)⇌2NO2(g) △H2=+68kJ•mol—1
N2(g)+O2(g)⇌2NO(g) △H3=+183kJ•mol—1
脱硝反应△H=
(2)直接供氨式燃料电池是以NaOH溶液为电解质的.电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出阳极的电极反应式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业制硝酸的主要反应为:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(l)△H
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H=_____ 。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
①反应在第2min到第4min时,O2的平均反应速率为_____ 。
②反应在第6min时改变了条件,改变的条件可能是_____ (填序号).
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)达到平衡状态的是_____ (填序号).
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
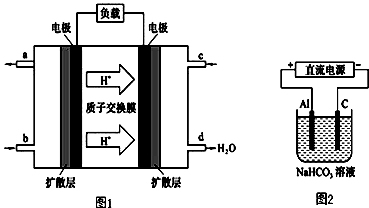
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为_____ 。
②该电池负极的电极反应式为:_____ 。
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是:_____ (用相关的离子方程式表示)。
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H=
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
| 浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
①反应在第2min到第4min时,O2的平均反应速率为
②反应在第6min时改变了条件,改变的条件可能是
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)达到平衡状态的是
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为
②该电池负极的电极反应式为:
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则该反应的化学方程式为____ ,反应进行到6s时,B的平均反应速率为____ mol·L-1·s-1。

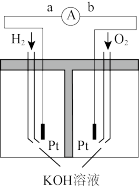
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。该装置负极反应方程式为____ 。
(3)写出乙烷和氯气反应生成一氯乙烷的化学方程式:____ ,该反应类型为____ ;写出乙烯和溴的四氯化碳溶液反应的化学方程式:____ ,该反应类型为____ 。
(1)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则该反应的化学方程式为

(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。该装置负极反应方程式为

(3)写出乙烷和氯气反应生成一氯乙烷的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量,体积均为1L),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
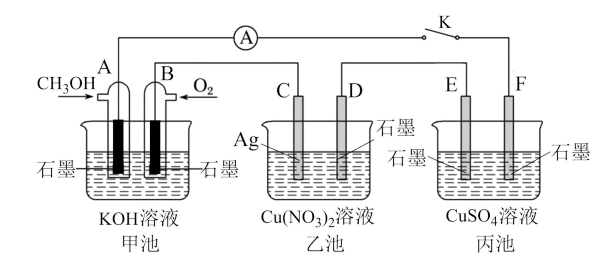
(1)甲、乙、丙三池中为原电池的是___________ (填“甲池”,“乙池”,“丙池”),A电极的电极反应式为___________ 。
(2)丙池中E电极为___________ (填“正极”、“负极”、“阴极”或“阳极”),该池总反应的化学方程式为___________ 。
(3)当甲池中B电极上消耗O2的体积为560mL(标准状况)时,乙池中C极质量理论上减轻___________ g,则丙池溶液的pH为___________
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___________ (填选项字母)。

(1)甲、乙、丙三池中为原电池的是
(2)丙池中E电极为
(3)当甲池中B电极上消耗O2的体积为560mL(标准状况)时,乙池中C极质量理论上减轻
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___________ (填选项字母)。
| A.Cu | B.CuO | C.CuCO3 | D.Cu(OH)2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】探究原电池原理并应用原电池原理制作多种电池,对现实生活具有重要的意义。
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:

①甲装置中铝片上的电极反应方程式为:_______ 。乙装置中铝片上的电极反应方程式式是_______ 。
②根据上述实验结果分析,下列说法正确的是_______ 。
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。该电池的负极材料为_______ ;该电池充电时,溶液的pH_______ (填“增大”、“减小”或“不变”)。
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:

铂电极b上的电极反应方程式式为_______ ,室温下,若该电池消耗1molH2时可提供电能257.4kJ的能量,则该燃料电池的能量转化率为_______ 。(已知:室温下,1molH2完全燃烧生成液态水时,释放286.0kJ的能量。)
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:

①甲装置中铝片上的电极反应方程式为:
②根据上述实验结果分析,下列说法正确的是
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。该电池的负极材料为
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:

铂电极b上的电极反应方程式式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,是原电池的装置图。请回答:___________ ; 在反应中溶液中的阴离子移向___________ (填“A”或“B”),反应进行一段时间后溶液C的pH___________ (填“升高”“降低”或“基本不变”)
(2)若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为___________ , B极电极反应式为___________ 。
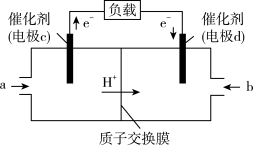
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:___________ (填“正极”或“负极”),若线路中转移2 mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为___________ L。
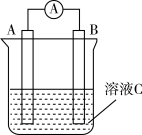
(2)若需将反应Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学电源在日常生活和工业生产中有着重要的应用。
I.如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题

(1)甲烷燃料电池负极反应式是______________________ 。
(2)石墨(C)极的电极反应式为______________________ 。
(3)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁极上生成的气体体积为___________ L;丙装置中阴极析出铜的质量为___________ g,一段时间后烧杯中c(Cu2+)___________ (填“增大”、“减小”或“不变”)
Ⅱ.“长征”火箭发射使用的燃料是液态偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分)。某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,回答相关问题:

(4)从a口加入___________ (填名称)。H+移动方向是___________ (填“A到B”或“B到A”)
(5)A极发生的电极反应式:______________________ 。
(6)若以该电池为电源用石墨做电极电解200mL0.5mol/L的CuSO4溶液,电解一段时间后,两极收集到相同体积(相同条件)的气体,则整个电解过程转移的电子的数目是___________ 。
I.如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题

(1)甲烷燃料电池负极反应式是
(2)石墨(C)极的电极反应式为
(3)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁极上生成的气体体积为
Ⅱ.“长征”火箭发射使用的燃料是液态偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分)。某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,回答相关问题:

(4)从a口加入
(5)A极发生的电极反应式:
(6)若以该电池为电源用石墨做电极电解200mL0.5mol/L的CuSO4溶液,电解一段时间后,两极收集到相同体积(相同条件)的气体,则整个电解过程转移的电子的数目是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.某化学兴趣小组利用如图所示的装置研究有关电化学的相关知识。当闭合该装置的开关时,观察到电流表的指针发生了偏转,已知丙为电解精炼铜装置。请回答下列问题:
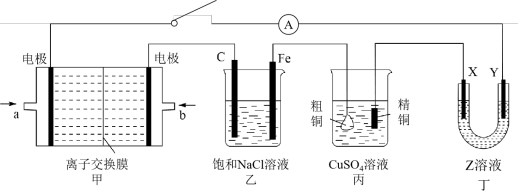
(1)若甲装置为甲醇(CH3OH)燃料电池,电解质溶液为KOH溶液,电极a上发生的电极反应式是___________ 。
(2)25℃,若乙装置中饱和NaCl溶液体积为500 mL,电路接通后一段时间,丙中精铜电极增重1.6 g,则此时乙装置中溶液pH为___________ (电解前后溶液体积变化忽略不计),阴极电极反应式为___________ ,欲使乙溶液复原需加入的物质是___________ (填名称)。
(3)若使用丁装置在铜牌上镀银,则铜牌应该与___________ (填“X”或“Y”)电极相连,Z溶液可选用___________ (填化学式)溶液。
II.纳米级Cu2O由于具有优良的催化性能而受到关注,采用甲醇燃料电池为电源,用离子交换膜控制电解液中的c(OH−)制备纳米Cu2O,其装置如图戊。
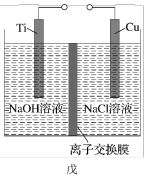
(4)装置戊中铜电极应连接甲醇燃料电池的___________ (填“正”或“负”)极,该电解池中离子交换膜为___________ (填“阴”或“阳”)离子交换膜。
(5)该电解池的阳极反应式为___________ 。

(1)若甲装置为甲醇(CH3OH)燃料电池,电解质溶液为KOH溶液,电极a上发生的电极反应式是
(2)25℃,若乙装置中饱和NaCl溶液体积为500 mL,电路接通后一段时间,丙中精铜电极增重1.6 g,则此时乙装置中溶液pH为
(3)若使用丁装置在铜牌上镀银,则铜牌应该与
II.纳米级Cu2O由于具有优良的催化性能而受到关注,采用甲醇燃料电池为电源,用离子交换膜控制电解液中的c(OH−)制备纳米Cu2O,其装置如图戊。

(4)装置戊中铜电极应连接甲醇燃料电池的
(5)该电解池的阳极反应式为
您最近一年使用:0次



