电解工作原理的实际应用非常广泛。
(1)电解精炼银时,阴极反应为_____ 。
(2)工业上为了处理含有 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有 和
和 沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法
沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误 的是_____(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
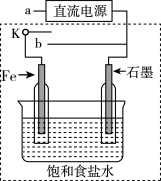
①当开关K与a连接时,两极均有气泡产生。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为_____ 。请写出此时Fe电极上的电极反应_____ 。
(4)1L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3mol 通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a=
通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a=_____ ,阳极生成_____ mol 。
。
(1)电解精炼银时,阴极反应为
(2)工业上为了处理含有
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有 和
和 沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法
沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法A.阳极反应: |
B.阴极反应: |
| C.在电解过程中工业废水由酸性变为碱性 |
| D.可以将铁电极改为石墨电极 |
(3)某同学设计了如图装置进行以下电化学实验。

①当开关K与a连接时,两极均有气泡产生。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1L某溶液中含有的离子如下表:
| 离子 |  |  |  |  |
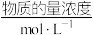 | 1 | 1 |  | 1 |
 通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a=
通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),则a= 。
。
更新时间:2024-03-15 15:50:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.如图所示是一个电化学装置的示意图。

请回答下列问题:
(1)图中甲池是_______ (填“原电池”、“电解池”或“电镀池”)。
(2)A(石墨)电极的名称是_______ (填“正极”、“负极”、“阴极”或“阳极”)。
(3)若把KOH溶液换成熔融Al2O3,传导O2-,写出通入CH3OH的电极的电极反应式:_______ 。
(4)乙池中反应的化学方程式为_______ 。
(5)当乙池中B极质量增加5.4g时,甲池中理论上消耗O2的体积为_______ L(标准状况),此时丙池中某电极析出1.6g某金属,则丙池中的某盐溶液可能是_______ (填字母)。
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
II.某课外活动小组进行电化学实验,请回答下列问题:
(6)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
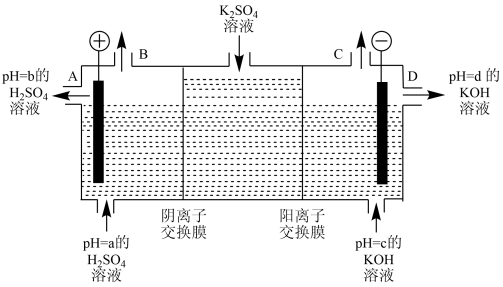
①该电解槽的阳极反应式为_______ ,通过阴离子交换膜的离子数_______ (填“>”“<”或“=”)通过阳离子交换膜的离子数;
②电解一段时间后,C口与B口产生气体的质量比为_______ 。

请回答下列问题:
(1)图中甲池是
(2)A(石墨)电极的名称是
(3)若把KOH溶液换成熔融Al2O3,传导O2-,写出通入CH3OH的电极的电极反应式:
(4)乙池中反应的化学方程式为
(5)当乙池中B极质量增加5.4g时,甲池中理论上消耗O2的体积为
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
II.某课外活动小组进行电化学实验,请回答下列问题:
(6)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。

①该电解槽的阳极反应式为
②电解一段时间后,C口与B口产生气体的质量比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为探究金属的腐蚀情况,某同学取一张用饱和NaCl溶液浸湿的石蕊试纸,平铺在一块金属板上,按如图所示的方法连接电路。
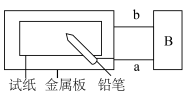
(1)若试纸为红色石蕊试纸,金属板为一锌片,B处为一灵敏电流计,接通电路,将铅笔芯(主要成分为石墨)放置在试纸上一段时间,发现电流计指针发生偏转,则铅笔芯与试纸接触处的电极反应式为__________________________ ,此时铅笔芯作____________ 极,铅笔芯与试纸接触处颜色____________ (填序号)。
a.变白 b.变蓝
c.不变 d.无法确定
(2)若金属板为一铂片,B处为一直流电源,接通电源后,①当试纸为红色石蕊试纸,用铅笔在试纸上写字,若出现蓝色字迹,则铅笔芯与试纸接触处的电极反应式为_________ ;
②当试纸为蓝色石蕊试纸,将铅笔芯放置在试纸上一段时间后,若接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色,则铅笔芯与试纸接触处的电极反应式为____________ 。
(3)上述(1)中的变化在本质上与钢铁的____________ 腐蚀类似,若将(1)中的锌换成铁,写出其总反应方程式: ___________________________ 。

(1)若试纸为红色石蕊试纸,金属板为一锌片,B处为一灵敏电流计,接通电路,将铅笔芯(主要成分为石墨)放置在试纸上一段时间,发现电流计指针发生偏转,则铅笔芯与试纸接触处的电极反应式为
a.变白 b.变蓝
c.不变 d.无法确定
(2)若金属板为一铂片,B处为一直流电源,接通电源后,①当试纸为红色石蕊试纸,用铅笔在试纸上写字,若出现蓝色字迹,则铅笔芯与试纸接触处的电极反应式为
②当试纸为蓝色石蕊试纸,将铅笔芯放置在试纸上一段时间后,若接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色,则铅笔芯与试纸接触处的电极反应式为
(3)上述(1)中的变化在本质上与钢铁的
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
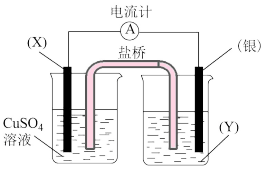
①电极X的材料是_______ ,电解质溶液Y是_______ 。
②银电极为电池的_______ 极,发生的电极反应式为_______ 。
(2)如图所示,甲、乙为相互串联的两个电解池。

①甲池为粗铜的精炼装置,A电极为_______ (填“阳极”或“阴极”),电极材料是_______ ,电极反应式为_______ 。
②乙池中Fe极的电极反应式是_______ ,若在乙池中滴入少量酚酞溶液,电解一段时间后,Fe极附近呈_______ 色。
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

①电极X的材料是
②银电极为电池的
(2)如图所示,甲、乙为相互串联的两个电解池。

①甲池为粗铜的精炼装置,A电极为
②乙池中Fe极的电极反应式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:
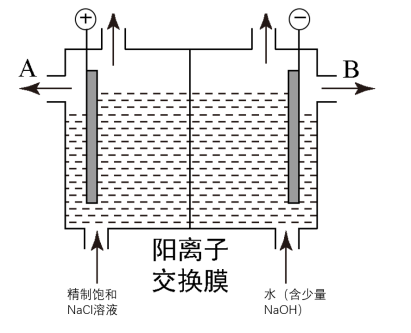
请回答下列问题:
(1)A极为电解槽的_______ 极(正、负、阴、阳),电极反应式为_______ 。
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许_______ (填离子符号,下同)通过,而不允许_______ 和气体通过。
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及 、
、 、
、 、
、 等杂质,因此必须精制。精制时所用试剂为①
等杂质,因此必须精制。精制时所用试剂为① ②
② ③
③ ④盐酸,这四种试剂的添加顺序为
④盐酸,这四种试剂的添加顺序为_______ (填序号)。
(4)若将标准状况下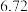 L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是
L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是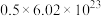 ,产物中得到了两种含氯化合物,写出该反应的离子方程式:
,产物中得到了两种含氯化合物,写出该反应的离子方程式:_______ 。

请回答下列问题:
(1)A极为电解槽的
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及
 、
、 、
、 、
、 等杂质,因此必须精制。精制时所用试剂为①
等杂质,因此必须精制。精制时所用试剂为① ②
② ③
③ ④盐酸,这四种试剂的添加顺序为
④盐酸,这四种试剂的添加顺序为(4)若将标准状况下
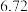 L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是
L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是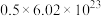 ,产物中得到了两种含氯化合物,写出该反应的离子方程式:
,产物中得到了两种含氯化合物,写出该反应的离子方程式:
您最近半年使用:0次
【推荐2】回答下列问题:
(1)用CCl4萃取碘水中的I2,萃取后单质碘主要在下层,理由是______ 。
(2)如图是氯气工业制法的实验室原理部分示意图,写出其化学方程式_____ 。
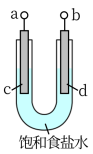
已知Na+向c极方向移动,则正极是___________ ,___________ 电极产生可燃性气体(选填a、b、c、d)。
(3)工业上将氯酸钠与一定量的氯化钾进行复分解反应从而制备氯酸钾。 。已知四种化合物的溶解度随温度变化曲线如下图所示。
。已知四种化合物的溶解度随温度变化曲线如下图所示。
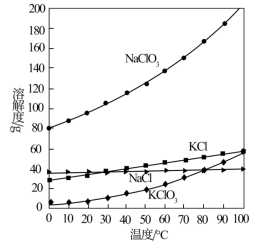
反应液经冷却至35℃以下时可析出氯酸钾晶体,原因是___________ 。在冷却降温析出KClO3过程中,常伴有NaCl析出,分离出母液,将粗氯酸钾进行进一步提纯的方法是___________ ,操作步骤是加水溶解,___________ ,洗涤,干燥,最后制得氯酸钾成品。
(1)用CCl4萃取碘水中的I2,萃取后单质碘主要在下层,理由是
(2)如图是氯气工业制法的实验室原理部分示意图,写出其化学方程式

已知Na+向c极方向移动,则正极是
(3)工业上将氯酸钠与一定量的氯化钾进行复分解反应从而制备氯酸钾。
 。已知四种化合物的溶解度随温度变化曲线如下图所示。
。已知四种化合物的溶解度随温度变化曲线如下图所示。
反应液经冷却至35℃以下时可析出氯酸钾晶体,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学是一门以实验为基础的自然科学,根据已有实验知识回答下列问题:
如图是某实验小组改进的中和反应反应热测定实验装置。组装仪器后,先在塑料瓶中加入 盐酸,然后通过注射器注入
盐酸,然后通过注射器注入 溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
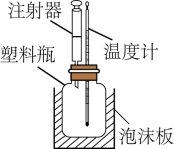
(1)塑料瓶外泡沫板的作用是__________ ,缺少的仪器是__________ 。
(2)已知稀溶液中, 盐酸与
盐酸与 溶液恰好完全反应时,放出
溶液恰好完全反应时,放出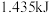 热量,写出表示
热量,写出表示 与
与 反应的中和热的热化学方程式
反应的中和热的热化学方程式__________ 。
(3) 可以用以下反应制备。在25℃和
可以用以下反应制备。在25℃和 时,由
时,由 和
和 完全反应生成2mol
完全反应生成2mol (均为气体),已知反应的
(均为气体),已知反应的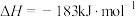 ,H—H的键能:
,H—H的键能: 、Cl—Cl的键能:
、Cl—Cl的键能: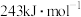 ,则H—Cl的键能为
,则H—Cl的键能为__________  。
。
(4) 还可以用电解饱和食盐水产生的
还可以用电解饱和食盐水产生的 和
和 制备。如图为电解饱和食盐水原理示意图。
制备。如图为电解饱和食盐水原理示意图。
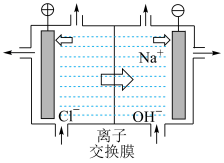
①写出电解饱和食盐水中阳极的电极方程式:__________ ;
②使用的交换膜是__________ (填“阴”或“阳”)离子交换膜;
③当装置转移 电子时,阴极产生气体的体积为
电子时,阴极产生气体的体积为__________ L(标准状况)。
如图是某实验小组改进的中和反应反应热测定实验装置。组装仪器后,先在塑料瓶中加入
 盐酸,然后通过注射器注入
盐酸,然后通过注射器注入 溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
(1)塑料瓶外泡沫板的作用是
(2)已知稀溶液中,
 盐酸与
盐酸与 溶液恰好完全反应时,放出
溶液恰好完全反应时,放出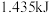 热量,写出表示
热量,写出表示 与
与 反应的中和热的热化学方程式
反应的中和热的热化学方程式(3)
 可以用以下反应制备。在25℃和
可以用以下反应制备。在25℃和 时,由
时,由 和
和 完全反应生成2mol
完全反应生成2mol (均为气体),已知反应的
(均为气体),已知反应的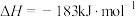 ,H—H的键能:
,H—H的键能: 、Cl—Cl的键能:
、Cl—Cl的键能: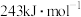 ,则H—Cl的键能为
,则H—Cl的键能为 。
。(4)
 还可以用电解饱和食盐水产生的
还可以用电解饱和食盐水产生的 和
和 制备。如图为电解饱和食盐水原理示意图。
制备。如图为电解饱和食盐水原理示意图。
①写出电解饱和食盐水中阳极的电极方程式:
②使用的交换膜是
③当装置转移
 电子时,阴极产生气体的体积为
电子时,阴极产生气体的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为 。
。
(1)放电时,正极的电极反应式:______ ,电解质溶液中硫酸的浓度______ (填“增大”“减小”或“不变”),当外电路通过1mol 时,理论上负极板的质量增加
时,理论上负极板的质量增加______ g。
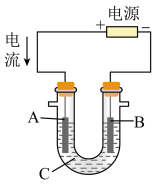
(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用______ 溶液,A电极的材料是______ ,B电极反应式是______ 。
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
 。
。(1)放电时,正极的电极反应式:
 时,理论上负极板的质量增加
时,理论上负极板的质量增加(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】甲醇是一种重要的化工原料和新型燃料。如图是甲醇燃料电池工作的示意图,连接电键K工作一段时间。
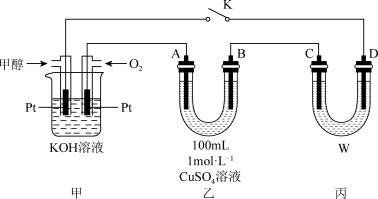
(1)甲中负极的电极反应式为_______ 。
(2)若丙中 为铝,
为铝, 为石墨,
为石墨, 溶液为稀
溶液为稀 ,若能使铝的表面生成一层致密的氧化膜,则
,若能使铝的表面生成一层致密的氧化膜,则 电极反应式为
电极反应式为_______ 。
(3)若 、
、 、
、 、
、 均为石墨,
均为石墨, 溶液为饱和氯化钠溶液:
溶液为饱和氯化钠溶液:
①工作一段时间后,断开电键K ,向乙中所得溶液加入 后恰好使电解质溶液复原,则丙中
后恰好使电解质溶液复原,则丙中 电极上生成的气体标况下的体积
电极上生成的气体标况下的体积_______ 。
②丙中为使两极产物不发生反应,可以在两极之间放置_______ (“阴”或“阳”)离子交换膜。
(4)若把乙装置改为精炼铜装置(粗铜含 、
、 、
、 、
、 、
、 等杂质),下列说法正确的是_______。
等杂质),下列说法正确的是_______。
(5)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:
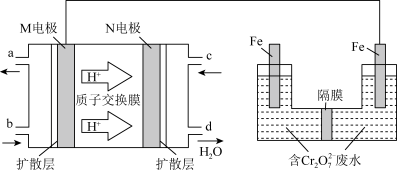
①M电极通入物质_______ (填 CH3OH或O2)
②电解池中阳极反应式为:_______ ; 转化为Cr3+的离子方程式为:
转化为Cr3+的离子方程式为: _______ 。

(1)甲中负极的电极反应式为
(2)若丙中
 为铝,
为铝, 为石墨,
为石墨, 溶液为稀
溶液为稀 ,若能使铝的表面生成一层致密的氧化膜,则
,若能使铝的表面生成一层致密的氧化膜,则 电极反应式为
电极反应式为(3)若
 、
、 、
、 、
、 均为石墨,
均为石墨, 溶液为饱和氯化钠溶液:
溶液为饱和氯化钠溶液:①工作一段时间后,断开电键K ,向乙中所得溶液加入
 后恰好使电解质溶液复原,则丙中
后恰好使电解质溶液复原,则丙中 电极上生成的气体标况下的体积
电极上生成的气体标况下的体积②丙中为使两极产物不发生反应,可以在两极之间放置
(4)若把乙装置改为精炼铜装置(粗铜含
 、
、 、
、 、
、 、
、 等杂质),下列说法正确的是_______。
等杂质),下列说法正确的是_______。| A.电解过程中,阳极减少的质量与阴极增加的质量相等 |
B. 为粗铜,发生氧化反应 为粗铜,发生氧化反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 |
| D.杂质都将以单质的形式沉淀到池底 |
 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:
①M电极通入物质
②电解池中阳极反应式为:
 转化为Cr3+的离子方程式为:
转化为Cr3+的离子方程式为:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I、依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
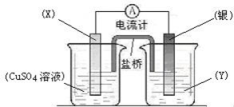
(1)电极X的材料是_______ ;电解质溶液Y是__________ 。
(2)银电极为电池的___ 极,发生的电极反应为____________ ; X电极上发生的电极反应为___________________ 。
(3)外电路中的电子是从_____ 电极流向_______ 电极。
II、如图所示,甲、乙为相互串联的两个电解池。请回答:
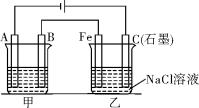
(1)甲池若为用电解原理精炼铜的装置,则A电极为________ 极,电极材料是________ ,电极反应为_______________________________ 电解质溶液可以是________________ 。
(2)乙池中Fe极电极反应为____________________________ 若在乙池中滴入少量酚酞溶液,电解一段时间后,铁极附近呈__________ 色。
(3)若甲池A极增重12.8 g,则乙池C(石墨)极放出气体在标准状况下的体积为___________ 。

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
II、如图所示,甲、乙为相互串联的两个电解池。请回答:

(1)甲池若为用电解原理精炼铜的装置,则A电极为
(2)乙池中Fe极电极反应为
(3)若甲池A极增重12.8 g,则乙池C(石墨)极放出气体在标准状况下的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有一套电化学装置,如下图所示,E 为沾有 Na2SO4溶液的滤纸,并加入几滴酚酞。A、B分别为Pt片,压在滤纸两端,R、S为电源的电极。M、N是用多微孔的 Ni 制成的电极材料,它在碱性溶液中可以视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的 KMnO4溶液,断开K,接通外电源一段时间后,C、D中有气体产生。
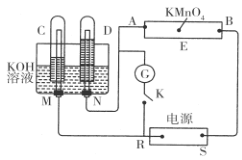
(1)S为________ (填“正”或“负”)极。
(2)A极附近溶液的现象是______________ , B 极附近发生的电极反应式为___________ 。
(3)滤纸上的紫色点向______ (填“A”或“B”)方移动。
(4)当 C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,D中的电极为________ (填“正”或“负”)极,电极反应式为___________________________ 。

(1)S为
(2)A极附近溶液的现象是
(3)滤纸上的紫色点向
(4)当 C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,D中的电极为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某实验小组尝试在钢制钥匙上镀铜。
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。
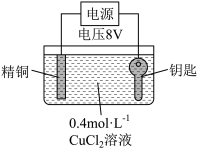
实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是_______ 。
(2)实验II中钥匙应与电源的_______ 极连接。
(3)钥匙表面产生的气体是_______ 。
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是________ 。
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是________ 。(已知CuOH是一种难溶于水的黄色固体)
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。

实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是
(2)实验II中钥匙应与电源的
(3)钥匙表面产生的气体是
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求填写下列空白
(1)写出Na2O2的电子式_____
(2)Al(OH)3在碱性溶液中的电离方程式为_____
(3)用离子方程式表示Na2S溶液呈碱性的原因_____
(4)在锌粒与稀硫酸的反应体系中,若滴加几滴CuSO4溶液,发现放出气体的速率明显加快,说明其原因:_____ ;若加入少量醋酸钠固体,发现放出气体的速率明显减慢,说明其原因_____ 。
(5)用惰性电极电解U形管中的饱和食盐水(已滴加酚酞),_____ 极附近溶液会变红。写出用惰性电极电解氯化铜溶液的化学反应方程式_____ 。
(1)写出Na2O2的电子式
(2)Al(OH)3在碱性溶液中的电离方程式为
(3)用离子方程式表示Na2S溶液呈碱性的原因
(4)在锌粒与稀硫酸的反应体系中,若滴加几滴CuSO4溶液,发现放出气体的速率明显加快,说明其原因:
(5)用惰性电极电解U形管中的饱和食盐水(已滴加酚酞),
您最近半年使用:0次



