反应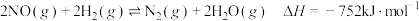 的反应机理如下.下列说法错误的是
的反应机理如下.下列说法错误的是
① (快)
(快)
②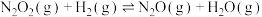 (慢)
(慢)
③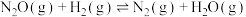 (快)
(快)
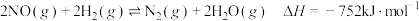 的反应机理如下.下列说法错误的是
的反应机理如下.下列说法错误的是①
 (快)
(快)②
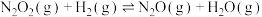 (慢)
(慢)③
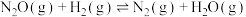 (快)
(快)| A.②反应的活化能最大 |
B.②中 与 与 的碰撞仅部分有效 的碰撞仅部分有效 |
C. 和 和 是该反应的催化剂 是该反应的催化剂 |
| D.总反应中逆反应的活化能比正反应的活化能大 |
更新时间:2024-04-05 21:15:30
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】对于反应2NO+2H2 N2+2H2O,科学家根据光谱研究提出如下反应历程:
N2+2H2O,科学家根据光谱研究提出如下反应历程:
第一步2NO N2O2 快反应
N2O2 快反应
第二步:N2O2+H2→N2O+H2O 慢反应
第三步:N2O+H2→N2+H2O 快反应
上述反应中可近似认为第二步反应不影响第一步反应的平衡,下列叙述正确的是
 N2+2H2O,科学家根据光谱研究提出如下反应历程:
N2+2H2O,科学家根据光谱研究提出如下反应历程:第一步2NO
 N2O2 快反应
N2O2 快反应第二步:N2O2+H2→N2O+H2O 慢反应
第三步:N2O+H2→N2+H2O 快反应
上述反应中可近似认为第二步反应不影响第一步反应的平衡,下列叙述正确的是
| A.第二步反应的活化能大于第三步的活化能 |
| B.N2O2起催化作用 |
| C.第三步反应中N2O与H2的每一次碰撞都是有效碰撞 |
| D.若第一步反应的ΔH<0,则升高温度,正反应速率减小,逆反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于一定条件下进行的化学反应:2SO3(g)  2SO2(g)+O2(g),改变下列条件,可以提高反应物活化分子百分数的是( )
2SO2(g)+O2(g),改变下列条件,可以提高反应物活化分子百分数的是( )
①增大压强②升高温度③加入催化剂④增大反应物浓度
 2SO2(g)+O2(g),改变下列条件,可以提高反应物活化分子百分数的是( )
2SO2(g)+O2(g),改变下列条件,可以提高反应物活化分子百分数的是( )①增大压强②升高温度③加入催化剂④增大反应物浓度
| A.①② | B.②③ |
| C.①②③ | D.①②④ |
您最近一年使用:0次



