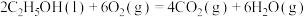下列有关热化学方程式的说法正确的是
A.甲烷的标准燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为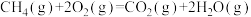  |
B.500℃、30MPa下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为: ,放热19.3kJ,其热化学反应方程式为:  |
C.已知稀溶液中 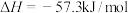 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
D.CO(g)的燃烧热是283.0kJ/mol,则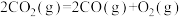 反应的 反应的 |
更新时间:2024-03-21 18:39:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】H2(g)+2ICl(g)→2HCl(g)+I2(g)能量曲线如图。描述正确的是


| A.反应①为放热反应,反应②为吸热反应 |
| B.若加入催化剂可降低反应热 |
| C.热化学方程式为H2(g)+2ICl(g)→2HCl(g)+I2(g)-218kJ |
| D.若反应的生成物为2HCl(g)+I2(s),则反应热数值将变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列热化学方程式书写正确的是( 的绝对值均正确)
的绝对值均正确)
 的绝对值均正确)
的绝对值均正确)A. (燃烧热) (燃烧热) |
B. (中和热) (中和热) |
C. (反应热) (反应热) |
D. (反应热) (反应热) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】含有11.2 g KOH的稀溶液与1 L 0.1 mol·L-1的H2SO4溶液反应,放出11.46kJ的热量,表示该反应的中和热的热化学方程式为
A.KOH(aq)+ H2SO4(aq)= H2SO4(aq)= K2SO4(aq)+H2O(l) △H=-11.46 kJ·mol-1 K2SO4(aq)+H2O(l) △H=-11.46 kJ·mol-1 |
| B.2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l) △H=-11.46 kJ·mol-1 |
C.KOH(aq)+ H2SO4(aq)= H2SO4(aq)= K2SO4(aq)+H2O(l) △H=-57.3 kJ·mol-1 K2SO4(aq)+H2O(l) △H=-57.3 kJ·mol-1 |
| D.2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l) △H=-114.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知热化学方程式:H+(aq)+OH-(aq)===H2O(l) ΔH1=-57.3 mol·L-1; H2SO4(浓)+NaOH(aq)===
H2SO4(浓)+NaOH(aq)=== Na2SO4(aq)+H2O(l) ΔH2=m,下列说法不正确的是
Na2SO4(aq)+H2O(l) ΔH2=m,下列说法不正确的是
 H2SO4(浓)+NaOH(aq)===
H2SO4(浓)+NaOH(aq)=== Na2SO4(aq)+H2O(l) ΔH2=m,下列说法不正确的是
Na2SO4(aq)+H2O(l) ΔH2=m,下列说法不正确的是| A.上述热化学方程式中的计量数表示分子数。 |
| B.ΔH1>ΔH2 |
C.ΔH2应为 H2SO4(浓)溶于水的能量变化与中和热之和。 H2SO4(浓)溶于水的能量变化与中和热之和。 |
| D.|ΔH1|〈|ΔH2| |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列化学反应的表示正确的是
A.尿素和NaClO溶液在碱性条件下反应: |
B.过量氨水和硫酸铜溶液反应: |
C.1-溴丙烷与氢氧化钠水溶液共热: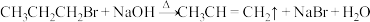 |
D.常温下N2H4为液体,具有很高的燃烧热(622.08 kJ⋅mol-1),肼燃烧的热化学方程式: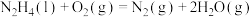 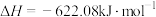 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH = -890.3 kJ·mol-1 |
B.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH= -38.6 kJ/mol 2NH3(g) ΔH= -38.6 kJ/mol |
| C.等量H2在O2中完全燃烧,生成H2O(l)比生成H2O(g)放出的热量多 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的ΔH不同 |
您最近一年使用:0次


 。则下列判断错误的是
。则下列判断错误的是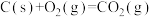

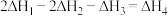
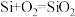


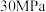 下,将
下,将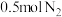 和
和 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成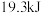 ,热化学方程式为:
,热化学方程式为:


 ;
;
 ;
;
 ,则
,则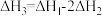

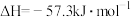 ,若将含
,若将含 的浓硫酸与含
的浓硫酸与含 的溶液混合,放出的热量大于
的溶液混合,放出的热量大于
 晶体和
晶体和 晶体于烧杯中混合搅拌,烧杯壁下部变冷,放出的气体使蓝色石蕊试纸变红
晶体于烧杯中混合搅拌,烧杯壁下部变冷,放出的气体使蓝色石蕊试纸变红 ,则稀醋酸与稀氢氧化钠溶液反应生成1mol水放出57.3kJ热量
,则稀醋酸与稀氢氧化钠溶液反应生成1mol水放出57.3kJ热量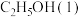 的燃烧热的热化学方程式为:
的燃烧热的热化学方程式为: