常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示。
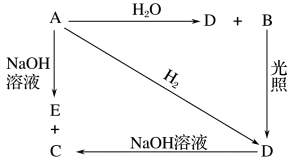
(1)请分别写出A、C、E的化学式:A_____ ,C________ ,E_______ 。
(2)写出A和H2O反应的化学方程式:_______________ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的气体A应用NaOH溶液吸收,其反应的化学方程式为______________________ 。
(4)漂白粉的有效成分是___________ (填化学式),漂白粉溶于水后,受空气中CO2的作用,产生有漂白、杀菌作用的次氯酸,反应的化学方程式为______________________ 。
(5)检验C中阴离子的方法______________________ 。

(1)请分别写出A、C、E的化学式:A
(2)写出A和H2O反应的化学方程式:
(3)通常情况下,为了防止污染环境,在做完实验后,多余的气体A应用NaOH溶液吸收,其反应的化学方程式为
(4)漂白粉的有效成分是
(5)检验C中阴离子的方法
更新时间:2024-03-22 08:52:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E是高中阶段学习的常见单质或化合物,单质A在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸。化合物C是漂白粉的有效成分。化合物D是淡黄色物质,可用于呼吸面具,可由一种活泼金属E在氧气中燃烧得到。回答问题:
(1)物质D的名称___________________ ,化合物D中非金属元素的化合价为________ 。
(2)化合物C能漂白的化学方程式为_______________________________________ 。
(3)单质B与水反应的离子方程式为_________________________________________ 。
(4)化合物D与水反应的离子方程式__________________________________________ 。
(5)若46gE与0.8mol 恰好完全反应, 则Na2O和Na2O2的物质的量之比为
恰好完全反应, 则Na2O和Na2O2的物质的量之比为_____ 。
(1)物质D的名称
(2)化合物C能漂白的化学方程式为
(3)单质B与水反应的离子方程式为
(4)化合物D与水反应的离子方程式
(5)若46gE与0.8mol
 恰好完全反应, 则Na2O和Na2O2的物质的量之比为
恰好完全反应, 则Na2O和Na2O2的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某兴趣小组模拟工业制漂白粉,设计了如下图所示的实验装置。已知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)2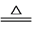 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O

回答下列问题:
(1)甲装置中仪器a的名称是_________________ ,MnO2在反应中所起的作用是_____________ 。
(2)装置乙中饱和食盐水的作用是_________________ 。
(3)①制取漂白粉的化学方程式是____________________ 。
②该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],其主要原因是____________________ 。
③为提高Ca(ClO)2的含量,可采取的措施是___________________ (任写一种即可)。
(4)漂白粉应密封保存,原因是__________ 、_________________ (用化学方程式表示)。
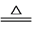 5CaCl2+Ca(ClO3)2+6H2O
5CaCl2+Ca(ClO3)2+6H2O
回答下列问题:
(1)甲装置中仪器a的名称是
(2)装置乙中饱和食盐水的作用是
(3)①制取漂白粉的化学方程式是
②该小组制得的漂白粉中n(CaCl2)远大于n[Ca(ClO)2],其主要原因是
③为提高Ca(ClO)2的含量,可采取的措施是
(4)漂白粉应密封保存,原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E是中学化学常见单质, X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系 (反应物和产物中的H2O已略去):
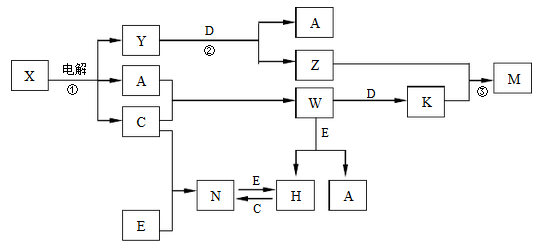
(1)Y的电子式为____________ ,构成E单质的元素在周期表中的位置_____________ 。
(2)反应②的离子方程式为_____________________ 。
(3)足量C通入Y的溶液中可得到一种常见的消毒剂。在该消毒剂中通入少量CO2可得一种酸式盐,从酸性强弱角度请你写出得到的结论:_______________________ 。
(4)①写出检验N中阳离子常用的试剂名称___________________ ,N也可用来净水,请写出相关离子方程式________________________ 。
②H的溶液在空气中久置,会变浑浊,请写出相关离子方程式_____________
(5)C可用来制取漂白粉,为测定漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为_____________ (不考虑生成CaSO4):
静置。待完全反应后,用1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为__________ (保留到小数点后两位)。

(1)Y的电子式为
(2)反应②的离子方程式为
(3)足量C通入Y的溶液中可得到一种常见的消毒剂。在该消毒剂中通入少量CO2可得一种酸式盐,从酸性强弱角度请你写出得到的结论:
(4)①写出检验N中阳离子常用的试剂名称
②H的溶液在空气中久置,会变浑浊,请写出相关离子方程式
(5)C可用来制取漂白粉,为测定漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为
静置。待完全反应后,用1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图是实验室制备氯气并进行一系列相关实验的装置。
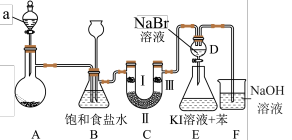
(1) 和浓HCl制备氯气的化学反应方程式为:
和浓HCl制备氯气的化学反应方程式为:___________ 。
(2)装置B中饱和食盐水的作用是___________ ;装置B也可以监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ依次放入:________ 。
(4)打开活塞将装置D中少量溶液加入装置E中,振荡。观察到的现象是___________ ,该现象___________ (填“能”或“不能”)说明溴的氧化性强于碘,原因是___________ 。

(1)
 和浓HCl制备氯气的化学反应方程式为:
和浓HCl制备氯气的化学反应方程式为:(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ依次放入:
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)打开活塞将装置D中少量溶液加入装置E中,振荡。观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某研究性学习小组设计如下实验装置利用氯气与石灰乳反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
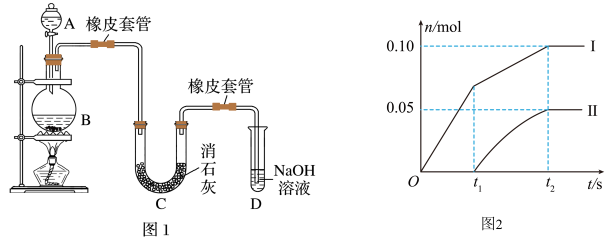
(1)A仪器的名称是_________ ,D的作用____________ 。
(2)漂白粉将在U形管中产生,其反应的化学方程式是____________________ 。
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是__________ ,有同学测出了反应后溶液中ClO-、 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。
a.图中曲线I表示_____________ 离子的物质的量随反应时间变化的关系。
b.所取石灰乳中含有Ca(OH)2的物质的量为______________ mol。
②试判断另一个副反应是(写出此反应方程式)__________________ ,为避免此副反应发生,可采取的措施是___________

(1)A仪器的名称是
(2)漂白粉将在U形管中产生,其反应的化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。a.图中曲线I表示
b.所取石灰乳中含有Ca(OH)2的物质的量为
②试判断另一个副反应是(写出此反应方程式)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有下列短周期元素的数据:(已知Be的原子半径为0.089nm)
(1)④号元素在元素周期表中的位置是___________
(2)①与⑥可构成原子个数比为1:1的化合物,写出该化合物的电子式___________
(3)第三周期元素简单离子半径最小的是___________ (写离子符号)。
(4)元素①的氢化物分别与⑤的单质反应的化学方程式为___________ 。该化合物是由___________ (填“极性”“非极性”)共价键形成的。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径/nm | 0.074 | 0.143 | 0.152 | 0.117 | 0.099 | 0.186 | 0.075 | 0.071 |
| 最高正化合价 | +3 | +1 | +4 | +7 | +1 | +5 | ||
| 最高负化合价 | -2 | -4 | -1 | -3 | -1 |
(2)①与⑥可构成原子个数比为1:1的化合物,写出该化合物的电子式
(3)第三周期元素简单离子半径最小的是
(4)元素①的氢化物分别与⑤的单质反应的化学方程式为
您最近一年使用:0次



